Общая микробиология - Шлегель Г. 1987
Перенос электронов в анаэробных условиях
Образование метана при восстановлении карбоната
Метан образуется при анаэробном разложении органических веществ. Его запасы весьма значительны; примерные подсчеты показывают, что 1-1,5% углерода, поступающего в результате минерализации органических веществ в виде СО2 в атмосферу, сначала попадает туда в виде метана и лишь затем превращается под воздействием гидроксильных радикалов (ОН) в СО, а потом в СO2. К экосистемам, в которых образуется метан, относятся большие площади, занятые тундрой и болотами (отсюда другое название метана-болотный газ); рисовые поля; осадки на дне прудов и озер; лиманы, марши и эстуарии; отстойники очистных сооружений и, наконец, желудки (рубцы) более чем 109 жвачных животных. В анаэробных условиях органические вещества сначала через ряд промежуточных этапов сбраживаются до ацетата, СO2 и Н2. Эти продукты метаболизма первичных и вторичных деструкторов используются метанобразуюгцими (метаногенными) бактериями.
Систематическое положение метанобразующих бактерий. По морфологии эти бактерии можно подразделить на палочковидные (Methanobacterium), кокковидные (Methanococcuś), сарциноподобные (Methanosarcind) и спирилловидные (Methanospirillum) (табл. 9.2). Метанобразующие бактерии составляют обособленную группу микроорганизмов. Они отличаются от других бактерий не только типом метаболизма, но и некоторыми признаками, касающимися состава клеточных структур. У них нет типичного пептидогликанового остова; Methanococcus обладает лишь белковой стенкой; у Methanospirillum имеется полипептидный чехол; клеточная стенка Methanosarcina barkeri построена из полисахарида, в состав которого входят уроновые кислоты, нейтральные сахара и аминосахара. Пенициллин не подавляет роста метанобразующих бактерий.
Таблица 9.2. Некоторые метанобразующие бактерии
|
Субстраты (доноры водорода) |
Автотрофный рост |
|
|
Мethanobacterium thermoautotrophicum |
H2 |
+ |
|
Methanobrevibacter (Methanobacterium) arboriphilicum |
Н2 |
+ |
|
Methanobrevibacter (Methanobacterium) ruminarttium |
Н2 или формиат |
- |
|
Methanobacterium formicicum |
Н2 или формиат |
+ |
|
Methanomicrobium (Methanobacterium) mobile |
Н2 или формиат |
- |
|
Methanococcus vannielii |
Н2 или формиат |
н. о.1 |
|
Methanococcus (Methanosarcina) mazei |
Н2, метанол, ацетат |
+ |
|
Methanosarcina barkeri |
Н2, метанол, ацетат, моно-, ди- и триметиламин |
|
|
Methanospirilium hungatii |
Н2 или формиат |
н.о. |
|
Methanothrix soehngenii |
Ацетат |
— |
1 н.о.-не определяли.
Цитоплазматическая мембрана содержит липиды, состоящие из эфиров глицерола и изопреноидных углеводородов (разд. 3.13). Рибосомы по своей величине сходны с рибосомами эубактерий (70S), однако последовательность оснований в рибосомных РНК, особенно в 16S-pPHK, существенно иная, чем у эубактерий. В отношении последовательности 16S-pPHK метанобразующие бактерии значительно сильнее отличаются, например, от Е. coli, чем цианобактерии. Кроме того, механизм трансляции нечувствителен к антибиотикам, подавляющим синтез белка у эубактерий. На основании этих, а также ряда других отличительных признаков метанобразующие бактерии относят к архебактериям (разд. 3.13).
Физиология. Метанобразующие бактерии - строгие анаэробы: кислород воздуха убивает их. У них нет ни каталазы, ни супероксиддисмутазы. Именно из-за высокой чувствительности этих бактерий к кислороду наши сведения об их физиологии, биохимии и экологии пока сравнительно скудны. Только после разработки специальных методов (например, метода Хангейта) появилась возможность пересевать и выделять метанобразующие бактерии без доступа кислорода.
Большинство до сих пор выделенных видов в чистой культуре способно использовать в качестве донора водорода Н2, а некоторые из них - также формиат, метанол, ацетат или метиламин. В ряде анаэробных экосистем основным субстратом для образования метана служит ацетат. Таким образом, круг субстратов очень узок.
Метанобразующие бактерии составляют последнее звено анаэробной пищевой цепи (стр. 266), в начале которой находятся полисахариды (целлюлоза, крахмал), белки и жиры. В этой цепи участвуют также 1) бактерии, сбраживающие целлюлозу до сукцината, пропионата, бутирата, лактата, ацетата, спиртов, СO2 и Н2; 2) ацетогенные бактерии, сбраживающие эти первичные продукты брожения до ацетата, формиата, СO2 и Н2 (эти вещества в свою очередь служат субстратами для метанобразующих бактерий).
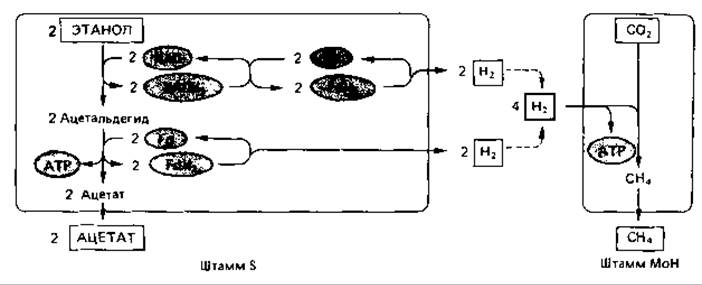
Рис. 9.6. Передача водорода от одного вида бактерий другому представлена здесь на примере компонентов культуры Methanobacterium omelianskii. На протяжении 30 лет ее считали чистой культурой, и только в 1967 г. она была разделена на штамм МоН (methanobacterium oxidizing hydrogen) и сопутствующий штамм S.
Метанобразующие бактерии, очевидно, находятся в тесном взаимодействии с бактериями, выделяющими водород (рис. 9.6). В микросреде обитания таких бактерий газообразный водород в свободном состоянии практически не встречается. Водород, выделяемый бактериями и растворенный в среде, сразу же поглощается метанобразующими видами. Известно, что высокое парциальное давление Н2 подавляет метаболизм и рост многих бактерий, образующих водород. Это означает, что не только метаногенные бактерии зависят от продуцентов Н2, но и те в свою очередь зависят от поглощающих Н2 метанообразователей. Таким образом, имеет место ассоциация типа мутуалистического симбиоза.
Метанобразующие бактерии способны активировать водород и осуществлять его окисление, сопряженное с восстановлением СO2. Поскольку клеточные вещества ряда видов могут синтезироваться из СO2 как единственного источника углерода, можно рассматривать способ существования этих бактерий как хемоавтотрофный. Для получения энергии СO2 используется в качестве акцептора водорода, что ведет к образованию метана:
Таким образом, метанообразование можно по аналогии с другими видами дыхания называть карбонатным дыханием. Поэтому метанобразующие виды характеризуют как анаэробные автотрофные бактерии, окисляющие водород:
![]()
Некоторые метанобразующие бактерии могут превращать в метан и окись углерода. При этом в качестве промежуточных продуктов образуются СО2 и Н2:
![]()
Биохимия образования метана и получения энергии. В биохимическом превращении Н2 и СO2 в метан или ацетата в метан и СO2 участвует ряд коферментов и простетических групп, которые до сих пор были найдены только у метанобразующих бактерий: производное деазарибофлавина F420, метаноптерин, метанофуран, никельтетрапиррольный фактор F430 и кофермент М (меркаптоэтансульфонат). Структура их показана на рис. 9.7. Наиболее вероятные пути образования метана из
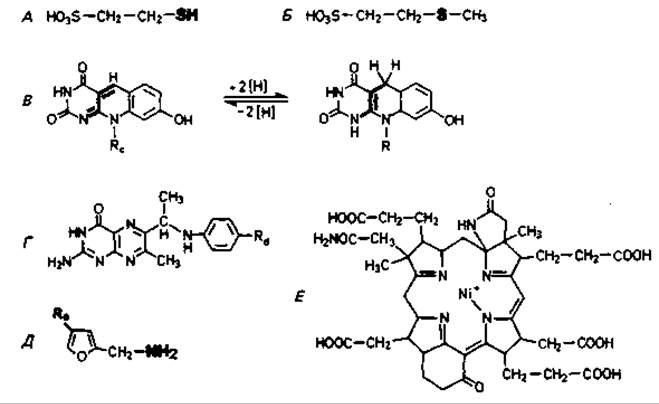
Рис. 9.7. Коферменты и простетические группы, имеющиеся у метаногенных бактерий. A - кофермент М; Б - метилкофермент М; В - F420, производное деазарибофлавина; Г - метаноптерин; Д - метанофуран; Е - фактор F430 после отделения от метил-СоМ-метилредуктазы. Реактивные группы соединений Г и E не указаны. Rc, Rd и Rc - различные боковые цепи, состоящие из нескольких компонентов.
ацетата и из СO2 + Н2 представлены на приведенных схемах:
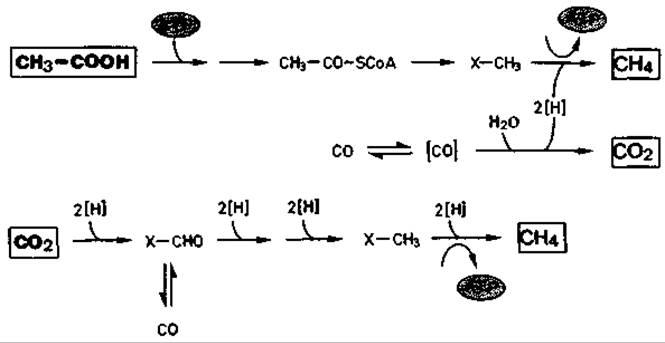
Пока мало что известно о ферментах, участвующих в отдельных реакциях. Вопрос о регенерации АТР тоже окончательно еще не выяснен. С точки зрения термодинамики только последняя реакция, приводящая к образованию метана, может сопровождаться синтезом АТР. Эксперименты на Methanosarcina barkeri - бактерии, способной также осуществлять реакцию СН3ОН + Н2→ СН4 + Н2O, дали следующие результаты. Добавление обоих субстратов к бактериальной суспензии приводило к выведению протонов, образованию АТР и синтезу метана. При участии метилтрансферазы метанол может прямо превращаться в метилкофермент М, при восстановлении которого образуется метан:
![]()
Восстанавливающий фермент - метил-СоМ-метилредуктаза - представляет собой мультиферментный комплекс, который содержит, в частности, белковые факторы F420, F430 и гидрогеназу. Вероятно, реакция всегда сопровождается выведением из клетки протонов, и создающийся в результате этого протонный потенциал доставляет энергию для регенерации АТР. Из этих результатов можно заключить, что вообще метанобразующие бактерии синтезируют АТР не путем фосфорилирования на уровне субстрата, а путем окислительного фосфорилирования в анаэробных условиях («анаэробное дыхание»).
Биохимия ассимиляции СO2. Автотрофная фиксация СO2 у метанобразующих бактерий [так же как и у сульфатредуцирующих (гл. 9.2) и ацетогенных (гл. 9.5) анаэробов, использующих водород] происходит без участия реакций рибулозобисфосфатного цикла. Путь синтеза клеточных веществ из СO2 идет через синтез ацетил-СоА и пирувата. Этапы этого пути были установлены с помощью радиоактивных соединений, а также в результате исследования ферментов Methanobacterium thermoautotrophicum. Механизмы этих превращений в настоящее время интенсивно изучаются.
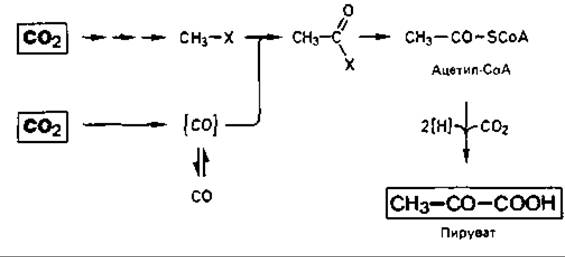
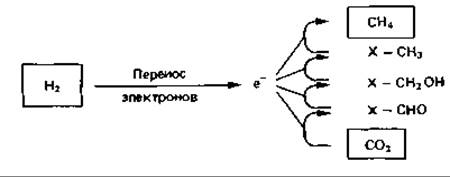
СО2 восстанавливается до метанола (в связанной форме). Вторая молекула СO2 восстанавливается с помощью СО-дегидрогеназы до СО. Восстановительные эквиваленты генерируются путем активации Н2 гидрогеназами и переносятся ферментами, реагирующими с фактором F420 или с NADP. Карбонилирование метил-Х ведет к образованию ацетил-Х, а в результате восстановительного карбоксилирования ацетил-СоА с помощью пируватсинтазы получается пируват, из которого известными путями синтезируются клеточные вещества.
Практическое значение метанобразующих бактерий. Отстойники, в которых происходит анаэробный распад органических веществ сточных вод населенных пунктов, относятся к обычному оснащению коммунальных водоочистных сооружений. В индустриальных странах гниение ила служит в первую очередь стабилизации первичного ила, а также активного ила, образующегося при аэробной очистке сточных вод. Метан, выделяющийся при гниении ила, частично используется определенными микроорганизмами, а частично его применяют в качестве топлива. В сельском хозяйстве применяют биогаз-ферментеры, а также ямы для навоза, чтобы сбраживать (с получением метана) экскременты животных вместе с отбросами, содержащими целлюлозу. Метод образования биогаза, основной частью которого является метан, обладает двумя важными преимуществами: во-первых, сохраняется содержащийся в экскрементах азот, а также те ценные качества удобрения, которыми обладает сероводородный ил; во-вторых, происходит образование биогаза (в основном метана), который может быть использован в качестве источника энергии как в сельскохозяйственном производстве, так и в домашнем хозяйстве.