Общая микробиология - Шлегель Г. 1987
Использование неорганических доноров водорода: аэробные хемолитотрофные бактерии
Окисление двухвалентного железа
Железобактерия Thiobacillus ferrooxidans окисляет двухвалентное железо до трехвалентного:
![]()
Эта бактерия очень похожа на Т. thiooxidans, жизнеспособна при pH среды до 2,5, однако энергию она получает не только за счет окисления восстановленных соединений серы, но и за счет окисления ионов Fe2+. Эта железобактерия обитает в кислых рудничных водах, содержащих сульфиды различных металлов, в том числе пирит (FeS2). С несомненностью установлено, что ацидофильные железобактерии способны к хемоавтотрофному образу жизни.
Недавно были также открыты термофильные штаммы тиобацилл, окисляющих железо и серу. Штаммы термофила Sulfolobus acidocaldarius тоже могут окислять двухвалентное железо1. Из почв, содержащих антимонит, удалось выделить автотрофную бактерию Stibiobacter senarmontii, способную окислять Sb3+ до Sb5+.
Выщелачивание металлов из руд. Способность некоторых ацидофильных бактерий, окисляющих железо и серу, превращать сульфиды и элементарную серу в водорастворимые сульфаты тяжелых металлов используется для выщелачивания бедных руд с целью получения меди, цинка, никеля, молибдена и урана. Метод выщелачивания уже применяют в широком масштабе для получения металлов из отвалов породы, однако область его применения, возможно, удастся распространить и на подземный горный промысел. В наиболее простом случае пропускают воду через толстый слой измельченного камня, содержащего руду [например, пирит (FeS2)] с сопутствующими сульфидами различных металлов, таких как Cu2S (халькозин), CuS, ZnS, NiS, MoS2, Sb2S3, CoS и PbS, а затем собирают раствор, содержащий сульфаты. После концентрирования такого раствора из него осаждают соответствующие металлы.
1 Двухвалентное железо окисляет также облигатно-автотрофная бактерия Leptospirillum ferrooxidans-Прим. ред.
Растворение сульфидов тяжелых металлов происходит благодаря совместному действию многих процессов: бактериального окисления восстановленных соединений серы (1) или элементарной серы (2) до серной кислоты, бактериального окисления Fe2 + до Fe3 + (3), и, наконец, химического окисления нерастворимых солей тяжелых металлов до растворимых сульфатов и серы (4):
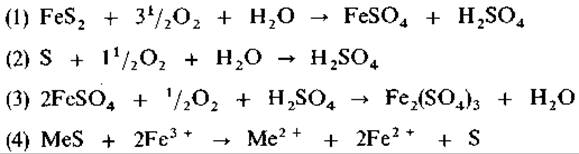
Таким образом, бактерии поставляют серную кислоту, а также регенерируют Fe3+; оба этих компонента расходуются при растворении руд.
Эти превращения осуществляют Thiobacillus thiooxidans и Т. ferrooxidans. Соответствующие штаммы бактерий отличаются необычной устойчивостью к довольно высоким концентрациям Сu2+, Со2+, Zn2+, Ni2+ и других ионов тяжелых металлов. В процессе выщелачивания участвуют также штаммы Sulfolobus, окисляющие серу и железо.
Другие железобактерии. К наиболее известным и легко распознаваемым железобактериям относятся также Gallionella ferruginea (см. рис. 3.16) и Leptothrix ochracea. Их можно найти, например, в дренажных трубах и горных ручьях среди хлопьев и толстых налетов оксидов железа. До последних лет оставалось неясным, способны ли эти бактерии использовать энергию, освобождающуюся при окислении Fe2+ в Fe3+, и расти как автотрофы. Недавно у представителей рода Gallionella была обнаружена рибулозобисфосфат-карбоксилаза; поэтому их относят сейчас к литоавтотрофным бактериям.
Бактерии окисляют не только железо, но и марганец. Хламидобактерия Leptothrix discophorus способна окислять Мn2+ до Мn4+. Однако еще не установлено точно, используется ли энергия, получаемая в результате такого окисления, для метаболических целей.
Облигатная хемолитоавтотрофия. Облигатная хемолитоавтотрофия - это выражение крайней степени приспособления и специализации организмов, окисляющих неорганические субстраты. Для того чтобы объяснить этот феномен, было предложено и проверено несколько гипотез:
1. Можно исходить из предположения, что цикл трикарбоновых кислот не является необходимым для окисления неорганического субстрата (подобно тому как он не нужен для брожения). В самом деле, восстановительные эквиваленты, получающиеся благодаря окислению неорганического субстрата, поступают в дыхательную цепь. Должны быть обеспечены лишь синтетические функции цикла трикарбоновых кислот (образование 2-оксоглутарата и сукцината). Но для этого фермент 2-оксоглутаратдегидрогеназа не нужен. Проверка показала, что у ряда облигатно-автотрофных бактерий его действительно нет. 2-Оксоглутаратдегидрогеназа не обнаруживалась и у многих факультативно-автотрофных бактерий, если клетки росли на среде с неорганическим источником энергии. Таким образом, мутант факультативно-автотрофной бактерии, потерявший способность к синтезу 2-оксоглутаратдегидрогеназы, вел бы себя как облигатно-автотрофный микроорганизм.
2. Поскольку нитрифицирующие бактерии, а также бактерии, окисляющие серу, сульфит и железо, обладают «разделенной» дыхательной цепью, вполне возможно, что у некоторых облигатных автотрофов в первом участке этой цепи имеется необратимый этап, который делает невозможной ее нормальную функцию, а именно окисление NADH2 (этот отрезок используется только для обратного переноса электронов). Такое нарушение обратимости цепи, возможно связанное с регуляцией ферментов, могло бы служить для сохранения восстановительной силы (NADH2), полученной с большими затратами энергии.
Пока еще не удалось дать единое объяснение облигатной автотрофии. Возможно, что у разных физиологических групп бактерий этот феномен имеет разные причины.