Биологические мембраны - А. Н. Огурцов 2012
Электрогенез биомембран
Механизмы межклеточной сигнализации
Регуляция кровоснабжения мускулатуры
На рисунке 157 представлена схема капилляра мышечной ткани. Эти кровеносные сосуды выстланы изнутри слоем эндотелиальных клеток (мезенхимного происхождения), образующих эндотелий. Эндотелий обёрнут снаружи клетками гладкой мускулатуры.
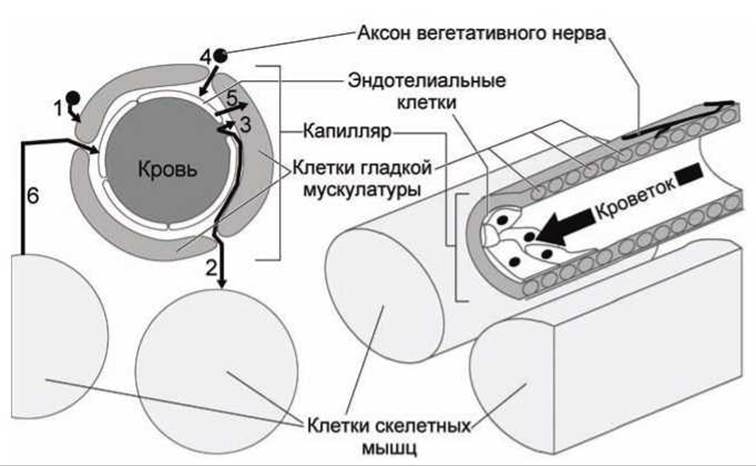
Рисунок 157 - Схема системы регуляции кровоснабжения
И эндотелиальные клетки, и клетки гладкой мускулатуры капилляров намного меньше клеток скелетных мышц (а сечение капилляров не бывает меньше сечения клетки скелетной мышцы). Оба этих типа клеток обслуживаются вегетативной (autonomie) нервной системой.
Клетки вегетативной нервной системы обычно используют один из двух трансмиттеров: ацетилхолин или норадреналин. Два других трансмиттера: адреналин и NО - также используются в системе регуляции кровоснабжения.
Нервные клетки, которые передают сигнал с помощью норадреналина в гладкую мускулатуру кровеносных сосудов (процесс (1) на рисунке 157), называются сосудосуживающими нервами, поскольку они стимулируют сужение капилляров. Клетки гладкой мускулатуры содержат а-адренергические рецепторы в плазматической мембране.
Связывание норадреналина с а-адренергическим рецептором активирует фосфолипазу PLCß, которая синтезирует ІР3, который, в свою очередь, запускает процесс переноса ионов кальция в цитозоль, что приводит к сокращению клетки гладкой мускулатуры, которая сжимает капилляр и уменьшает поток крови. Сосудосуживающие нервы используются для ограничения потока крови именно в те мышцы и органы, которые не используются организмом в данный момент.
Гормон адреналин химически подобен норадреналину, но более стабилен и может просуществовать в экзоплазме более минуты до ферментативного расщепления. Он выделяется в кровь эндокринными железами (надпочечниками) во время стресса и разносится по телу током крови. Тот адреналин, который диффундирует в клетки скелетных мышц (процесс (2) на рисунке 157), стимулирует начало гидролиза гликогена и синтеза глюкозо-6-фосфата.
В плазматической мембране клеток гладких мышц кровеносных сосудов внутри скелетной мускулатуры расположены ß-адренергические рецепторы, сопряжённые с ферментами аденилат циклаза. Однако, поскольку в этих клетках нет гликогена, то рост концентрации цАМФ, в ответ на связывание рецепторов с адреналином, активирует цАМФ-зависимую протеин-киназу А, которая фосфорилирует белки, стимулирующие расслабление клеток гладкой мускулатуры (процесс (3) на рисунке 157). В итоге, действие адреналина приводит к увеличению потока крови ко всем мышцам тела. При сильном стрессе количество адреналина в крови может вырасти настолько, что кровь "отхлынет" в мышцы от мозга и человек может упасть в обморок.
Так же как вегетативные сосудосуживающие нервы используются для ограничения потока крови в определённые ткани и органы, вегетативные сосудорасширяющие нервы используются для расширения кровеносных сосудов именно внутри тех мышц, которые организм собирается использовать.
Сосудорасширяющие нервы секретируют ацетилхолин (процесс (4) на рисунке 157), однако ни клетки гладкой мускулатуры, ни клетки эндотелия не имеют никотиновых ацетилхолиновых рецепторов. Вместо них эндотелиальные клетки имеют мускариновые ацетилхолиновые рецепторы. (Мускариновые рецепторы названы по имени их ингибитора мускарина, который содержится в ядовитых грибах Amanita muscarind).
Подобно а-адренергическим рецепторам мускариновый ацетил-холиновый рецептор сопряжён с Gq и PLCß, поэтому связывание с ацетилхолином приводит к росту цитозольной концентрации кальция. Эндотелиальные клетки не сокращаются при росте концентрации кальция, но они содержат фермент NO-синтаза, синтезирующий NO, который стимулируется ионами кальция.
Поэтому эндотелиальные клетки в ответ на появление ацетилхолина начинают синтезировать оксид азота (процесс (5) на рисунке 157). NО легко диффундирует сквозь мембраны эндотелиальных клеток и клеток гладкой мускулатуры. Попав внутрь клетки гладкой мускулатуры, NО связывается с рецептором, который активирует фермент гуанилат циклазу, что приводит к росту концентрации цГМФ.
Так же точно, как цАМФ для метаболического действия чаще всего использует в сигнальных цепях фермент цАМФ-зависимую протеин-киназу, которую поэтому часто называют просто протеин-киназа А, так и цГМФ использует для передачи своего сигнала цГМФ-зависимую протеин-киназу, которую также часто называют просто протеин киназа G. Протеин-киназа G в клетках гладкой мускулатуры активирует Са2+-АТФазу, которая начинает интенсивно выкачивать ионы кальция из цитозоля, клетка релаксирует и кровеносный сосуд расширяется.
Ферментами, которые прекращают действие трансмиттеров цАМФ и цГМФ являются цАМФ-диэстераза и цГМФ-диэстераза, соответственно.
Существует множество изоформ фермента цГМФ-диэстераза в различных тканях человеческого организма. Например, лекарственный препарат силденафил (sildenafil) (рисунок 158(a)), более известный под торговой маркой Виагра, является ингибитором цГМФ-диэстеразы пениса.
Действие силденафила не заметно, пока не синтезируется цГМФ. Когда же в ответ на локальное повышение концентрации NО, в клетках гладкой мускулатуры капилляров пениса начинается синтез цГМФ, то из-за блокирования цГМФ-диэстеразы, концентрация цГМФ значительно возрастает, что приводит к большей активации протеин-киназы G, большей активации Са+-АТФазы, снижению концентрации кальция, релаксации гладкой мускулатуры кровеносных сосудов, и, следовательно, большему притоку крови в ткань.
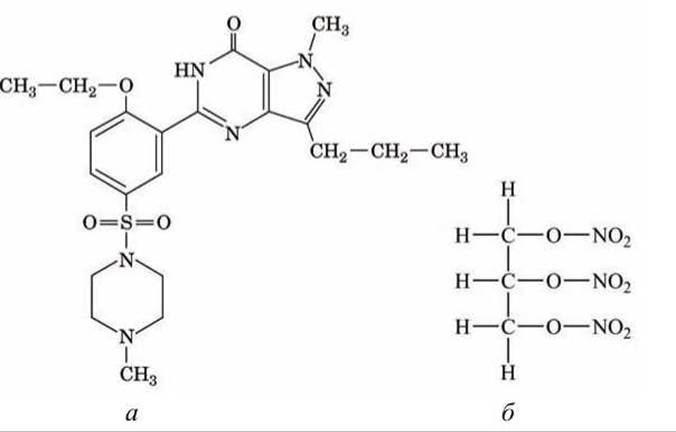
Рисунок 158 - Схемы молекул: а - силденафил (Виагра); б - нитроглицерин (тринитрат глицерина)
Рост мышечной массы интенсивно работающих мышц сопровождается ростом кровеносных сосудов во вновь образованных мышцах. Интенсивно работающие клетки скелетных мышц синтезируют фактор роста FGF (первоначально идентифицированный как фактор роста фибробластов, fibroblast growth factor, но, как оказалось впоследствии, действующий и на эндотелиальные, и на клетки гладкой мускулатуры) (процесс (6) на рисунке 157). Тирозин-киназный рецептор для FGF (аналогично PDGF-рецептору (рисунок 147)) через белки Ras и МАР- киназный каскад инициирует деление клетки, а, следовательно, и рост нового кровеносного сосуда.
Оксид азота. Открытие в 1987 году того факта, что NО является трансмиттером, объяснило терапевтическое действие нитроглицерина при стенокардии. Симптомом этого заболевания являются мышечные боли в сердце, которые возникают вследствие перегрузки сердечной мышцы. Нитроглицерин (рисунок 158(6)) током крови разносится по телу, медленно распадается, образуя NО, и расширяет кровеносные сосуды. Нагрузка на сердце падает, и боли в сердце уменьшаются.
Оксид азота в свободном виде существует в клетках только около пяти секунд, поэтому он не может диффундировать далеко от эндотелиальной клетки, в которой он был синтезирован. Именно поэтому NО является паракринным трансмиттером, который инициирует расслабление только тех клеток гладкой мускулатуры, которые соседствуют с эндотелиальной клеткой.
Эффект расширения кровеносных сосудов под влиянием ацетил-холина, происходящий только при наличии эндотелия - эпителиоподобных клеток, выстилающих внутреннюю поверхность всех сосудов, был обнаружен в 80-х годах XX века Р. Ферчготт (Robert Francis Furchgott). Первоначально трансмиттер, который выделялся эндотелиальными клетками в ответ не только на ацетилхолин, но и на многие другие внешние воздействия, приводящие к расширению сосудов, получил название сосудорасширяющий эндотелиальный фактор. Несколько позже было показано, что это вещество является оксидом азота (NО), и в клетках имеются особые ферментные системы, способные его синтезировать.
Оксид азота образуется ферментом NO-синтаза в результате окисления аминокислоты аргинина с одновременным синтезом другой аминокислоты цитруллина. Этот фермент был назван синтазой, а не синтетазой, поскольку для его работы не требуется энергия АТФ. NO-синтаза - это сложно устроенный фермент, представляющий собой гомодимер, состоящий из двух одинаковых белковых субъединиц, к каждой из которых присоединено несколько кофакторов, определяющих каталитические свойства фермента. Активность фермента проявляется только при объединении двух его субъединиц.
Активация NO-синтазы осуществляется кальций-связывающим белком кальмодулином. При повышении содержания ионов кальция в клетке он присоединяется к молекуле NO-синтазы, что приводит к активации фермента и синтезу NО.
Синтезировать и выделять NО способно большинство клеток организма человека и животных, однако наиболее изучены три клеточные популяции: эндотелий кровеносных сосудов, клетки нервной ткани (нейроны) и макрофаги - клетки соединительной ткани, обладающие высокой фагоцитарной активностью.
В связи с этим традиционно выделяют три основные изоформы NO-синтаз: нейрональную, макрофагальную и эндотелиальную (обозначаются соответственно как NO-синтаза I, II и III). Нейрональная и эндотелиальная изоформы фермента постоянно присутствуют в клетках и называются конститутивными, а вторая изоформа (макрофагальная) является индуцибельной - фермент синтезируется в ответ на определённое внешнее воздействие на клетку.
Активность конститутивных изоформ фермента прямо зависит от внутриклеточной концентрации ионов кальция или кальмодулина и, таким образом, повышается под влиянием различных агентов, приводящих к увеличению их уровня в клетке. Конститутивные изоформы NO-синтазы имеют преимущественно физиологическое значение, поскольку количество образуемого NО относительно невелико.
Индуцибельные изоформы NO-синтазы проявляют активность через некоторое время (как правило, 6-8 часов - время, необходимое для активации генов и начала синтеза фермента) после внешнего воздействия на клетки и продуцируют огромные (в 100-1000 раз больше, чем конститутивные изоформы фермента) количества NО. Поскольку высокие дозы NО токсичны для клеток, эта форма фермента считается патологической, в отличие от конститутивной. Активность индуцибельной NO-синтазы не зависит от уровня кальция или кальмодулина, поскольку, как полагают, кальмодулин постоянно и прочно связан с ферментом.
В настоящее время показано, что не только макрофаги, но многие другие клетки способны при определённых внешних воздействиях (в основном в условиях патологии) синтезировать индуцибельную форму NO-синтазы. Нейрональная и макрофагальная формы фермента находятся в клетках преимущественно в растворённом состоянии - в цитозоле, а эндотелиальная NO-синтаза обычно связана с клеточными мембранами.
Открытие оксида азота как высокоактивного межклеточного трансмиттера позволило прояснить многие неясные вопросы жизни клеточного сообщества в организме человека и животных. В 1992 году молекула NО в знак большого интереса к ней исследователей была названа молекулой года.
В 1998 году Роберт Ферчготт вместе с Луисом Игнарро (Louis J. Ignarró) и Феридом Мурадом (Ferid Murad) получили Нобелевскую премию по физиологии и медицине "за открытие роли оксида азота как сигнальной молекулы в регуляции сердечно-сосудистой системы".