МИКРОБИОЛОГИЯ Учебное пособие - 2012
ГЛАВА 9. ФИЗИОЛОГИЯ МИКРООРГАНИЗМОВ
9.3. ДЫХАНИЕ МИКРООРГАНИЗМОВ
Дыхание микроорганизмов представляет собой совокупность многочисленных биохимических реакций, в результате которых происходит перенос электронов, окисление субстрата и высвобождение энергии, необходимой для жизнедеятельности клетки.
Существуют два типа биологического окисления — прямое и непрямое. При прямом окислении неорганических веществ энергию получают автотрофные почвенные бактерии, которые с помощью ферментов оксидаз способны окислять атмосферным кислородом водород, метан, серу, аммиак и др. Непрямое окисление происходит путем переноса электронов от донора к акцептору. При биологическом окислении субстрата осуществляется одновременный перенос двух электронов; при этом от субстрата отщепляются также два протона. Такое окисление субстрата, сопровождаемое отщеплением атомов водорода, называется дегидрированием. Ферментные белки, отщепляющие от субстратов атомы водорода, называют дегидрогеназами.
Различают аэробное и анаэробное дегидрирование. При аэробном дегидрировании микроорганизмы используют в качестве конечного акцептора водорода атмосферный кислород. При аэробном дегидрировании происходит полное и неполное окисление. Конечными продуктами полного окисления являются вода и диоксид углерода. Неполное окисление приводит лишь к частичному освобождению энергии и образованию не полностью окисленных соединений — органических кислот (уксусной, лимонной, янтарной, яблочной, щавелевой и др.).
Анаэробное дегидрирование отличается от аэробного тем, что в качестве акцепторов водорода микроорганизмы используют не кислород, а некоторые окисленные неорганические соединения — нитраты, сульфаты, карбонаты, которые легко восстанавливаются до аммиака, сероводорода, метана.
9.3.1. Аэробное дыхание
Полное окисление органических соединений до СО2 и Н2О осуществляется микроорганизмами в процессе аэробного дыхания. Ниже приведено суммарное уравнение аэробного расщепления глюкозы:
![]()
При расщеплении глюкозы основным промежуточным продуктом обмена веществ является пировиноградная кислота (см. рис. 28), которая подвергается окислительному декарбоксилированию согласно уравнению:
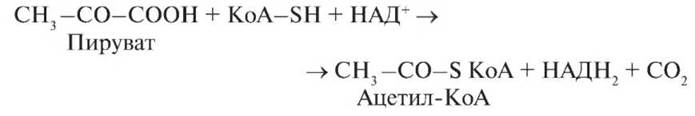
Помимо НАД+ и КоА—SH в данной реакции участвуют три других кофактора: тиаминпирофосфат (ТПФ), липоевая кислота и Mg2+. Образовавшийся при этом ацетил-КоА включается в цикл трикарбоновых кислот Кребса (ЦТК).
Окисление одной молекулы ацетил-КоА в цикле Кребса приводит к освобождению 2 молекул диоксида углерода и 8 протонов. Отданные субстратом протоны переносятся в цитоплазматическую мембрану у прокариотов или во внутреннюю мембрану митохондрий у эукариотов. В двойном липидном слое мембран локализованы компоненты дыхательной (электрон-транспортной) цепи, с помощью которых протоны и электроны переносятся на кислород. Важнейшими компонентами дыхательной цепи являются флавопротеины, железосерные белки, хиноны и цитохромы (рис. 26).
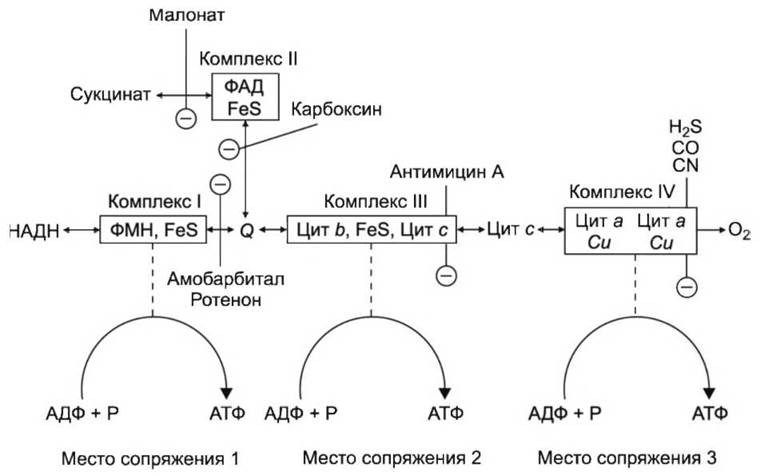
Рис. 26. Перенос электронов в цепи дыхательных ферментов
НАД(Ф)-зависимые дегидрогеназы катализируют отщепление водорода от молекул различных субстратов и передачу его на стартовый переносчик дыхательной цепи. После восстановления НАД(Ф)Н2 отщепляется от активного центра фермента и переносится к мембране, где передает протон флавиновой дегидрогеназе.
Флавопротеины представляют собой ферменты, простетической группой которых является флавинмононуклеотид (ФМН) или флавинадениндинуклеотид (ФАД). Реагирующими центрами служат два атома азота в изоаллоксазиновом кольце, каждый из которых связывается с одним [Н].
Железосерные белки (FeS) — окислительно-восстановительные системы, переносящие электроны. Эти белки содержат атомы железа, связанные как с серой аминокислоты цистеина, так и с неорганической дисульфидной серой. Участвующие в дыхательной цепи [2Fe + 2S] — центры способны переносить только один электрон. Железосерные белки содержатся в нескольких ферментных комплексах дыхательной цепи (I, II, III).
Хиноны — группа окислительно-восстановительных систем в дыхательной цепи. Во внутренней мембране митохондрий эукариотов и у грамотрицательных бактерий в цитоплазматической мембране имеется убихинон (кофермент Q), а у грамположительных бактерий — нафтохиноны. Хиноны способны переносить водород или электроны. В отличие от остальных переносчиков электронов хиноны не связаны со специфическими белками.
Цитохромы — окислительно-восстановительные системы, способные переносить только электроны. Простетической группой у цитохромов является гем. Центральный атом железа геминового кольца участвует в переносе электронов, меняя свою валентность:
![]()
В митохондиях эукариотов обнаружено пять цитохромов (b, c1, с, а, a3). Конечные цитохромы (а + a3), представляющие собой цитохромоксидазу, передают электроны на молекулярный кислород. Образование воды происходит при переносе 4 электронов на молекулу кислорода. Некоторые цитохромоксидазы переносят только 2 электрона, в результате чего появляется пероксид водорода. Впоследствии он расщепляется каталазой или пероксидазой.
Перенос водорода и электронов в дыхательной цепи сопровождается синтезом АТФ, т. е. реакции окисления сопряжены с реакциями фосфорилирования (места сопряжения 1, 2, 3 на рис. 26). Этот процесс, называемый окислительным фосфорилированием, протекает в мембранах при участии АТФ-синтазы. В основе фосфорилирования лежит разность окислительно-восстановительного потенциала донора и акцептора электронов (Eh). Обычно образование АТФ происходит на участках большей разности. При окислении 1 моля глюкозы по гексозодифосфатному пути и через цикл трикарбоновых кислот энергетический баланс составляет 38 АТФ.
Дыхательная цепь ингибируется или блокируется различными клеточными ядами. Амобарбитал, ротенон подавляют активность ФМН-дегидрогеназы, антимицин А блокирует перенос электронов между цитохромами b и с. Цианид, окись углерода и сероводород ингибируют только цитохромоксидазу.