Молекулярная биология: Структура и функции белков - Степанов В.М. 2005
Пептиды
Природные пептиды
Пептиды в природных объектах не только появляются в качестве промежуточных продуктов деградации белка, они часто играют самостоятельную физиологическую роль.
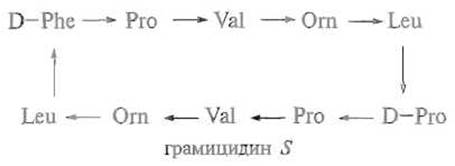
Пептидные антибиотики в большинстве своем синтезируются микроорганизмами по особому нематричному механизму и содержат в своем составе ряд небелковых аминокислот, а также D-изомеров. Многие из них являются циклопептидами. Среди таких антибиотиков отметим циклодекапептид грамицидин S — антимикробный агент широкого спектра действия:
Следует обратить внимание на присутствие в молекуле небелковой аминокислоты орнитина и D-изомера фенилаланина. Стрелки показывают направление пептидных связей в цикле.
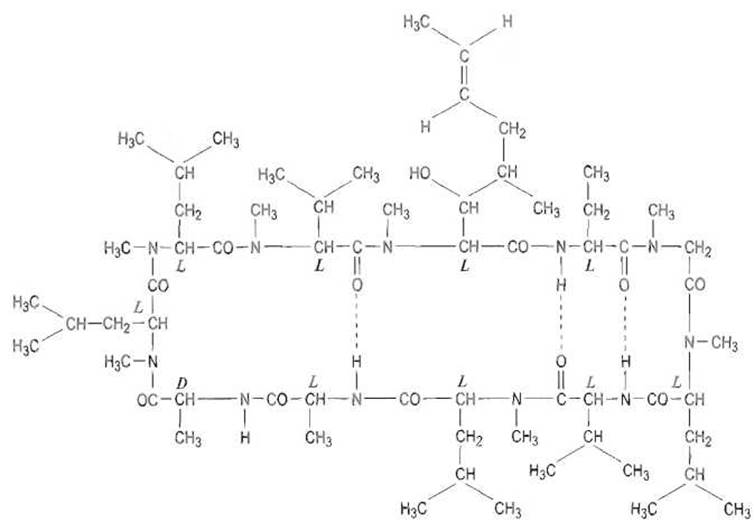
Эффективным иммунодепрессантом служит другой циклопептидный антибиотик — циклоспорин, содержащий N-метилированные и другие небелковые аминокислоты (непредельную оксиаминокислоту, а-аминомасляную кислоту, остаток D-аланина)
В последнее время обнаружены пептидные антибиотики, продуцируемые клетками животных, в особенности лимфоцитами. Они образуются по обычному пути биосинтеза белковых структур.
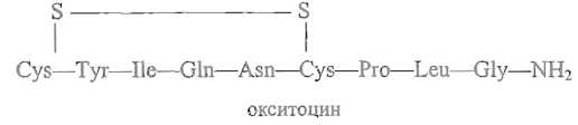
Пептидные гормоны, в более широком смысле — регуляторные пептиды, играют важнейшую роль в управлении метаболическими процессами в развитии организма, передаче сигналов. К их числу принадлежат некоторые короткие пептиды, например окситоиин, стимулирующий сокращение матки и лактацию:
Сходно построен нонапептид вазопресеин, подавляющий диурез и повышающий давление крови. Адренокортикотропный гормон (АКТГ), пептидная цепь которого состоит из 39 аминокислотных остатков, регулирует функцию надпочечников и может затрагивать целый ряд процессов, в том числе мотивацию, обучаемость, поведение а-Меланоцитостимулирующий гормон СН3СО—Ser—Tyr—Ser-Met—Glu—His—Phe—Arg—Trp—Gly—Lys—Pro—Val—NH2 контролирует образование меланина в пигментных клетках позвоночных, но влияет и на функционирование нервной системы, поведенческие реакции, а также развитие плода.
Следует отметить, что функции пептидных гормонов, как правило, многозначны, причем нередко в них удается выделить участки последовательности, ответственные за отдельные типы биологической активности. Для пептидных гормонов характерны процессы посттрансляционной модификации: в случае а-меланоцитостимулирующего гормона — ацетилирование а-NН2-группы и амидирование а-карбоксила.
Биосинтез пептидных гормонов и других регуляторных пептидов протекает так же, как и синтез белков. Многие физиологически активные пептиды, в особенности короткие, синтезируются в виде предшественников — полипептидов гораздо большей длины. Последние затем подвергаются ограниченномy протеолизу специфическими ферментами, которые, действуя на строго определенные связи, высвобождают активные пептиды. Так, энкефалины — пептиды, взаимодействующие с теми же рецепторами, что и морфин, и представляющие собой природные анальгетики, — синтезируются в виде предшественника, в пептидной цепи которого последовательности энкефалина Tyr—Gly—Gly—Phe—Leu или Tyr— Gly—Gly—Phe—Met повторяются несколько раз. Им предшествуют и за ними следуют пары Arg—Arg, которые служат сигналом для действия специфической протеиназы, расщепляющей пептидную связь после такой пары остатков аргинина:

Оба остатка аргинина затем отщепляются специфической кар- боксипептидазой, высвобождающей энкефалин.
Нередко оказывается, что пептиды могут имитировать поведение соответствующих пептидных фрагментов белка в его взаимодействии с другими биологическими молекулами, в частности с иными белками, например с рецепторами или структурообразующими молекулами. Так, пентапептидный фрагмент белка соединительной ткани ламинина, имеющий последовательность Туг—Не— Gly—Ser—Arg, ответствен за присоединение к этому белку клеток. Пентапептид такой же структуры способен препятствовать этому, по-видимому, блокируя рецепторы на поверхности клеток, вовлеченные во взаимодействие с ламинином.