ИММУНОЛОГИЯ - Ройт А. - Мир 2000
Глава 29. Иммунологические методы
ПОЛУЧЕНИЕ ЧИСТЫХ АНТИТЕЛ
В иммунологических исследованиях часто возникает необходимость в получении очищенных препаратов антител, т. е. антигенспецифичных либо неспецифичных иммуноглобулинов. Выделение неспецифичных иммуноглобулинов из сыворотки обычно проводят путем последовательного фракционирования белков, которое включает следующие этапы.
✵ Осаждение гамма-глобулинов в 30—50 % растворе сульфата аммония.
✵ Гель-фильтрация для получения молекул соответствующих размеров.
✵ Ионообменная хроматография с целью выделения молекул, несущих суммарный положительный заряд при нейтральном pH.
✵ Аффинная хроматография с использованием естественных лигандов иммуноглобулинов, например стафилококкового белка А (компонент клеточной стенки стафилококков, связывающийся с областью Сγ2 и Сγ3 большинства подклассов IgG, т. е. IgG1, IgG2 и IgG3).
Выделение антигенспецифичных иммуноглобулинов осуществляют методом аффинной хроматографии. Антиген «пришивают» к частицам сефарозы и связавшиеся с ним «чистые» антитела элюируют с иммуносорбента хаотропными агентами (например, тиоцианатом натрия) или буферным раствором (глицин—НCl или диэтиламина). Метод аффинной хроматографии применяют и для получения очищенных препаратов антигенов (рис. 29.15).
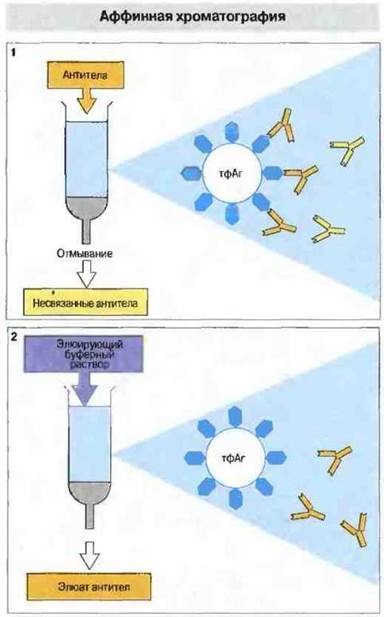
Рис. 29.15. С помощью аффинной хроматографии можно выделить чистую популяцию антител. 1. Готовят твердофазный иммуносорбент (тфАг), представляющий собой антиген, ковалентно связанный с инертной основой (например, частицами перекрестносшитого декстрана). Иммуносорбентом заполняют колонку, через которую пропускают смесь антител при физиологических условиях. Антитела к данному антигену связываются с иммуносорбентом, тогда как несвязавшиеся белки свободно проходят через колонку. 2. На следующем этапе связанные антитела элюируют с поверхности сорбента буферным раствором [например, ацетатным буфером (pH 3,0), диэтиламином (pH 11,5) или 3 М гуанидином-HCI], разрушающим связи в комплексе антиген-антитело. Этим методом можно получить и очищенные препараты антигенов, если использовать иммуносорбент, содержащий антитела. Аффинную хроматографию применяют также для выделения молекул других типов. Так, на поверхности частиц с «пришитым» лектином будут сорбироваться все молекулы, имеющие остатки определенных сахаридов; эти молекулы элюируют буферным раствором, содержащим свободные сахара, которые конкурируют с адсорбированными белками за участки связывания лектина.
Получение моноклональных антител
Другим способом получения индивидуальных антител определенной специфичности служит гибридомная технология - создание иммортализованной (бессмертной) линии клеток, продуцирующих антитела только одной специфичности, т. е. моноклональные (рис. 29.16). В такой культуре можно поддерживать антителообразование неопределенно долгое время. Моноклональные антитела несравнимо лучше соответствуют целям иммуноанализа, чем гетерогенные сыворотки, получаемые от иммунных животных, и поэтому нашли широкое применение в различных областях биологии в качестве высокоспецифичных зондов.
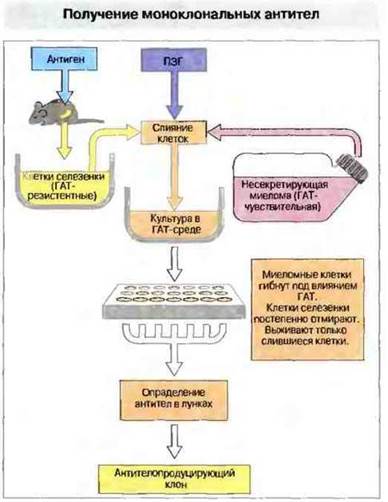
Рис. 29.16. Животных (обычно мышей или крыс) иммунизируют антигеном. Когда продукция антител достигает высокого уровня, из селезенки животных (могут быть использованы и лимфоузлы) готовят суспензию клеток Затем вызывают слияние спленоцитов с клетками миеломной линии, применяя для этой цели полиэтиленгликоль (ПЭГ) — агент, способствующий слиянию клеточных мембран. Процесс проходит успешно лишь у небольшого числа клеток. Клеточную смесь, содержащую слившиеся клетки, культивируют в ГАТ - среде, содержащей гипоксантин, аминоптерин и тимидин. Аминоптерин является высокотоксичным агентом, блокирующим один из метаболических путей - синтез пуринов. Клетки могут использовать обходный метаболический путь, если в среде присутствуют его интермедиаты - гипоксантин и тимидин. Спленоциты способны расти в ГАТ-среде, однако миеломные клетки в ней погибают, так как имеют метаболический дефект, не позволяющий использовать обходный путь синтеза пуринов. Клеточная суспензия, вносимая в ГАТ-среду, содержит спленоциты, клетки миеломы и слившиеся клетки. Спленоциты погибают в культуре естественным путем через 1-2 нед, клетки миеломы не выживают в ГАТ, слившиеся же клетки сохраняют жизнеспособность, поскольку сочетают свойства «бессмертной» миеломы и клеток селезенки, использующих обходный метаболический путь. Некоторые из слившихся клеток сохраняют также способность продуцировать антитела, как исходные спленоциты. Культуральную среду из всех лунок планшета, где зарегистрирован рост клеток, исследуют на присутствие антител желаемой специфичности (часто при помощи иммуносорбентного анализа). Культуры, продуцирующие антитела, клонируют, разводя клеточную взвесь при посеве с таким расчетом, чтобы на каждую лунку приходилась только 1 клетка. Эта клетка-предшественник дает начало формированию «бессмертного» клона, продуцирующего моноклональные антитела.
Эффективно продуцировать моноклональные антитела могут любые В-клетки, необходимо лишь сделать их для этого бессмертными и пролиферирующими. Чаще всего для этой цели получают гибридные клетки — путем слияния мышиных спленоцитов с миеломными В-клетками от мышей той же линии, не секретирующими собственных антител. Возможно также получить межлинейные или межвидовые гибриды, однако они часто нестабильны. Другой метод иммортализации — это трансформация клеток, например в случае В-клеток человека путем инфицирования вирусом Эпштейна-Барр.
Разработан также новый метод получения антител, основанный на использовании бактериофагов. С помощью этого интересного метода удается получить экспрессию на поверхности нитевидного бактериофага М13 вариабельных областей (Vh- и Vl) в виде фрагментов (Fv) антител, связывающих антиген с определенной специфичностью и авидностью. Располагая библиотекой таких экспрессируемых бактериофагом фрагментов, можно производить отбор (на основе взаимодействия со специфическим антигеном) фаговых частиц, продуцирующих тот или иной Fv-фрагмент. Кроме того, если данным бактериофагом инфицировать соответствующие бактерии, они начинают выделять Fv-белок в большом количестве в культуральную среду. Такой подход не требует обязательной иммунизации животных или человека (рис. 29.17).
Моноклональные антитела представляют собой четко определенный реагент, но они не обладают более высокой специфичностью по сравнению с поликлональной антисывороткой, распознающей антиген в результате взаимодействия иммуноглобулинов с его различными эпитопами.
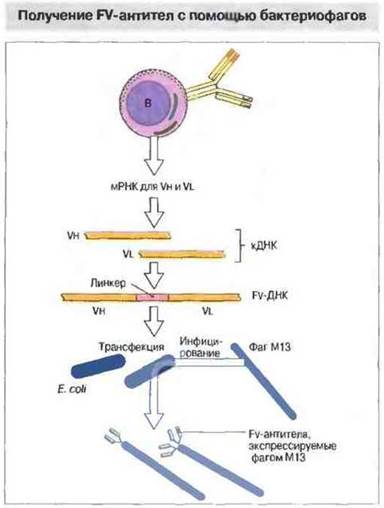
Рис. 29.17. Для получения Fv-фрагментов антител с помощью бактериофага вначале кДНК для Vh- и Vl-областей, синтезированную с использованием В-клеточной мРНК, амплифицируют методом полимеразной цепной реакции. Затем эти гены соединяют линкером, получая ген для Fv-фрагмента. Такой ген трансфицируют в бактерии (Е. соli), используя фазмидный вектор, содержащий лидерную последовательность и фрагмент гена, кодирующего белок оболочки фага М13. Далее, бактерии инфицируют фагом М13. Фаг реплицируется и экспрессирует на одном из своих полюсов Fv. Фаги нужной специфичности изолируют при помощи пэннинга на покрытых антигеном подложках и амплифицируют. Антигенспецифичные фаги можно использовать для инфицирования штаммов бактерий, обеспечивающих выделение Fv-белка в культуральную среду.