ИММУНОЛОГИЯ - Ройт А. - Мир 2000
Глава 8. Источники разнообразия антигенраспознающих структур
РЕКОМБИНАЦИИ ГЕНОВ Ig
Ген, кодирующий V-домен легкой цепи, образуется в результате рекомбинации V- и J-сегментов
Возможность изучения генов антител появилась благодаря разработке технологии рекомбинантных ДНК. С помощью этого метода было установлено, что константные и вариабельные области легких цепей кодируются двумя отдельными сегментами ДНК. В клетках, совсем не образующих антитела, эти генные сегменты расположены в отдаленных один от другого участках хромосомы, но при синтезе антител они оказываются в непосредственной близости. Однако даже в полностью дифференцированной В-клетке два этих сегмента непосредственно не соединяются — они разделены участком длиной примерно 1500 п.н. Между сегментами V и С в неперестроенной хромосоме, а также вплотную к сегменту V после внутрихромосомной рекомбинации располагается короткий участок ДНК, известный как соединительный сегмент J (от англ. joining). (J-сегмент не следует путать с J-цепью в молекулах IgM и димерного IgA.)
Система генов, кодирующих легкие цепи. Генный VK-сегмент кодирует V-область легких цепей с 1 по 95 позицию, а JK-сегмент — остальную часть V-области (рис. 8.8). В геноме человека обнаружен лишь один ген константной области легких цепей к-типа и 76 Ук-сегментов, из которых только 35 потенциально способны функционировать, 16 имеют минорные дефекты, а 25 представляют собой псевдогены. В результате рекомбинации ДНК в процессе дифференцировки лимфоидных клеток один из V-сегментов соединяется с одним из пяти J-сегментов. Впоследствии это может дать не менее (50 (т. е. 30 х 5) разных вариабельных областей k-цепей. Каждому V-сегменту предшествует участок ДНК, кодирующий короткий сигнальный (лидерный) пептид, который состоит из гидрофобных аминокислотных остатков и служит «опознавательным знаком» синтезируемой цепи для направления ее в эндоплазматический ретикулум, где лидерный пептид отщепляется. Далее начинается внутриклеточный процессинг молекулы иммуноглобулина с образованием его секретируемой формы и ее движение по пути выделения из клетки.
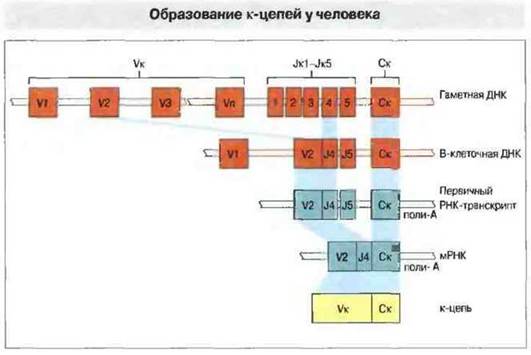
Рис. 8.8. В процессе созревания пре-В-клетки один сегмент из группы VK-сегментов (V1-Vn) гаметной ДНК в результате рекомбинаций сближается с одним из пяти Jk-сегментов (JK1-JK5). В зрелой В-клетке перестроенный сегмент ДНК транскрибируется е первичный РНК-транскрипт, который содержит длинную промежуточную последовательность добавочных J-сегментов и интроны. Путем сплайсинга (объединения) экзонов первичный РНК-транскрипт превращается в зрелую мРНК, которая транслируется в рибосомах в каппа (к)-цепи. Перестройка генов представлена здесь лишь одним из многих возможных типов рекомбинаций.
Локус генов легких λ-цепей у человека содержит набор V-генов и семь С-генов, причем каждый С-ген сопровождается расположенным рядом с ним J-геном. Несмотря на это отличие от локуса k-цепей, процесс рекомбинации V-J в локусе λ-цепей в общем весьма сходен с аналогичным процессом в локусе k-цепей (рис. 8.9).
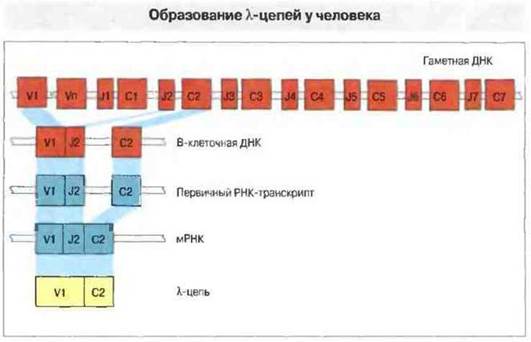
Рис. 8.9. В ходе дифференцировки В-клетки один из гаметных Vλ-ceгментов соединяется с Одним из J-сегментов, образуя ген V-J. Перестроенный таким образом ген транскрибируется в первичный РНК-транскрипт, содержащий интроны (некодирующие сегменты), экзоны (кодирующие белок) и полиаденилатный «хвост» (поли-А). В результате сплайсинга из первичного РНК-транскрипта вырезаются интроны, а зкзоны образуют молекулу мРНК, с которой затем транслируется белок.
После рекомбинации сегментов V и J между перестроенными VJ-генами и С-геном еще сохраняется интрон (некодирующая промежуточная последовательность). Весь этот отрезок ДНК (от лидерной последовательности до 3'-конца С-гена, включая интроны) полностью транскрибируется в гетерогенную ядерную РНК (гяРНК) — предшественник мРНК, из которого после удаления нитронов и соединения экзонов образуется молекула мРНК, способная транслироваться в белок.
Ген, кодирующий V-домен тяжелой цепи, образуется в результате рекомбинации V-, D- и J-сегментов
Вариабельные области тяжелых цепей, как и легких, кодируются генными сегментами V и J. Дополнительный вклад в разнообразие антител вносит третий генный сегмент, D (от англ. diversity— разнообразие) (рис. 8.10). Он высоковариабелен по нуклеотидной последовательности и по числу кодонов. В молекулах антител к декетрану он определяет два аминокислотных остатка; в антителах к фосфорилхолину - вставку до восьми дополнительных аминокислотных остатков, в антителах к левану этот участок аминокислотной последовательности полностью отсутствует. Несколько соединенных последовательно D-сегментов могут образовать увеличенную D-область с тремя потенциальными рамками считывания без стоп-кодонов, что дополнительно увеличивает разнообразие тяжелых цепей. В гаметных генах к настоящему времени идентифицировано всего 30 D-сегментов. Как установлено, 14-я хромосома содержит 87 Vн-сегментов, из которых не менее 32 — псевдогены. Примечательно, что дополнительные, «безродные» Vн- и D-сегменты были найдены в 15 и 16 хромосомах; некоторые из них, возможно, функциональны, но пока еще нет доказательств их вклада в разнообразие тяжелых цепей. Рекомбинационное соединение сегментов V, D и J - это основной источник гипервариабельности тяжелых цепей в третьем участке, определяющем комплементарность, — CDR-3, который представляет собой существенную часть антигенсвязываюшего центра. При иммунном ответе на некоторые антигены, например декстраны, почти все различия между молекулами антител разной специфичности касаются именно CDR-3.
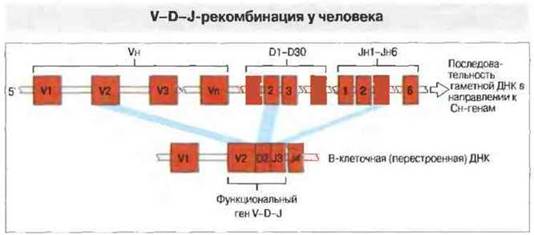
Рис. 8.10. В локусе генов тяжелых цепей путем соединения трех сегментов ДНК образуется экзон V-D-J, кодирующий Vн-домен. Из 80 Vh-генов около 50 функциональны, а остальные - псевдогены. При рекомбинации V-гена с одним из 30 D-сегментов и с одним из шести J-сегментов в В-клетке образуется функциональный ген V-D-J.
Перестройка и экспрессия генов V-областей происходит по особой программе в раннем периоде внутриутробного развития
При иммунизации животных внутриутробно или сразу после рождения способность к ответу на каждый антиген развивается четко определенным, вероятно запрограммированным, образом. Согласно этой программе, у человека первыми используются V-сегменты, ближайшие к J-ceгментам, причем интересно, что среди таких сегментов V61 представляет собой единственный участок консервативной последовательности. У всех приматов, чьи Vн-гены удалось изучить, этот генный сегмент представлен единственной копией без внутривидовых вариантов, а различия между человеком и другими приматами касаются только 2 % нуклеотидов.
Фетальный репертуар специфичностей сверхшироко представлен в аутоантителах как свидетельство того, что аутоиммунопатология отчасти может быть следствием задержанной перестройки гаметных V-генов. Подобным образом неперестроенные V-сегменты обильно представлены в незрелых В-клетках лимфом; 20 таких V-сегментов выявлены в 85 % случаев хронического лимфолейкоза.
Нуклеотидные последовательности, примыкающие к неперестроенным V-, D- и J-генам, управляют их рекомбинацией
Рекомбинация генных сегментов — это ключевой момент формирования функциональных генов вариабельных областей легких и тяжелых цепей. В настоящее время уже известен тонкий механизм этих генных перестроек и идентифицированы специфические нуклеотидные последовательности, действующие в этом процессе в качестве сигнальных (RSS, от англ. recombinationsignal sequences) (рис. 8.11).
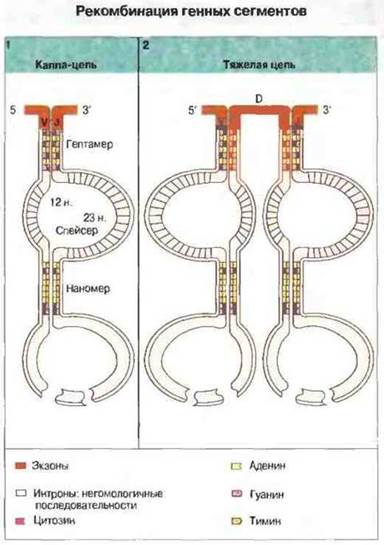
Рис. 8.11. Рекомбинация заключается в сплайсинге (соединении) сегментов V и J (например, в случае легких k-цепей) (1) или в сплайсинге V, D и J (в случае тяжелых цепей) (2). Ей способствует узнавание белками RAG-1 и RAG-2 нуклеотидной последовательности интронов на 3'-конце V- и D-сегментов и на 5'-конце J- и D-сегментов. Спейсеры из 12 и 23 нуклетидов имеют неконсервативную последовательность, но фиксированную длину, соответствующую примерно одному и двум виткам двойной спирали ДНК соответственно. Благодаря этому гептамеры и наномеры обеих спиралей идут рядом, что позволяет им одновременно взаимодействовать с белками RAG.
Сигнальная последовательность, расположенная ниже (с 3'-стороны) V- и D-сегментов, состоит из гептамера CACAGTG (или его аналога), следующего за ним спенсера неконсервативной структуры из 12 нуклеотидов и соседнего со спенсером наномера АСАААААСС или его аналога. Сигнальная последовательность, примыкающая непосредственно (с 5'-стороны) ко всем гаметным D- и J-сегментам, состоит из наномера, расположенного выше него неконсервативного спенсера из 23 нуклеотидов и — ещё выше — гептамера. Следующие за Vl-, Vн- и D-ceгментами гептамеры и наномеры комплементарны аналогичным последовательностям, предшествующим Jl-, D- и Jн-сегментам, и вступают с ними в рекомбинацию. Спейсер из 12 нуклеотидов соответствует приблизительно одному, а из 23 — двум виткам спирали ДНК.
Рекомбинационным процесс регулируют (по крайней мере отчасти) два гена, активирующих рекомбинацию (RAG-1 и RAG-2, от англ. recombination-activating genes). У мышеи, лишенных этих генов, не образуются Т-клеточные рецепторы и иммуноглобулины и поэтому отсутствуют зрелые Т- и В-клетки. На уровень экспрессии генов RAG-1 и RAG-2 влияет интерлейкин-7 (ИЛ-7) — цитокин, выделяемый стромальными клетками костного мозга. Очищенные белки RAG-1 и RAG-2, воздействуя на синтетические фрагменты ДНК, содержащие гепгамеры и наномеры вместе со спенсерами из 12 и 23 нуклеотидов, как на субстрат, способны вызывать образование синаптического комплекса из двух RSS. Сначала белок RAG-1 связывается с наномером, а неспособный прямо связаться с ДНК белок RAG-2 присоединяется к комплексу RAG-1/ДНК непосредственно рядом со спенсером из 12 нуклеотидов. После этого между спейсерами из 12 и 23 нуклеотидов возникает синапс (связывание), по-видимому, как результат взаимодействия между комплексами RAG-1-наномер—спейсер (23 н.) и RAG-2-RAG-1— наномер—спейсер (12 н.). После связывания происходит направляемое гептамерами расщепление ДНК на границах между ними и соединяющимися генными сегментами V-(D)-J.
Расщепление ДНК начинается с надреза цепи на границе между 5'-концом сигнального гептамера и функциональным геном. Затем белки RAG углубляют первоначальный надрез до полного разрыва обеих цепей с образованием «шпильки» на конце функционального гена, что in vitro вполне доступно для наблюдения. Проследить этот процесс in vivo труднее, поскольку шпильки еще до соединения генных сегментов часто подвергаются дальнейшим изменениям (рис. 8.12).
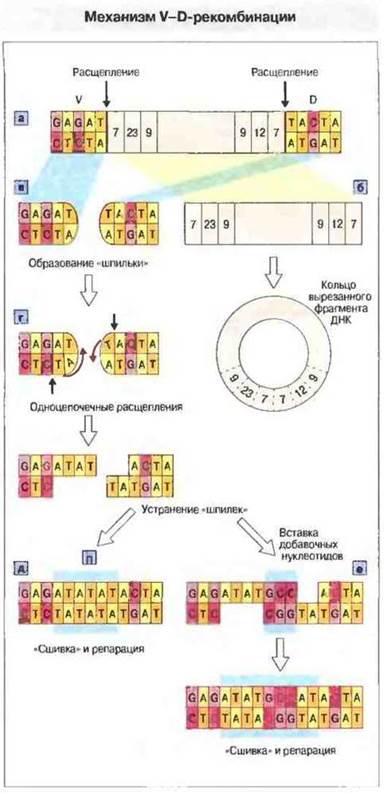
Рис. 8.12. а. После образования синаптического комплекса сигнальные последовательности рекомбинации (RSS) соединяющихся генных сегментов вырезаются вместе с промежуточным участком ДНК и затем (б), соединяясь противоположными концами, замыкаются в кольцо. в. Концы двух цепей двойной спирали каждого функционального гена соединяются ковалентно, принимая форму, напоминающую шпильку для волос. Для удаления «шпилек» эндонуклеаза надрезает одну из цепей ДНК в любой точке (г). Разрывы в нуклеотидной последовательности восполняются путем синтеза ДНК, и два конца «сшиваются» таким образом вместе (д). Расщепление одной из цепей ДНК вызывает образование палиндромных последовательностей (П), увеличивающих длину области соединения (голубой квадрат). Дополнительное разнообразие создается путем добавления нуклеотидов (N-региональная вариабельность) с помощью концевой дезоксинуклеотидил-трансферазы; в частности, это обнаружено при перестройке генов тяжелых цепей, но может происходить также при синтезе одной из подгрупп легких цепей (е).
Место сшивки генных V- и J-сегментов может незначительно варьировать
Небольшие отклонения в позициях соединения генных сегментов при рекомбинации служат еще одним источником разнообразия антител. Например, последний кодон Vк-сегмента обычно кодирует 95-й, а первый Jк-триплет - 96-й аминокислотный остаток легкой к-цепи, но иногда 96-й остаток кодируется составным триплетом, у которого второй и третий нуклеотиды (или только третий) принадлежат первому Jк-триплету, а первый (либо первый и второй) - относится к нитрону на 3'-конце Vк-сегмента (рис. 8.13), что вызывает вариации аминокислотной последовательности. Разумеется, для синтеза функционально полноценной легкой цепи необходима правильная рамка считывания; если при рекомбинации генных сегментов произойдет ее сдвиг, синтезируемые антитела могут быть неактивными.
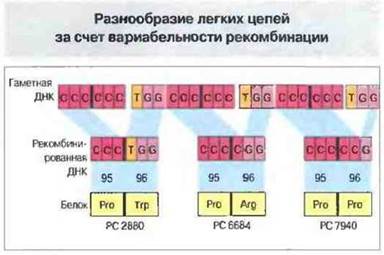
Рис. 8.13. В результате рекомбинационной вариабельности одни и те же гаметные Vk21- и J1-сегменты кодируют три разных белка - РС2880, РС6684 и РС7940. Благодаря рекомбинации, затронувшей конец кодона ССС, 95 и 96 позиции в белке PC 2880 занимают остатки пролина и триптофана соответственно. Рекомбинация одного нуклеотида, расположенного ниже кодона ССС, вызывает появление в указанных позициях белка РС6684 остатков пролина и аргинина. После рекомбинации двух нуклеотидов, расположенных ниже конца Vk21 -сегмента, в этих позициях белка PC 7940 находятся 2 остатка пролина.
Подобная погрешность соединения наблюдается и при рекомбинации генных сегментов D и J тяжелой цепи; отклонения могут достигать 10 нуклеотидов (рис. 8.14). Кроме того, возможна вставка еще нескольких нуклеотидов между сегментами D и Jн, а также между сегментами Vн и D, при участии концевой дезоксинукдеотидил-трансферазы без какой-либо матрицы (рис. 8.12). Добавлением таких «-N-нуклеотидов» создается дополнительное аминоконцевое разнообразие антител. У мышей активность концевой дезоксинуклеотидил-трансферазы с возрастом повышается, приводя к накоплению длинных N-сегментов у взрослых животных. В результате рекомбинационная вариабельность D-участка может быть настолько высокой, что изменяются все до одного генные D-сегменты.
При тяжелом комбинированном иммунодефиците (SCID, от англ. severe combined immune deficiency) из-за дефекта рекомбинаций V-(D)-J не образуются функциональные Т- или В-клетки.
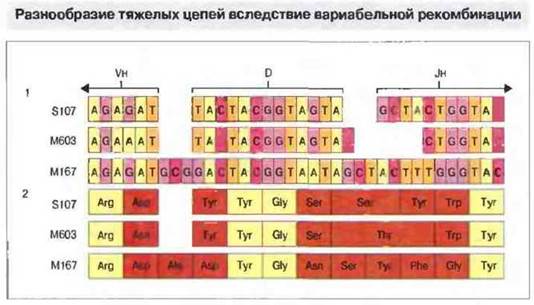
Рис. 8.14. Нуклеотидная последовательность (1) кодирующих генов сопоставлена с аминокислотной последовательностью (2) тяжелых цепей трех образцов антител к фосфорилхолину. Вариабельные рекомбинации между гаметными Vн-,D- и Jн-сегментами вызывают вариации аминокислотных последовательностей (показано коричневым цветом). В некоторых случаях (пример - белок М167), по-видимому, происходит вставка добавочных кодонов. При этом, однако, общая рамка считывания не сдвигается, так как число вставленных нуклеотидов кратно трем.