Биохимические основы жизнедеятельности организма человека - Волков Н.И., Несен Э.Н. 2000
Биохимические основы жизнедеятельности организма человека
Ферменты - биологические катализаторы
Механизм действия ферментов
Основным условием любой химической реакции является взаимодействие молекул реагирующих веществ. Произойти оно может только в том случае, если молекулы обладают достаточным количеством энергии, необходимой для преодоления существующего между ними энергетического барьера. Энергетический барьер обусловлен либо электростатическими силами отталкивания между молекулами, либо силами сцепления между атомами в молекуле (прочностью химических связей). Чем выше энергетический барьер, тем медленнее протекает реакция. В химическую реакцию вступают только "активированные" молекулы, которые имеют достаточно высокую энергию активации и способны преодолеть энергетический барьер данной реакции. Энергия активации — это энергия, которая необходима молекулам для вступления в реакцию.
В неживой природе активация молекул осуществляется путем нагревания (увеличение температуры на 10 °С увеличивает скорость реакции в 2—3 раза), повышения давления, облучения либо введением катализатора. В живом организме превращение веществ осуществляется благодаря снижению энергетического барьера реакции ферментами-катализаторами. Ферменты взаимодействуют с субстратом и снижают энергию активации, необходимую для начала реакции (рис. 35).
Согласно современным представлениям, которые сформулированы в работах В. Анри, Л. Михаэлиса, М. Ментена и других ученых, механизм взаимодействия ферментов с субстратами связан с образованием нестойких ферментсубстратных комплексов (ES). В процессе образования фермент-субстратного комплекса в субстрате происходит перераспределение энергии, что приводит к разрыву или образованию химических связей. Так, например, энергия активации сахарозы при гидролитическом расщеплении без фермента составляет 134 кДж ∙ моль-1 (25,6 ккал ∙ моль-1), а в присутствии фермента (сахаразы) — только 39,3 кДж ∙ моль-1 (8 ккал ∙ моль-1).
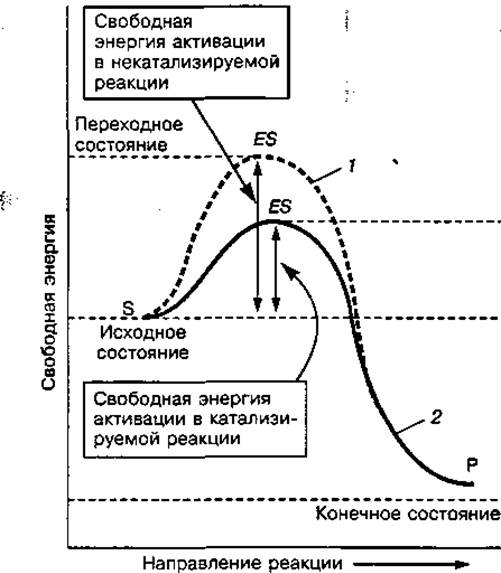
Рис. 35 Изменение энергии активации реагирующих веществ в неферментативной (1) и ферментативной (2) реакциях
Процесс взаимодействия фермента с субстратом протекает в несколько стадий, представленных на рис. 36. Основными из них являются:
✵ взаимодействие субстрата (S) с активным центром фермента (Е) и образование ферментсубстратного комплекса (ES);
✵ преобразование первичного ферментсубстратного комплекса в другие ферментсубстратные комплексы (ES* и ES**), в ходе которых вещества переходят в активное состояние и далее распадаются на фермент и продукты реакции (Р);
✵ отделение продуктов реакции от активного центра фермента и диффузия их в окружающую среду.
Схема записи ферментативного катализа имеет вид
![]()
Сам фермент в ходе реакции не изменяется и может взаимодействовать с новыми молекулами субстрата. Например, ферментативную реакцию гидролиза АТФ с участием Са2+-активируемой АТФ-азы схематически можно представить как
![]()
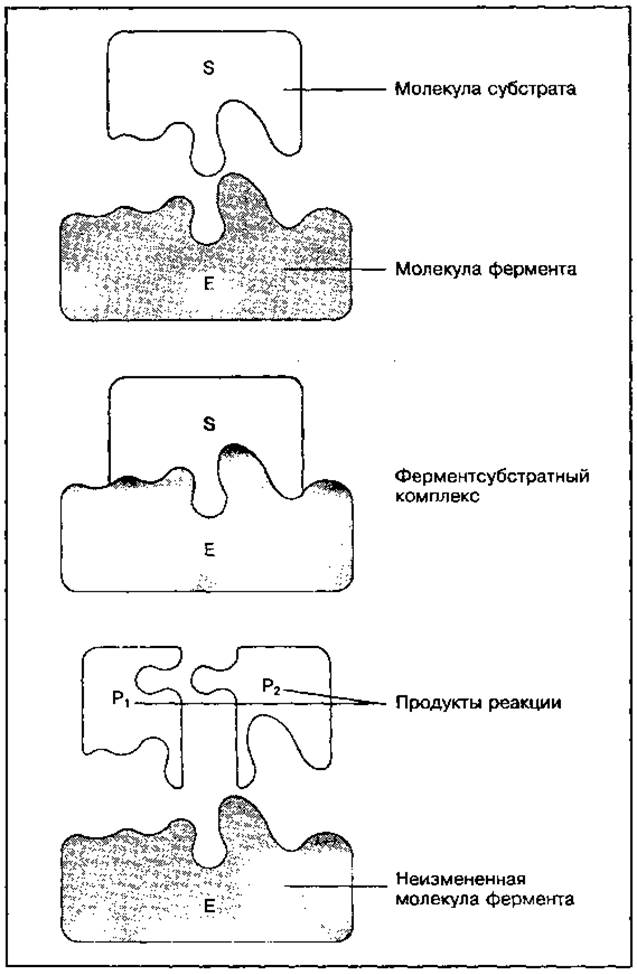
Рис. 36 Основные стадии процесса взаимодействия фермента с субстратом
Взаимодействие фермента с субстратом может произойти только при соответствии формы активного центра фермента со структурой молекулы субстрата, т. е. при их высоком сродстве. Существует несколько моделей, объясняющих механизм взаимодействия субстрата с ферментом. Так, согласно модели Э. Фишера, активный центр фермента имеет жесткую структуру и точно соответствует структуре молекулы субстрата. Молекула субстрата подходит к активному центру фермента, как «ключ к замку» (рис. 37, а). В соответствии с моделью Д. Кошланда «перчатка — рука», активный центр фермента не имеет жесткой конфигурации и создается субстратом в момент их взаимодействия аналогично перчатке, которая приобретает форму руки (рис. 37, б).
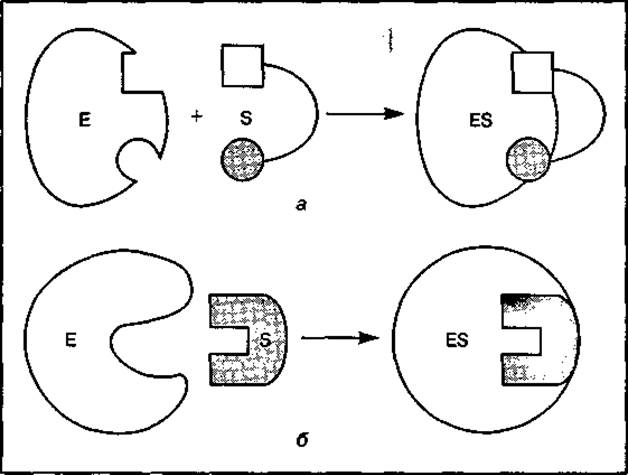
Рис. 37 Модели взаимодействия фермента с субстратом: а — модель "жесткой матрицы" по Э. Фишеру; б — модель "перчатка—рука" по Д. Кошланду