БИОХИМИЯ УЧЕБНИК ДЛЯ ВУЗОВ - Е. С. Северина - 2004
РАЗДЕЛ 5. БИОЛОГИЧЕСКИЕ МЕМБРАНЫ
IV. Участие мембран в межклеточных взаимодействиях
В плазматической мембране эукариотических клеток содержится множество специализированных рецепторов, которые, взаимодействуя с лигандами, вызывают специфические клеточные ответы. Одни рецепторы связывают сигнальные молекулы — гормоны, нейромедиаторы, другие — питательные вещества и метаболиты, третьи — участвуют в клеточной адгезии. Этот класс включает рецепторы, необходимые для узнавания клетками друг друга и для их адгезии, а также рецепторы, ответственные за связывание клеток с белками внеклеточного матрикса, такими как фибронектин или коллаген.
Способность клеток к специфическому взаимному узнаванию и адгезии важна для эмбрионального развития. У взрослого человека адгезивные взаимодействия «клетка — клетка» и «клетка —матрикс» продолжают оставаться существенными для поддержания стабильности тканей. В многочисленном семействе рецепторов клеточной адгезии наиболее изучены интегрины, селектины и кадгерины.
Интегрины — обширное суперсемейство гомологичных рецепторов клеточной поверхности для молекул межклеточного матрикса, таких как коллаген, фибронектин, ламинин и др. Являясь трансмембранными белками, они взаимодействуют как с внеклеточными молекулами, так и с внутриклеточными белками цитоскелета. Благодаря этому интегрины участвуют в передаче информации из внеклеточной среды в клетку, определяя таким образом направление её дифференцировки, форму, митотическую активность, способность к миграции. Передача информации может идти и в обратном направлении — от внутриклеточных белков через рецептор во внеклеточный матрикс.
Идентифицировано примерно 20 разных членов семейства рецепторов в разных типах клеток.
Примеры некоторых интегринов:
✵ рецепторы для белков внеклеточного матрикса. Они связываются с гликопротеиновыми компонентами внеклеточного матрикса, в частности с фибронектином, ламинином и витронектином (см. раздел 15);
✵ интегрины тромбоцитов (IIb и IIIа) участвуют в агрегации тромбоцитов, происходящей при свёртывании крови;
✵ лейкоцитарные белки адгезии. Для того чтобы мигрировать к месту инфекции и воспаления, лейкоциты должны вступить во взаимодействие с эндотелиальными клетками сосудов. Это взаимодействие может опосредовать связывание Т-лимфоцитов с фибробластами при воспалении.
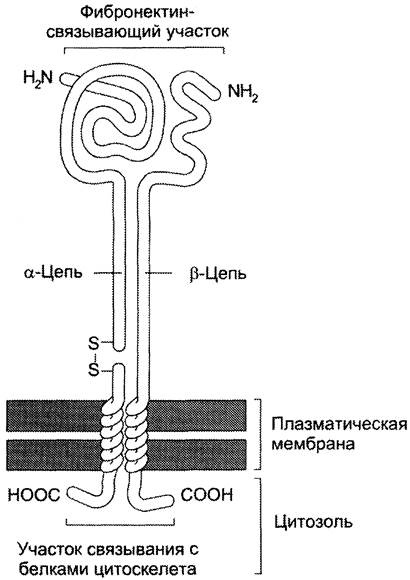
Интегрины — гетеродимеры, а каждая субъединица (α, β) содержит один трансмембранный домен (рис. 5-26).
Рис. 5-26. Рецептор фибронектина. Рецептор фибронектина принадлежит к семейству интегринов. Каждая субъединица имеет единственный трансмембранный домен, короткий цитоплазматический и протяжённый N-внеклеточный домены. Обе субъединицы (α, β) интегрина гликозилированы и удерживаются вместе нековалентными связями. α-Субъединица синтезируется в виде одной полипептидной цепи, затем расщепляемой на малую трансмембранную цепь и большую внеклеточную цепь, соединённые дисульфидными мостиками. β-Субъединица содержит 4 повтора из 40 аминокислотных остатков каждый. α-Субъединицы богаты цистеином и содержат множество внутрицепочечных дисульфидных связей (на рисунке не показаны). Связываясь с фибронектином снаружи и с цитоскелетом внутри клетки, интегрин действует как трансмембранный линкер.
Индивидуальные интегрины строго специфичны. Центр связывания интегринов образован внеклеточными доменами α- и β-субъединиц. Интегрины узнают и связываются с белками, содержащими определённую аминокислотную последовательность -Арг-Гли-Асп-, присутствующую в ряде матриксных белков (фибронектин, фибриноген, ламинин, коллаген I типа и другие). Эффект связывания усиливается в присутствии ионов Са2+ и Mg2+.
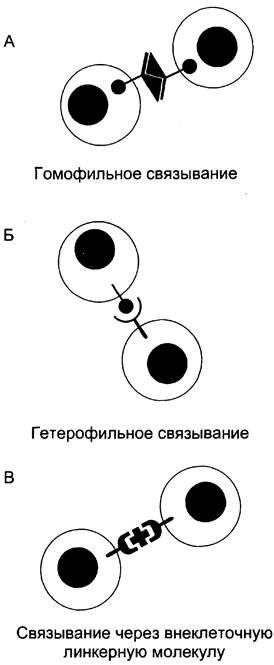
Кадгерины и селектины — семейства трансмембранных Са+-зависимых гликопротеинов, участвующих в межклеточной адгезии. Три возможных способа участия рецепторов этого типа в межклеточной адгезии представлены на рис. 5-27.
Рис. 5-27. Способы взаимодействия между молекулами клеточной поверхности в процессе межклеточной адгезии. А — рецепторы одной клетки могут связываться с такими же рецепторами соседних клеток (гомофильное связывание): Б — рецепторы одной клетки могут связываться с рецепторами другого типа соседних клеток (гетерофильное связывание): В — рецепторы клеточной поверхности соседних клеток могут связываться друг с другом с помощью поливалентных линкерных молекул.
Кадгерины разных тканей очень схожи, гомологичные аминокислотные последовательности составляют 50 — 60%. Каждый рецептор имеет один трансмембранный домен. В отсутствие Са2+ конформация кадгеринов меняется, и они становятся доступными для протеолитических ферментов, которые их расщепляют. Наиболее полно охарактеризованы 3 группы кадгериновых рецепторов:
✵ Е-кадгерин находится на поверхности многих клеток эпителиальных и эмбриональных тканей;
✵ N-кадгерин локализован на поверхности нервных клеток, клеток сердца и хрусталика;
✵ Р-кадгерин расположен на клетках плаценты и эпидермиса.
Кадгерины играют важную роль при начальной межклеточной адгезии, на стадиях морфо- и органогенеза. Они обеспечивают структурную целостность и полярность тканей, особенно эпителиального монослоя.
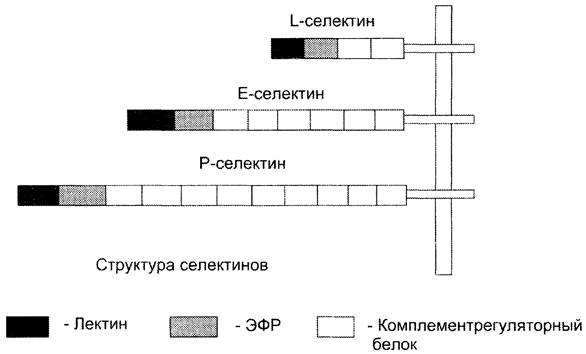
В семействе селектиновых рецепторов наиболее хорошо изучены три белка: L-селектин, Р-селектин и Е-селектин. Внеклеточная часть селектинов состоит из 3 доменов: первый домен представлен 2-9 блоками повторяющихся аминокислотных остатков (комплементрегуляторный белок), второй — домен эпидермального фактора роста (ЭФР), третий — N-концевой лектиновый домен (рис. 5-28). Селектины L, Р, Е различаются количеством блоков в комплементрегуляторном белке. Лектины — семейство белков, специфически взаимодействующих с определёнными последовательностями углеводных остатков в составе гликопротеинов, протеогликанов и гликолипидов внеклеточного матрикса.
Рис. 5-28. Структура селектинов.
Углеводные структуры — поливалентные линкерные молекулы, которые могут быть сульфатированы, фукозилированы и сиализированы, т. е. могут содержать остатки серной кислоты, фукозы и сиаловой кислоты. Связывание лигандов с рецепторами происходит в области N-концевого лектинового домена.