Основы биохимической инженерии Часть 1 - Бейли Дж., Оллис Д. 1989
Стехиометрия и энергетика метаболических превращений
Взаимосвязанность метаболических реакций; АТР и NAD
АТР и другие фосфаты
В гл. 3 и 4 мы рассматривали кинетику реакций в системах с изолированными ферментами, а также практическое применение свободных ферментов и ферментных препаратов. Большинство упоминавшихся в гл. 3 работ по изучению кинетики ферментативного катализа и большая часть приведенных в гл. 4 примеров практического применения ферментов относятся к гидролазам, которые по определению расщепляют или разлагают большие молекулы на более мелкие с участием воды в качестве второго субстрата. Такие процессы деградации сопровождаются снижением свободной энергии системы и поэтому в закрытой системе происходят спонтанно. В настоящем разделе мы рассмотрим механизмы, которые позволяют открытой системе, а именно живой клетке, сочетать реакции, протекающие с выделением энергии (экзэргонические), с реакциями и другими функциями, осуществляющимися только с затратой определенного количества энергии (эндэргонические процессы).
Ранее мы уже упоминали о строении и некоторых свойствах аденозинтрифосфата (АТР; см. разд. 2.3.1 и рис. 2.8), где, в частности, отмечали, что ферментативный гидролиз АТР до ADP и неорганического фосфата сопровождается большим отрицательным изменением свободной энергии:
АТР + Н2O → ADP + Pi ∆G°' = -7,3 ккал/моль (5.11)
Здесь Pi — неорганический фосфат. Таким образом, в ходе гидролиза АТР выделяется большое количество энергии, а в обратной реакции присоединения фосфата к ADP энергия может запасаться и храниться в виде АТР для последующего использования. Давайте рассмотрим, как реализуется последний процесс в условиях сопряженных химических реакций.
Понятие об общем промежуточном соединении можно проиллюстрировать на примере другой последовательности реакций, являющейся частью пути метаболизма Эмбдена — Мейергофа — Парнаса. Превращение альдегида в карбоновую кислоту (в водном растворе) сопровождается понижением свободной энергии примерно на 7000 кал/моль. Как показано на рис. 5.3, в изолированной системе эта свободная химическая энергия полностью рассеялась бы в растворе. В живой клетке, однако, этого не происходит. При биохимическом окислении глюкозы превращение глицеральдегид-3-фосфата в соответствующую карбоновую кислоту (3-фосфоглицерат) сопровождается регенерацией АТР из ADP (см. реакцию 2 на рис. 5.3). Таким образом, обусловленное окислением альдегида уменьшение свободной энергии благодаря участию ферментативной системы клетки сочетается с одновременной регенерацией АТР.
1) Окисление альдегида до карбоновой кислоты в изолированной системе (в водном растворе)
RCHO + H2O → 2H + RCOO- + H+ ∆G1⁰' ≈ -7 ккал/моль
2) Те же реакции, сопряженные с регенерацией АТР (окисление глюкозы)
RCHO + HPC42- + ADP3- → 2H + RCOO- + ATP4- ∆G2⁰' ≈ 0 ккал/моль
3) Вычитая из реакции 2 реакцию 1, получим
АDР3- + НРС42- + Н+ → АТР4- + Н2O ∆G⁰' ≈ +7 ккал/моль
4) Элементарные стадии реакции 2:
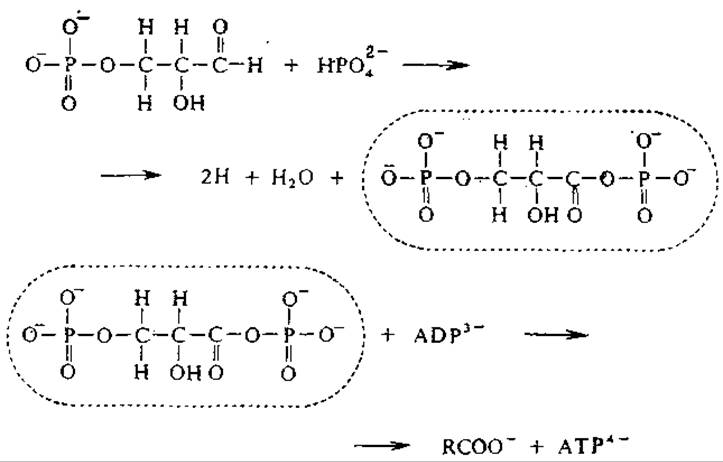
РИС. 5.3. Примеры реакций с общим промежуточным соединением.
Поскольку в результате реакции 2 свободная энергия практически не изменяется, то высвобождающаяся при окислении глицеральдегид-3-фосфата свободная энергия, очевидно, трансформируется в так называемую высокоэнергетическую (макроэргическую) фосфатную связь аденозинтрифосфата.
Последовательность элементарных реакций, в действительности происходящих в клетке, изображена в нижней части рис. 5.3. К наиболее существенным характеристикам этих двух последних реакций относятся, во-первых, наличие общего промежуточного соединения, являющегося продуктом первой реакции и реагентом во второй, и, во-вторых, большая свободная энергия реакции гидролиза (отщепления фосфатной группы) промежуточного фосфорилированного соединения по сравнению с гидролизом АТР. Равновесие последней стадии смещено вправо, т. е. в сторону образования продукта реакции; таким образом, этот этап метаболизма глюкозы одновременно представляет собой и один из нескольких центров регенерации АТР, необходимого для эндергопических реакций. Регенерация АТР осуществляется путем превращения частично метаболизированного питательного вещества в высокоэнергетическое фосфорилированное промежуточное соединение, которое затем в результате катализируемой ферментом реакции передает фосфатную группу ADP.
Фосфорилирование различных соединений, в том числе и ADP, используется клеткой для нескольких целей. Во-первых, фосфорилированные соединения представляют собой удобное хранилище значительной части свободной энергии, выделяющейся в процессе окисления клеточного топлива. Свободная энергия гидролиза некоторых соединений, называемых фосфатными донорами, превышает ∆G⁰' гидролиза АТР (например, величины ∆G⁰' для гидролиза фосфоенолпирувата и 1,3-дифосфоглицерата равны —14,8 и —11,8 ккал/моль соответственно). Следовательно, гидролиз этих соединений может использоваться для фосфорилирования ADP. Аналогично гидролиз АТР может быть связан с фосфорилированием некоторых соединений, в результате которого образуются «низкоэнергетические» фосфаты; величины ∆G⁰' расщепления последних ниже соответствующей величины для реакции гидролиза АТР (например, ∆G⁰' гидролиза глюкозо-6-фосфата и глицеро-1-фосфата составляют —3,3 и —2,20 ккал/моль соответственно).
Вторая важная функция фосфорилирования в жизни клеток связана с неспособностью сильноионизированных органических веществ проникать через клеточные мембраны. Благодаря этому обстоятельству заряженные фосфорилированные соединения, являющиеся промежуточными соединениями во многих путях метаболизма, остаются внутри клетки, что в свою очередь позволяет получить максимум энергии и химического сырья из питательных веществ. Обычно дефосфорилирование является последней стадией метаболического пути; неионизированные отходы жизнедеятельности клетки могут выводиться в среду.