Основы биохимии - Филиппович Ю. Б. 1999
Коферменты, витамины и некоторые другие биоактивные соединения
Витамины
Общее понятие о витаминах и их классификация. Витамины представляют сборную в химическом отношении группу органических соединений, поэтому с точки зрения химического строения им нельзя дать общего определения. Физические свойства веществ, относящихся к витаминам, столь же разнообразны, как и их химическая природа. Физиологическое действие витаминов на животных, растительные ткани и микроорганизмы тоже весьма различно, и отдельные витамины в этом отношении совершенно не похожи друг на друга.
Витамины объединены в отдельную группу природных органических соединений по признаку абсолютной необходимости их для гетеротрофного организма в качестве дополнительной к белкам, жирам, углеводам и минеральным веществам составной части пищи.
В большинстве случаев витамины не синтезируются гетеротрофными организмами и их недостаток сопровождается возникновением патологических явлений.
В количественном отношении потребность в витаминах ничтожна: так, человек в среднем должен потреблять ежедневно около 600 г (в пересчете на сухое вещество) основных питательных веществ и только 0,1—0,2 г дополнительных факторов питания — витаминов.
Отсюда ясно, что витамины в организме выполняют каталитические функции. Во многих случаях, как будет показано ниже, витамины являются составными частями ферментов и необходимы для их функционирования.
В последнее время изучается роль витаминов для автотрофных организмов, в частности растений, где витамины синтезируются. Оказалось, что для жизнедеятельности растений они тоже абсолютно необходимы и выполняют здесь также главным образом каталитические функции. Следовательно, на первый план в характеристике витаминов как особой группы соединений выступает их способность в ничтожных концентрациях обеспечивать осуществление ферментативных процессов.
Таким образом, витамины могут быть охарактеризованы как группа органических веществ, обладающих разнообразным строением и физико-химическими свойствами, абсолютно необходимых для нормальной жизнедеятельности любого организма и выполняющих в нем непосредственно или в составе более сложных соединений каталитические и регулярные функции.
Витамины были открыты в 1880 г. нашим соотечественником Н. И. Луниным. Они привлекли внимание именно как дополнительные факторы питания животных. В своей диссертации «О значении неорганических солей для питания животных», защищенной 18 сентября 1880 г. в Дерптском (ныне Тартуском) университете, Н. И. Лунин пришел к выводу, что кроме белков, жиров, сахаров, солей и воды животные (мыши) нуждаются также в других, неизвестных еще веществах. По его мнению, обнаружить эти вещества и изучить их значение в питании было бы исследованием, представляющим большой интерес. В дальнейшем работы Н. И. Лунина были подтверждены и развиты другими учеными. В 1912 г. польский исследователь К. Функ предложил называть эти неизвестные вещества витаминами, т. е. аминами жизни (от лат. Vita — жизнь), так как одно из них, выделенное и изученное им, содержало аминогруппу. Термин этот стал затем применяться ко всем обязательным дополнительным пищевым факторам. И хотя многие из них не содержат аминогрупп и вообще азота, название «витамины» до сих пор прочно удерживается в биологии и медицине.
Благодаря усилиям многих биохимиков и физиологов за более чем столетнюю историю витаминологии выделено около трех десятков витаминов, изучены их состав и строение, физиологическое действие и в подавляющем большинстве случаев осуществлен химический синтез соответствующих препаратов. Среди исследований советского периода выделяются работы В. Н. Букина, А. В. Палладина, Л. А. Черкес, М. Н. Шатерникова, А. В. Труфанова, В. В. Ефремова, К. М. Леутского, Б. А. Кудряшова, М. И. Смирнова, Ю. М. Островского, Р. В. Чаговца и др.
При изучении витаминов сначала каждому из них давали название по имени того заболевания, которое развивалось при отсутствии витамина в пище. При этом к названию соответствующей болезни добавлялась приставка анти, так как введение витамина в диету приводило к быстрому излечению (табл. 12). Заболевания же, развивающиеся при полном отсутствии витаминов в пище, стали обозначать как авитаминозы, при недостаточном их поступлении — как гиповитаминозы, при избыточном — как гипервитаминозы. Позже, по предложению Мак-Коллума (1913), отдельные витамины по мере их выделения условились обозначать буквами латинского алфавита: А, В, С и т. д. Наконец, после того как была исследована химическая природа ряда витаминов, стали вводить химические их названия. В настоящее время используют все три вида номенклатуры витаминов. Наметилась тенденция перехода к химическим наименованиям, которые биохимическая секция Международного союза по чистой и прикладной химии с 1956 г. признала международными. Важнейшие витамины и их названия перечислены в табл. 12; некоторые из них (Q, F, В15, U) иногда относят к витаминоподобным веществам.
Таблица 12 Важнейшие витамины их номенклатура
|
Номенклатура |
Суточная потребность человека, мг |
||
буквенная |
химическая (официальная международная) |
физиологическая (по отношению к человеку) |
|
|
Жирорастворимые |
|||
А |
Ретинол |
Антиксерофгальмический |
2,5 |
D |
Кальциферол |
Антирахитический |
0,0025 |
Е |
Токотриенол |
Антистерильный (токоферол) |
15,0 |
К |
Филлохинон |
Антигеморрагический |
0,25 |
Q |
Убихинон |
— |
— |
F |
Комплекс ненасыщенных жирных кислот (линолевая, линоленовая и арахидоновая кислоты) |
1000 |
|
Водорастворимые |
|||
B1 |
Тиамин |
Антиневритный |
2,0 |
В2 |
Рибофлавин |
Витамин роста |
2,0 |
В3 |
Пантотеновая кислота |
Антидерматитный фактор |
12 |
PP(B5) |
Никотиновая кислота и никотинамид |
Антипеллагрический |
25 |
В6 |
Пиридоксин |
Антидерматитный |
2,0 |
B12 |
Цианкобаламин |
Антианемический |
0,003 |
B15 |
Глюконодиметиламиноацетат |
Антианоксический |
2,0 |
Bс |
Птероилглутаминовая кислота |
Антианемический |
0,2 |
ВТ |
Кврнитин |
— |
— |
С |
Аскорбиновая кислота |
Антискорбутный |
75 |
Н |
Биотин |
Антисеборрейный |
0,15 |
Р |
Рутин, биофлавоноид |
Капилляроукрепляющий витамин |
50 |
U |
S-метилметионин |
Противоязвенный |
— |
Особенно велико значение витаминов для развивающегося детского организма, о чем дает представление табл. 13.
Таблица 13 Суточная потребность (мг) в некоторых витаминах для детей и подростков (по М. И. Смирнову, 1974)
Возраст, лет |
В1 |
В2 |
В6 |
С |
РР |
7—10 |
1,4 |
1,9 |
1,7 |
60 |
15 |
11—13 14—17 |
1,7 |
2,3 |
2,0 |
72 |
19 |
юноши |
1,9 |
2,5 |
2,2 |
79 |
21 |
девушки |
1,7 |
2,2 |
1,9 |
69 |
18 |
По растворимости в воде и жировых растворителях витамины делят на две группы: водо- и жирорастворимые.
Жирорастворимым и некоторым водорастворимым витаминам свойственна витамерия. Явление это состоит в том, что физиологическим действием, характерным для того или иного витамина, обладает не одно, а несколько сходных по химическому строению соединений, называемых витамерами.
По физиологическому действию на организм человека витамины принято делить на следующие группы (табл. 14).
Аналогичное влияние оказывают витамины на процессы жизнедеятельности у животных. Отсутствие или недостаток витаминов в корме приводит к нарушению нормального развития, замедлению роста, снижению продуктивности и другим нежелательным последствиям. Особенно дефицитны в подавляющем большинстве кормов витамины D, А и В12. Введение их в рацион питания животных позволяет резко повысить продуктивность животноводства.
Таблица 14 Групповая характеристика некоторых витаминов (по П. И. Шилову п Т. Н. Яковлеву, 1974)
Группа витаминов (по лечебно-профилактическому эффекту) |
Краткая клинико-физиологическая характеристика |
Название основных витаминов |
Повышающие общую реактивность организма |
Регулируют функциональное состояние центральной нервной системы, обмен веществ и трофику тканей |
В1, В2, РР, А, С |
Антигеморрагические1 |
Обеспечивают нормальную проницаемость и устойчивость кровеносных сосудов, повышают свертываемость крови |
С, Р, К |
Антианемические |
Нормализуют и стимулируют кроветворение |
В12, Вс, С |
Антиинфекционные |
Повышают устойчивость организма к инфекции: стимулируют выработку антител, усиливают защитные свойства эпителия |
С, А |
Регулирующие зрение |
Усиливают остроту зрения, расширяют поле цветного зрения |
А, В2, С |
1 Геморрагия (от греч. гайма — кровь в рагг — прорыв) — кровотечение, кровоизлияние, выход крови из сосудов.
Витамин А (ретинол). Изучение этого витамина начато в 1909 г., а синтез осуществлен в 1933 г. Витамин А имеет несколько витамеров, из которых наиболее распространенным считают витамин A1 (его много в печени морских рыб):
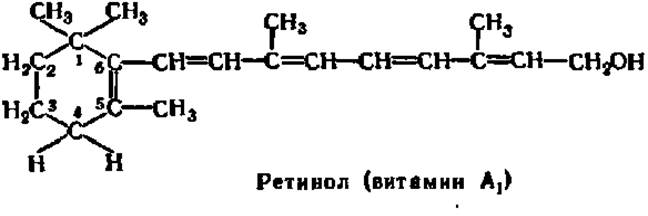
Витамин А2 отличается от А1 добавочной двойной связью между 3-м и 4-м углеродными атомами шестичленного цикла (содержится в печени пресноводных рыб). Обе формы (A1 и А2) существуют в виде ряда геометрических изомеров, но лишь некоторые из них физиологически активны. Таким образом, витамин А состоит из смеси циклических ненасыщенных спиртов характерного химического строения с большим числом сопряженных двойных связей.
Это кристаллические тела лимонно-желтого цвета с температурой плавления от 59 до 64° С (в зависимости от вида геометрического изомера), хорошо растворимые в жирах и жирорастворителях: бензине, серном эфире, хлороформе, ацетоне и др.
Витамины группы А легко окисляются как в лабораторных условиях (посредством МnO2), так и в организме. Окисляясь в организме при участии биокатализатора, ретинол (спирт) превращается в ретиналь (альдегид), тоже обладающий активностью витамина А:
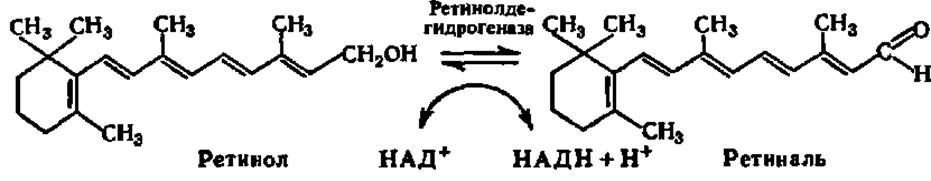
Однако при отсутствии О2 ретинол устойчив даже при 100° С. В тканях животных организмов, например в печени, витамин А часто находится в форме сложных эфиров с пальмитиновой кислотой. В таком виде он более устойчив и, следовательно, может запасаться впрок, высвобождаясь по мере надобности. К другим тканям и органам ретинол транспортируется, соединяясь с ретинолсвязывающим белком крови, впервые выделенным в 1968 г. (М = 21000, составлен из 181 аминокислотного остатка, первичная структура выяснена в 1974 г.).
При отсутствии в пище витамина А в организме животного и человека развивается ряд специфических патологических изменений (А-авитаминоз): ослабление зрения (сумеречная, или «куриная», слепота), поражение эпителиальных тканей (сухость, слущивание эпителия), в том числе роговицы глаза (сухость ее и воспаление называются ксерофтальмией, отсюда и название витамина А — антиксерофтальмический). Кроме того, при А-авитаминозе наблюдается торможение роста, падение в массе и общее истощение организма.
Сухость кожи и слизистых оболочек, способствующая проникновению в организм болезнетворных микробов, ведет к возникновению дерматитов, бронхитов и катаров дыхательных путей. Витамин А, предохраняющий от этих инфекционных заболеваний, относят поэтому к группе антиинфекционных витаминов.
У растений только при достаточном содержании предшественников витамина А (каротиноиды) происходят нормальное прорастание пыльцы и оплодотворение.
Механизм участия витамина А в поддержании нормального состояния эпителиальных тканей неизвестен. Роль его в поддержании остроты зрения выяснена: окисленная форма витамина А (ретиналь) в виде цис-изомера является простетической группой белка — опсина, образуя родопсин — основное светочувствительное вещество сетчатки (ретины) глаза (отсюда и название ретинол). Родопсин открыт более столетия тому назад (1876) Ф. Боллом.
Опсин имеет М = 38850, содержит два олигосахаридных фрагмента, соединенных с полипептидной цепью из 348 аминокислотных остатков, чередование которых выяснено. Он вмонтирован в мембрану диска наружного сегмента фоторецепторной клетки типа палочки, пронизывая мембрану компактно расположенными семью а-спиралями, к одной из которых присоединен иминной связью, возникающей при взаимодействии альдегидной группы с ε-NН2- группой лиз296, 11-цис-ретиналь (рис. 60). Под действием кванта света происходит превращение цис-ретиналя в транс-форму (чувствительность этой реакции — единичный фотон):
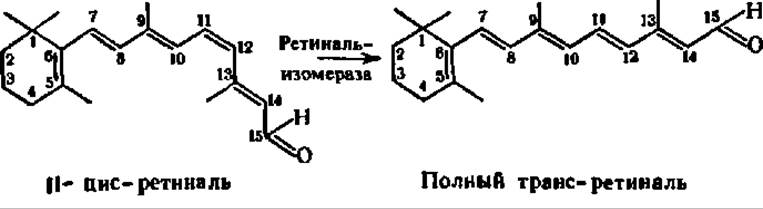
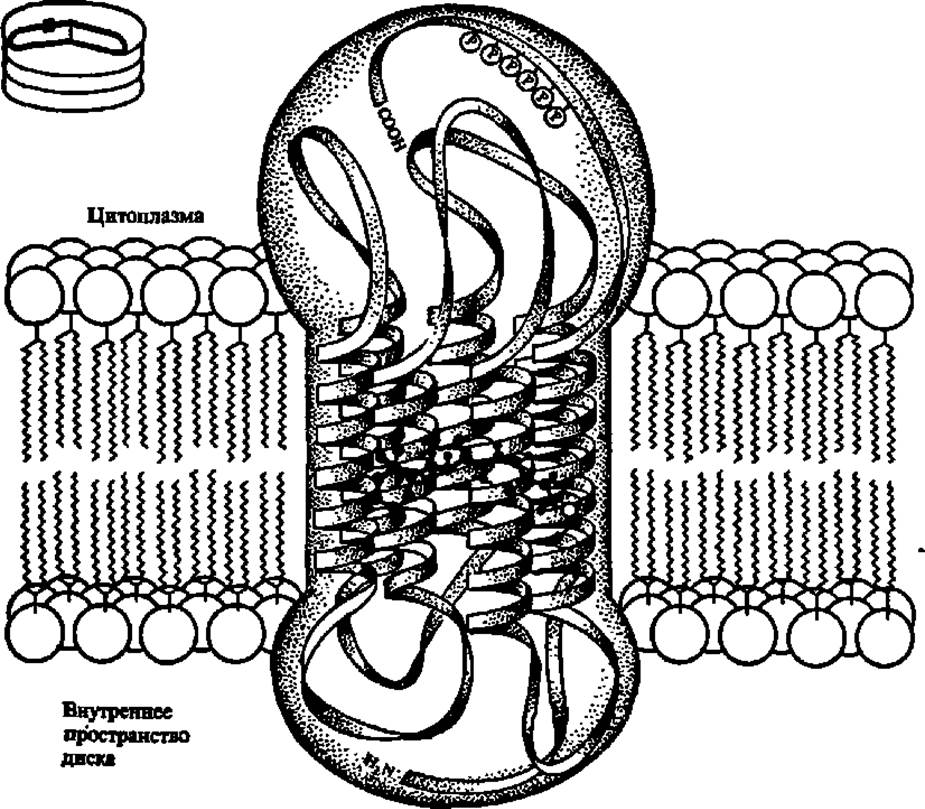
Рис. 60. Структура фоторецепторного белка — родопсина и его расположение в мембране диска фоторецепторной клетки (пояснение в тексте):
в левом верхнем углу рисунка — фрагмент наружного сегмента фоторецепторной клетки, состоящего примерно из двух тысяч дисков; квадратом обозначено местоположение родопсина в мембране
Это, в свою очередь, возбуждает активность родопсина, вследствие чего несколько сотен молекул трансдуцина (~ 500) — белка (М = 85 000), относящегося к G-семейству (см. с. 457) и являющегося вторым членом биохимического каскада усиления светового сигнала (это происходит в течение 1 мс), распадается на а-субъединицу (М = 39000), у которой одновременно гуанозиндифосфат заменяется на гуанозинтрифосфат (см. с. 458), и димер из ß- и у-субъединиц (М = 35000 и 8000 соответственно). Комплекс а-субъединицы трансдуцина с гуанозинтрифосфатом взаимодействует с третьим членом каскада усиления — фосфодиэстеразой циклического гуанозинмонофосфата (состоит из четырех субъединиц: а — 88 кДа, ß — 84 кДа и двух у, по 11 кДа каждая), которая в присутствии белка, ее активирующего (он является интегральным белком ретинальной мембраны), превращает в течение секунды несколько сотен молекул цГМФ в линейные. Гидролиз циклического гуанозинмонофосфата сопровождается закрытием натриевых каналов плазматической мембраны фоторецепторной клетки, ее гиперполяризацией и возникновением электрического импульса, поступающего в синапс внутреннего сегмента и передаваемого в центральную нервную систему. Проходящий одновременно процесс фосфорилирования С-концевой части молекулы родопсина (см. рис. 60) снимает его дальнейшее воздействие на распад трансдуцина, т. е. фоторецепторный цикл завершается.
Квантово-химические расчеты строения ретиналя позволяют более глубоко понять его возможную роль в зрительном акте. Система из сопряженных двойных связей в молекуле ретиналя создает условия для возникновения геометрических изомеров в первую очередь (как это следует из значений порядка связей — см. с. 191) по двойным связям между 9—10-м и 11—12-м атомами углерода (они здесь минимальны по сравнению с таковыми при 7—8-м и 13—14-м атомами):
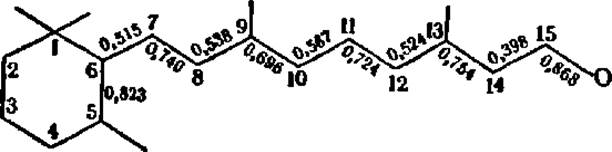
Если при взаимодействии цис-ретиналя (в составе родопсина) с квантами света происходит возбуждение электронов, что можно рассматривать как начальную фазу возникновения электрического импульса, то, видимо, цис-транс-переход может служить своеобразным блокирующим механизмом, обеспечивающим односторонний ход процесса утилизации световой энергии.
Источниками витамина А для человека являются рыбий жир, печень рыб и домашних животных, желток яйца, сливочное масло, зеленые части растений и красномякотные овощи (морковь, перец, томаты и др.). В двух последних витамин А содержится в виде провитамина, которым является ß-каротин. Молекула ß-каротина распадается в кишечной стенке человека и животных с образованием двух молекул витамина А1(см. с. 418).
Применение витамина А в животноводстве приносит ощутимый эффект. Когда жарким летом пастбища выгорают и содержание витамина А, точнее. провитамина А — каротина в травах резко падает, у каракульских овец возникает А-авитаминоз, снижающий их плодовитость. Подкормка витамином А обеспечивает возрастание приплода на 5—7 ягнят на каждые 100 овцематок, т. е. примерно на 3 млн. ягнят в южных районах нашей страны. Кроме того, добавление витамина А или каротина в корм молодняку (цыплята, телята, поросята) обеспечивает их лучшую выживаемость и более быстрый рост, а включение его в рационы при откорме крупного рогатого скота повышает прирост живой массы на 12—15%.
Витамин D (кальциферол). Изучение этого витамина начато в 1916 г.; в 1931 г. он был получен синтетическим путем.
Как и витамин А, витамин D существует в виде нескольких витамеров. Наиболее распространены витамины D2 и D3; их можно рассматривать как производные стеролов (см. гл. IX):
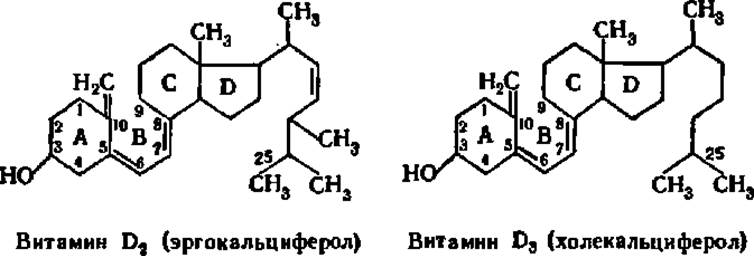
Провитаминами D2 и D3 являются соответственно эргостерол и холестерол, которые переходят в активную форму в результате размыкания связи между 9-м и 10-м углеродными атомами кольца В под действием солнечной радиации (холестерол предварительно дегидрируется и переходит в 7-дегидрохолестерол, являющийся непосредственно провитамином). Следовательно, при наличии соответствующих провитаминов (например, 7-дегидрохолестерол у человека) витамин D3может синтезироваться в организме, и его поступление с пищей не обязательно.
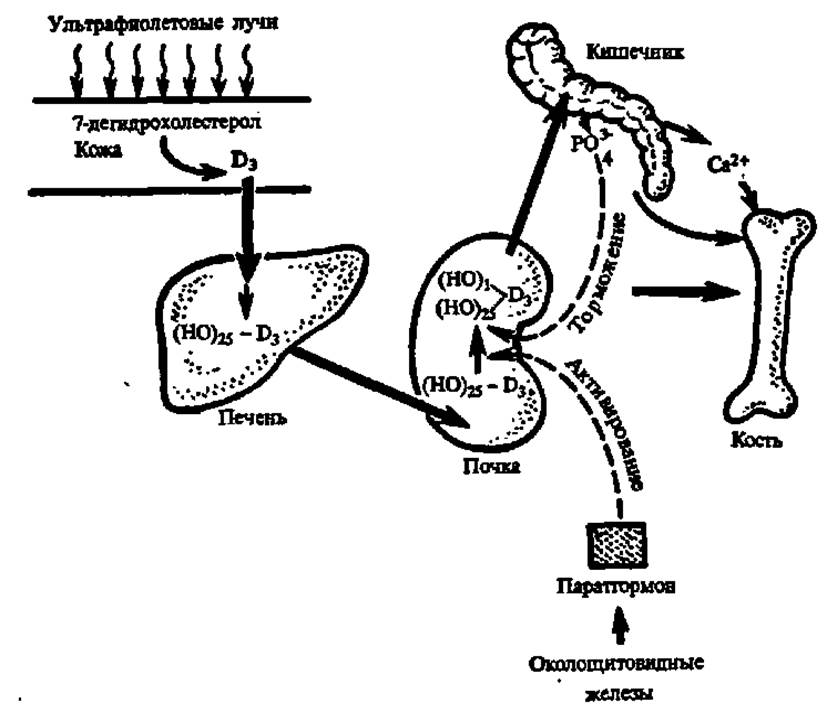
Рис. 61. Превращения витамина D3, их регуляция и воздействие диоксипроизводных на фосфорно-кальциевый обмен
Витамины D2и D3 — бесцветные кристаллы, плавящиеся при температуре 115—116° С, не растворимые в воде, но хорошо растворяющиеся в жирах и растворителях жиров (хлороформ, бензол, серный и уксусно-этиловый эфир, ацетон, спирт). Оба они малостабильны и быстро разрушаются под действием окислителей (распад идет по двойной связи между 7-м и 8-м углеродными атомами кольца В) и минеральных кислот.
При отсутствии в рационе витамина D у детей развивается широко известное заболевание — рахит. Причина его состоит в расстройстве фосфорно-кальциевого обмена и нарушении нормального отложения фосфата кальция в костной ткани. Предполагают, что при D-авитаминозе нарушается всасывание Са и Р в желудочно-кишечном тракте и образование фосфорных эфиров ряда органических соединений; вероятно, оба эти процесса взаимосвязаны. В последнее время показано, что всасывание, перенос Са и кальцификация костей регулируются не непосредственно витамином D3, а его гормонально-активным метаболитом, содержащим оксигруппы в 1-м и 25-м положениях. Именно он, связываясь с ядерными рецепторами, обеспечивает биосинтез информационной РНК для наработки Са-связывающих белков и гормонов (кальцитонин и паратгормон), регулирующих обмен кальция (рис. 61).
Источником витамина D для человека являются рыбий жир, сливочное масло, желток яйца, печень животных, молоко.
Особенно важен витамин D для кур-несушек и дойных коров. Подсчитано, что в скорлупу куриного яйца переходит 1/10 часть всего Са, содержащегося в теле курицы, а с каждым литром молока из организма коровы выносится более 1 г Са. Даже малейшее нарушение всасывания Са в кишечнике животных при D-авитаминозе пагубно сказывается на их состоянии и продуктивности. Поэтому витамин D находит широкое применение в животноводстве для повышения продуктивности птицы и крупного рогатого скота, обеспечивая рост привесов на 12—15%.
Витамин Е (токоферол). Первые сведения о существовании витамина, регулирующего процесс размножения, появились в 1922 г. Однако только в 1936 г. из масла пшеничных зародышей и хлопкового масла были выделены три производных бензопирана, которые оказались витамерами витамина Е: a-, ß- и у-токоферолами (от греч. токос — потомство, феро — несу). В 1938 г. а-токоферол был синтезирован:
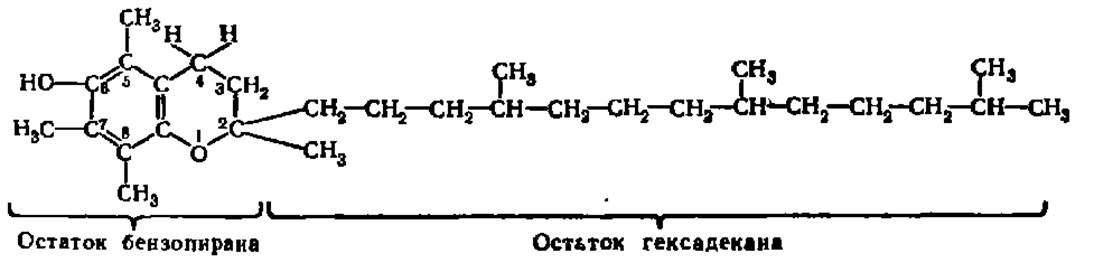
ß-Токоферол отличается от a-токоферола тем, что лишен метильной группы в положении 7, а у-токоферол — в положении 5. В последующее время были выделены еще четыре токоферола, отличающиеся числом и расположением метальных групп в бензольном ядре.
Токоферолы — бесцветные маслянистые жидкости, хорошо растворимые в растительных маслах, спирте, серном и петролейном эфире. Химически они весьма устойчивы; выдерживают нагревание до 100° С с концентрированной НС1 и 170° С на воздухе; разрушаются под воздействием ультрафиолетового излучения; оптически активны.
Витамин Е может окисляться до а-токоферилхинона, структура которого очень близка к структуре витаминов К и Q (см. ниже):
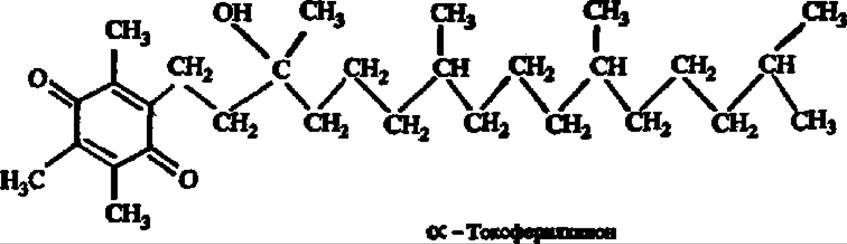
Близость химического строения витаминов Е, К и Q обусловливает сходство механизмов их действия в организме.
Долгое время считали, что значение витамина Е исчерпывается лишь его влиянием на процесс размножения, так как при отсутствии или недостатке витамина Е у человека и животных нарушается эмбриогенез (развитие плода в организме матери) и наблюдаются дегенеративные изменения репродуктивных органов. У растений витамины Е способствуют прорастанию пыльцы. Однако более глубокое изучение Е-авитаминоза показало ошибочность такого представления. Е-авитаминоз выражается в нарушении нормального функционирования и структуры многих тканей: развиваются мышечная дистрофия, дегенерация спинного мозга и паралич конечностей, жировое перерождение и т. п., т. е. общее заболевание организма.
Механизм действия витамина Е в организме двоякий. С одной стороны, витамин Е — важнейший внутриклеточный агент, предохраняющий от окисления жиры и другие легко окисляемые соединения, это один. из самых сильных природных антиоксидантов, прежде всего липидов. Реагируя с пероксидными радикалами липидов и сами при этом окисляясь, токоферолы обрывают цепи окисления. С другой стороны, витамин Е функционирует как структурный компонент биологических мембран, образуя своим углеводородным радикалом молекулярные комплексы с ненасыщенными высшими жирными кислотами фосфолипидов и стабилизируя (защищая от окисления) мембраны. Так как это обеспечивает нормальное протекание биохимических процессов, то понятны те множественные нарушения функций, которые наблюдаются при Е-авитаминозе. Недавно высказана еще одна точка зрения на механизм действия витамина Е — возможное участие в регуляции биосинтеза некоторых ферментов на уровне транскрипции в генетическом аппарате клетки их матричных РНК. Кроме того, есть данные о том, что витамин Е контролирует обмен и функции убихинона и имеет, таким образом, отношение к сопряжению окисления с фосфорилированием АДФ, т. е. к биоэнергетике организма.
Источником витамина Е для человека являются растительные масла (подсолнечное, кукурузное, хлопковое, соевое, конопляное и др.), салат, капуста и зерновые продукты. Потребность в этом витамине ничтожна, так что Е-авитаминозы и гиповитаминозы — явление очень редкое, тем более, что витамин Е откладывается во многих тканях (главным образом в жировой). Запасы его обеспечивают восполнение убыли даже при полном отсутствии витамина в пище в течение нескольких месяцев.
Витамин К (филлохинон). Первые наблюдения, указывающие на существование особого витамина, регулирующего процесс свертывания крови, были сделаны в 1929 г. Дальнейшие работы привели к открытию двух природных витаминов K1и К2, которые оказались производными нафтохинона. Витамин K1был синтетически получен в 1939 г.:
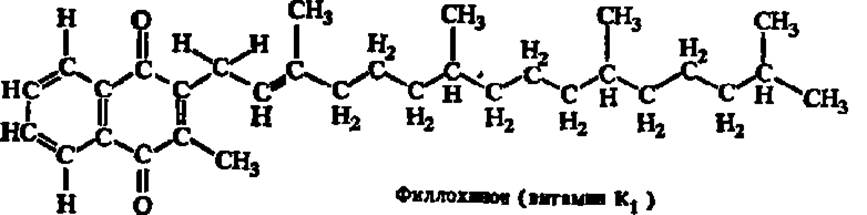
Витамин К2 отличается строением боковой цепи, содержащей от 30 до 45 углеродных атомов и несущей соответственно от 6 до 9 двойных связей. Он специфичен для бактерий и также получен синтетически (К2(35)). Его общая формула такова (и принимает значения от 5 до 8):
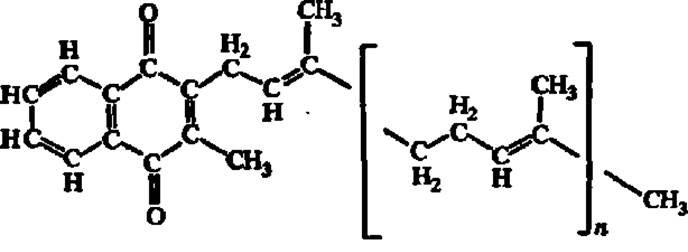
Кроме витаминов К1 и К2, многие производные нафтохинона обладают аналогичным физиологическим действием. Из них широкое практическое применение нашел синтезированный в 1942 г. А. В. Палладиным препарат «викасол» (бисульфитное соединение метилнафтохинона, растворимое в воде). Он является производным витамина К3 (метилбензохинон):
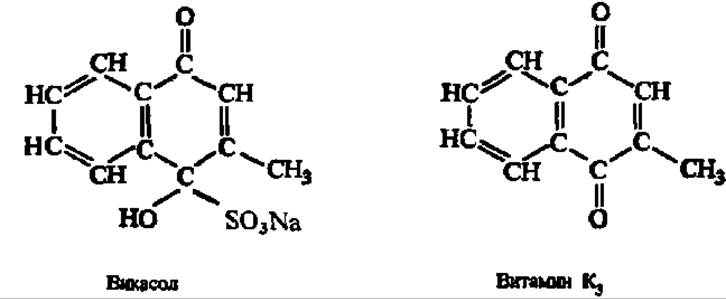
Витамин Kt —желтоватая маслянистая жидкость с температурой кипения 115—145° С, не растворимая в воде. Очень неустойчив при нагревании в щелочной среде и при облучении. Витамин К2(35) — желтые кристаллы с температурой плавления 54° С, еще более неустойчив, чем витамин K1. Витамин К3 — желтый кристаллический порошок с температурой плавления 106° С, не растворим в воде, но растворим в спирте и эфире. Викасол — бесцветный, мелкокристаллический порошок.
Витамин К способствует синтезу компонентов, участвующих в свертывании крови, и положительно влияет на состояние эндотелиальной оболочки кровеносных сосудов. При недостатке его в пище могут возникать самопроизвольные кровотечения (носовые кровотечения, кровавая рвота, внутренние кровоизлияния и т. п.). Полагают, что витамин К принимает участие в синтезе протромбина и ряда других белковых факторов, необходимых для свертывания. Протромбин переходит в тромбин, а последний вызывает превращение фибриногена в фибрин, т. е. непосредственно обеспечивает коагуляцию крови. Витамин К1, следовательно, стоит у самых истоков этой сложной системы.
Основное назначение витамина К у растений и микробов состоит в переносе электронов при осуществлении процесса фотосинтеза. В последнее время показано, что посттрансляционная модификация белков путем превращения глутамильных радикалов в у-карбоксиглутамильные (см. с. 301) осуществляется витамин К-зависимой карбоксилазой, локализированной в мембране эндоплазматической сети. Роль витамина К при этом сводится к отнятию атома водорода от у-углеродного атома радикала глутаминовой кислоты.
Источниками витамина К для человека являются томаты, капуста, тыква, зеленые части растений, печень животных. Кроме того, витамин К синтезируется микробами, нормально обитающими в кишечнике. Кишечная микрофлора — постоянный поставщик витамина К для человека и животных.
Витамин Q (убихинон). Эта группа жирорастворимых витаминов открыта совсем недавно. Она очень близка по строению и, вероятно, по функциям к витаминам Е и К, что явилось формальным основанием для зачисления убихинонов в разряд витаминов. В 1955 г. убихинон был впервые выделен из жира животных.
Витамины Q распространены повсеместно. Они найдены в микроорганизмах, растениях, теле человека и животных, в пищевых веществах. Поэтому чрезвычайно трудно установить их незаменимость в пище и доказать, что они не синтезируются самим животным организмом. Тем не менее в опытах с пищевой недостаточностью на обезьянах, крысах, кроликах, цыплятах, индюках и хомяках показана витаминная активность убихинонов. Полагают, что если полиизопреноидная боковая цепь витамина Q может легко синтезироваться в животном организме, то циклическая хиноидная часть, видимо, в нем не создается. Химическая структура и механизм действия убихинона рассмотрены на с. 121, а его участие в функционировании дыхательной цепи — в гл. X.
Источником витамина Q являются растительные и животные ткани, в которых протекают интенсивные окислительно-восстановительные процессы. Так, например, высокой концентрацией убихинона (n = 10) отличаются сердечная мышца, печень и бурая жировая ткань животных, впадающих в зимнюю спячку. Убихинон (n = 10) применяют в терапии сердечно-сосудистых заболеваний.
Витамин F (комплекс ненасыщенных жирных кислот). В этот комплекс входят линолевая, линоленовая, арахидоновая и, возможно, некоторые другие ненасыщенные высшие кислоты. Биологически наиболее активны арахидоновая и линолевая кислоты; линоленовая кислота усиливает действие линолевой кислоты. В 1928 г. Гоген и Гантер предложили считать эти три кислоты витамином. Линолевая и линоленовая кислоты получены синтетически.
Принадлежность высших ненасыщенных жирных кислот к витаминам признается не всеми, так как неизвестна их каталитическая функция в организме и отсутствуют явные признаки авитаминозов у человека. Однако при исключении линолевой, линоленовой и арахидоновой кислот из корма крыс и собак наблюдались яркие симптомы F-авитаминоза: сухость и шелушение кожи, выпадение шерсти, омертвение кончика хвоста, задержка роста и падение в весе.
Витамин F участвует в регуляции обмена липидов. Особенно важно, что непредельные высшие жирные кислоты способствуют выведению из организма животных и человека холестерола, а это препятствует развитию атеросклероза. Отмечено также положительное действие витамина на состояние кожного и волосяного покровов.
Механизм действия витамина F неизвестен. В специальном исследовании с применением ряда синтетических непредельных кислот выявлено, что биологическая активность ненасыщенных жирных кислот связана с наличием двойных связей между 6—7-м и 9—10-м углеродными атомами.
В последние годы прояснился биохимический эффект действия арахидоновой кислоты: она оказалась предшественником нового типа гормонов — простагландинов:
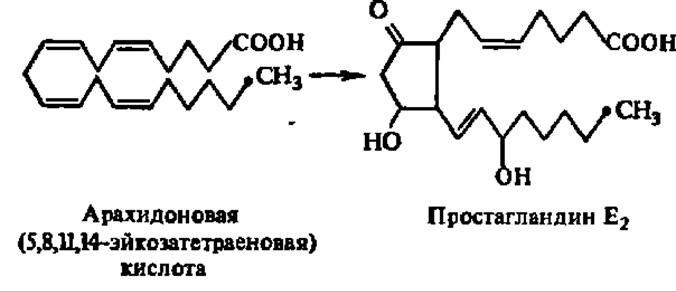
Из арахидоновой кислоты и других полиеновых кислот синтезируется около 20 различных простагландинов, оказывающих мощное влияние на обмен веществ и физиологические функции у человека и животных. В частности, ряд простагландинов влияет на деятельность гладких мышц сосудов матки и других органов и тканей, в связи с чем их используют для лечения гипертонической болезни, облегчения родов, прерывания беременности и т. п. (см. с. 463).
Витамин B1(тиамин). Витамин B1занимает особое место в истории учения о витаминах — это первый кристаллический витамин, полученный в лаборатории. Впервые его исследовал польский ученый К. Функ в 1912 г., а уже в 1913 г. витамин B1 был получен в виде кристаллов, в 1936 г. — синтезирован. Строение витамина B1таково:
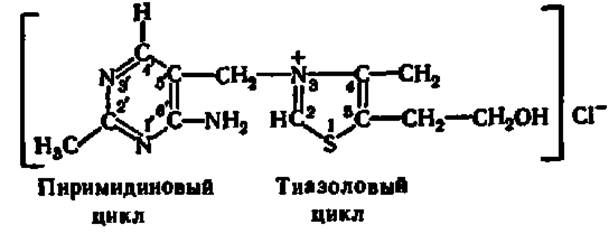
Так как витамин В1 наряду с аминогруппой содержит в молекуле атом S, ему было дано химическое название — тиамин (от греч. тион — сера).
В приведенной выше форме, т. е. в виде соли четырехзамещенного аммонийного основания (тиаминхлорид), витамин B1 существует в кислой среде. Для нейтральной и щелочной среды характерна иная структура — с разомкнутым тиазоловым кольцом; при этом в молекуле тиамина появляются свободные альдегидная и сульфгидрильная группы. Строение молекулы тиамина подтверждено синтезом.
Тиамин представляет собой мелкие бесцветные кристаллы горького вкуса, хорошо растворимые в воде. Растворы его в кислой среде устойчивы и выдерживают нагревание до высоких температур. В нейтральной и особенно в щелочной среде тиамин быстро разрушается. При окислении он переходит в тиохром — соединение, обладающее ярко-синей флуоресценцией в ультрафиолетовом свете, благодаря чему, его легко определить количественно.
При В1-авитаминозе развивается заболевание, получившее название полиневрита (болезнь «бери-бери»). Оно состоит в прогрессирующей дегенерации нервных окончаний и проводящих пучков, следствием чего являются потеря кожной чувствительности, нарушение нормальной моторики желудочно-кишечного тракта, сердечные боли и т. п.; в конце концов наступает паралич и смерть. Кроме человека, заболеванию подвержены птицы, кролики, собаки, крысы, морские свинки и многие другие животные.
Механизм действия витамина B1 детально исследован. При посредстве тиамин-пирофосфокиназы (олигомер из субъединиц с молекулярными массами 27000 и 30000 Да и максимальной активностью у тетрамера), переносящей остаток пирофосфата с АТФ на тиамин, он превращается в тиаминпирофосфат:
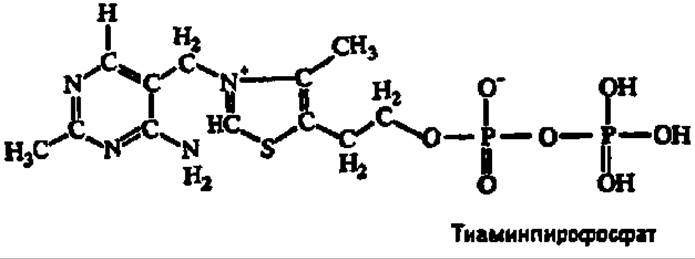
Недавно обнаружено, что тиаминпирофосфат может фосфорилироваться далее при участии тиаминдифосфаткиназы; возникающей тиаминтрифосфат считают запасной формой тиаминпирофосфата, хотя есть уже данные о его абсолютной незаменимости для функционирования нервной ткани. Тиаминпирофосфат является коферментом декарбоксилаз кетокислот. При декарбоксилировании, в частности, пировиноградной кислоты сначала образуется промежуточное соединение, распадающееся далее с выделением СO2:
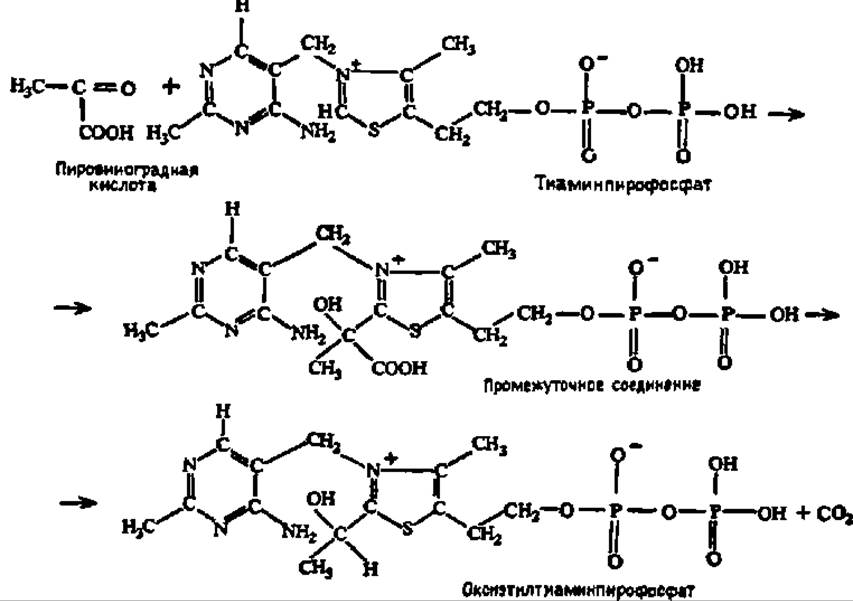
Образование промежуточного соединения пировиноградной и других а-кетокислот с тиаминпирофосфатом объясняется своеобразием его электронной структуры: второй углеродный атом тиазола обладает повышенной электронной плотностью вследствие диссоциации от него протона; поэтому к нему легко присоединяется а-углеродный атом кетокислоты, характеризующийся дефицитом электронной плотности.
Оксиэтилтиаминпирофосфат, в свою очередь, распадается с высвобождением тиаминпирофосфата и продукта деструкции пировиноградной кислоты либо в виде ацетальдегида, который далее превращается в этиловый спирт, либо в виде ацетил-КоА (см. с. 352). Самое главное состоит в том, что при этом устраняется сама пировиноградная кислота, возникающая в больших количествах при распаде углеводов (и частично аминокислот). Она является сильным ядом для нервной системы, действие которого приводит к тяжелым последствиям, отмеченным выше при рассмотрении В1-авитаминоза.
Тиаминпирофосфат катализирует также реакции переноса двууглеродных фрагментов, будучи коферментом соответствующих ферментов. Нарушение этих процессов при недостатке витамина сказывается на состоянии организма и тоже проявляется как В1-авитаминоз. В последнее время привлекают внимание некоферментные функции фосфорных производных витамина B1: участие их в реакциях фосфорилирования, регуляции обмена фосфолипидов и др.
Источником витамина B1 для человека являются главным образом хлеб и крупы в тех случаях, когда зерно в процессе технологической обработки не теряет зародышей и оболочек, которые в основном содержат тиамин (ржаная мука, неполированный рис и т. д.). Очень много витамина B1в пекарских и пивных дрожжах.
Витамин В2 (рибофлавин). Растворы этого витамина ярко-желтого цвета, характеризующиеся желто-зеленой флуоресценцией, были получены еще в прошлом столетии, но лишь в 1932 г. препарат был выделен в концентрированном виде, а затем получен в виде оранжевых кристаллов в форме игл, собранных в друзы (tпл=282°С), или пластинок (tпл = 290° С). В настоящее время витамин В2 синтезирован.
Основу молекулы рибофлавина составляет изоаллоксазин, в котором сочетаются бензольный, пиразиновый и пиримидиновый циклы. Производное изоаллоксазина, метилированное в положениях 6 и 7, а в положении 9 имеющее остаток пятиатомного спирта — рибита, и есть витамин В2. Его химическое название «рибофлавин» отражает наличие в молекуле остатка рибита и желтый цвет окисленной формы препарата. По строению это 6,7-диметил-9-рибитилизоаллоксазин:
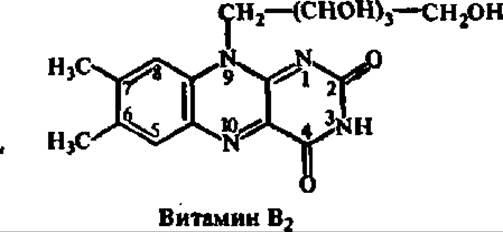
Рибофлавин химически неустойчив, легко разрушается при кипячении и на свету. Под действием света он распадается на рибит и 6,7-диметилизоаллоксазин, или люмихром. Особенно важна способность рибофлавина легко окисляться и восстанавливаться, что лежит в основе биологического действия этого витамина. Наибольшей способностью присоединять атомы Н обладают атомы N, находящиеся в 1-м и 10-м положениях в молекуле изоаллоксазина; у них максимальны индексы свободных валентностей (1,470 и 1,035 соответственно), характеризующие реакционные возможности в данной точке молекулы.
В2-авитаминоз у человека выражается в остановке роста, выпадении волос, поражении слизистых оболочек (особенно, в уголках рта), быстрой утомляемости зрения, понижении работоспособности, нарушении нормального синтеза гемоглобина; патологические изменения возникают и в нервной системе.
Механизм действия витамина В2 изучен. В виде фосфорного эфира (по концевой гидроксильной группе рибита) или в виде еще более сложных соединений (в частности, с нуклеотидами) рибофлавин является коферментом оксидоредуктаз (см. с. 119). Их известно около 30. Они осуществляют ряд важных реакций в организме — окисление L и D-аминокислот, альдегидов, моноаминов, пуриновых оснований (ксантиноксидаза), углеводов (глюкозооксидаза) и др. В их активных центрах часто присутствуют ионы Fe, Mo, Со; некоторые флавопротеины окисляют субстраты молекулярным кислородом, т. е. являются оксидазами, но среди них есть первичные и вторичные дегидрогеназы.
Источником витамина В2 для человека являются молоко и зеленые овощи; много витамина В2 в печени и почках животных, в пивных и пекарских дрожжах.
Витамин В3 (пантотеиовая кислота). Этот витамин, впервые обнаруженный в 1933 г., через несколько лет (1939) был получен в кристаллическом состоянии. В 1940 г. удалось расшифровать его химическую структуру и осуществить синтез. Оказалось, что это D(+)-(a, у-диокси-ß, β-диметилбутирил)-β-аланин:
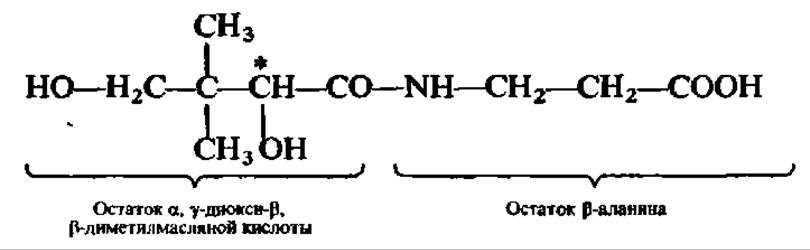
Пантотеновая кислота содержится во всех животных, растительных и микробных объектах (греч. пантотен — повсюду). Это вязкая, светло-желтая, маслянистая жидкость, смешивающаяся с водой и уксусной кислотой. Биологической активностью обладает только правовращающий (+) оптический изомер. Пантотеновая кислота малоустойчива, легко окисляется и гидролизуется в присутствии кислот и щелочей по месту пептидной (—СО—NH—)-связи.
При недостатке пантотеновой кислоты в организме человека и животных развиваются разнообразные патологические явления: поражение кожных покровов и слизистых оболочек внутренних органов, дегенеративные изменения ряда органов и тканей (особенно страдают железы внутренней секреции), потеря волосяного покрова, депигментация волос и т. д. Наиболее ярким симптомом В3-авитаминоза у человека является онемение пальцев ног, сопровождающееся покалыванием; затем возникает жгучая боль в пальцах и подошвах, распространяющаяся до голени («жжение ног»). Все это объясняется тем, что пантотеновая кислота входит в состав исключительно важного органического соединения — коэнзима А, который занимает ключевые позиции в синтезе и расщеплении жирных кислот и обеспечивает осуществление реакций, необходимых для взаимопревращения углеводов и жиров:
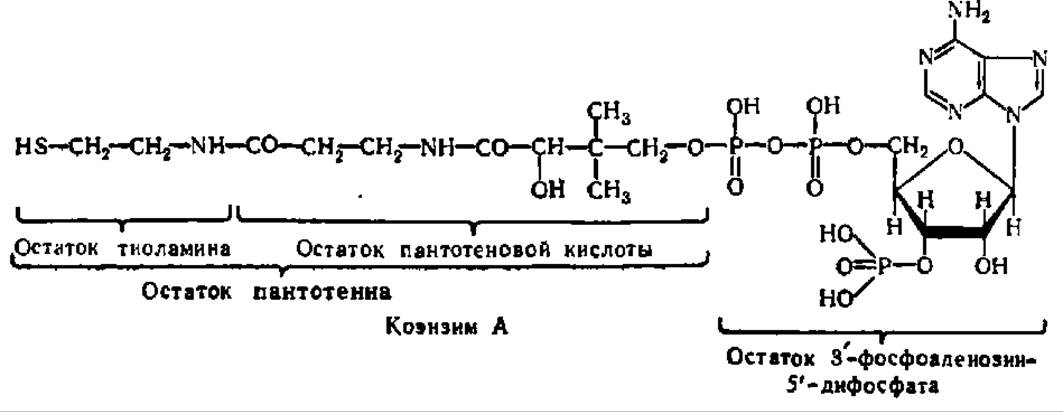
Богатым источником пантотеновой кислоты являются дрожжи, печень, яичный желток, зеленые части растений; в небольших же количествах она содержится во всех пищевых продуктах. Кроме того, пантотеновая кислота синтезируется микрофлорой кишечника.
Витамин РР (никотиновая кислота и никотинамид). Никотиновая кислота и ее амид (никотинамид, ниацин) известны очень давно:
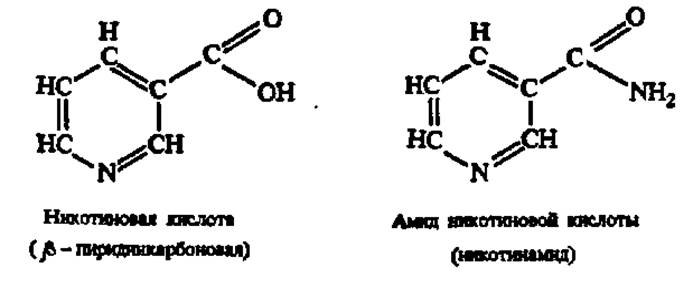
Однако только в 1937 г. было показано, что эти вещества являются витаминами, так как они предохраняют от заболевания пеллагрой и излечивают уже возникшее заболевание: pellagra (итал.) означает «жесткая или шершавая кожа». Начальные стадии заболевания пеллагрой выражаются в воспалении слизистых оболочек желудочно-кишечного тракта, а последующие — в воспалении кожи (дерматитах) на участках тела, подверженных освещению солнцем. Поэтому он назван витамином РР: по начальным буквам preventive pellagra (итал.), что означает «предотвращающий пеллагру».
Никотиновая кислота — белое, кристаллическое вещество (tпл— 235,5° С) слабокислого вкуса, хорошо растворимое (особенно при нагревании) в воде; она весьма устойчива и при действии обычных химических и физических агентов не разрушается. Аналогично ведет себя амид никотиновой кислоты, представляющий бесцветные иглы с tпл = 131—132° С.
Собственно антипеллагрическим действием обладает только амид никотиновой кислоты, а сама она является провитамином. Механизм действия никотинамида выяснен. Он входит в состав важнейшего кофермента дегидрогеназ — никотинамидадениндинуклеотида (см. с. 118) и его производного — никотинамидадениндинуклеотидфосфата.
Некоторое количество никотиновой кислоты синтезируется в организме животных и человека из аминокислоты — триптофана. Этот синтез протекает при участии витамина В6. Таким образом, РР-авитаминоз развивается при неполноценном белковом питании (мало триптофана) и недостатке витамина В6. Поэтому пеллагру в настоящее время расценивают не как чисто РР-авитаминоз, а как полиавитаминоз, т. е. заболевание, вызванное отсутствием ряда витаминов и зависящее от количества триптофана в диете.
Никотиновая кислота и ее амид широко распространены в растительных и животных объектах. Источником витамина РР для человека служит пшеничный хлеб, печень и почки животных, картофель и многие другие продукты.
Витамин В6 (пиридоксин). Витамин В6 сейчас рассматривают как сочетание трех индивидуальных веществ: пиридоксола, пиридоксаля и пиридоксамина. Каждое из них обладает свойствами витамина, ибо в организме способно перейти в пиридоксальфосфат, который собственно и участвует в химических реакциях, связанных с деятельностью данного витамина:
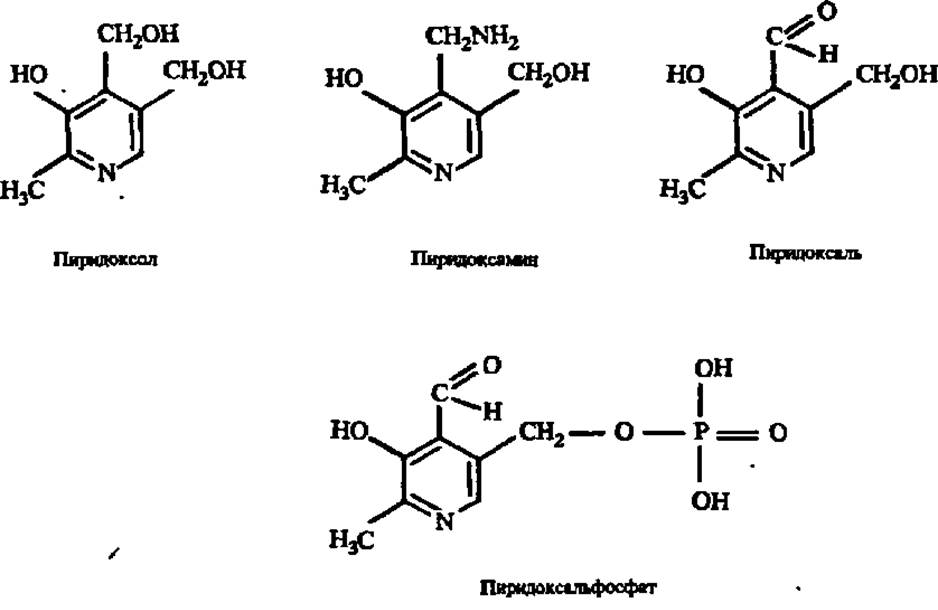
Из трех названных выше веществ, образующих пиридоксиновый комплекс, наиболее изучен пиридоксол, открытый в 1934 г. и синтезированный в 1939 г. Он представляет собой бесцветные кристаллы (tпл = 160° С), горькие на вкус, хорошо растворимые в воде и спирте. Растворы пиридоксола устойчивы к нагреванию с кислотами и щелочами, но быстро теряют активность под действием света.
Пиридоксальфосфат является коферментом в реакциях декарбоксилирования ряда аминокислот, а также реакциях переаминирования аминокислот с кетокислотами. Механизм реакции переаминирования и участия в нем пиридоксальфосфата детально рассмотрен в гл. III (см. с. 124—127).
Отсутствие в пище пиридоксина сопровождается резким нарушением обмена белков, так как реакции переаминирования аминокислот с кетокислотами обеспечивают фонд свободных аминокислот, необходимых для биосинтеза белковых тел. Основным симптомом В6-авитаминоза является нарушение кроветворения и развитие различного рода дерматитов, которые не поддаются лечению никотиновой кислотой. У молодых животных наступает остановка роста. В последнее время обнаружено, что В6-авитаминоз сопровождается нарушением обмена липидов, что ведет к развитию атеросклероза.
Источником витамина В6 для человека являются говядина, рыба, горох, яичный желток и зеленые части растений. Так как витамин Вб очень широко распространен в продуктах питания, то в обычных условиях В6-авитаминоз у человека не наблюдается.
Витамин В12 (цианкобаламин). Впервые в кристаллическом состоянии витамин В12 получен в 1948 г. Его химическая структура отличается большой сложностью; она была расшифрована в 1953 г., а затем в результате десятилетних усилий (1961—1971) выдающегося органика Р. Б. Вудворда был осуществлен синтез витамина В12.
Молекула витамина В12 состоит (рис. 62) из так называемой планарной группы, которая содержит восстановленные пиррольные кольца с атомом Со в центре, и расположенных перпендикулярно к ней двух нуклеозидных групп, имеющих диметилбензимидазол и аденин в качестве азотистых оснований и a-D-рибофуранозу в качестве углевода.
Планарная группа витамина В12 является хромофором, вследствие чего игольчатые кристаллы цианкобаламина окрашены в рубиново-красный цвет, а его водные растворы —в светло-сиреневый. Кристаллы витамина В12 темнеют при 210—220° С и плавятся при t ~ 300° С. Витамин В12 хорошо растворим в воде, спиртах, низших органических кислотах жирного ряда и фенолах, но не растворяется в бензоле, серном эфире, хлороформе и ацетоне. На свету он теряет активность, но в темноте может храниться долго и представляет собой очень устойчивое вещество. Витамин В12 оптически активен. Установлено, что в природе существует ряд соединений, обладающих активностью витамина В12. Строение нескольких из них расшифровано: в псевдовитамине В12 вместо бензимидазола содержится аденин, в факторе А—2-метиладенин, в факторе В отсутствует нуклеотидная часть и т. д.
При недостатке витамина В12 в пище человека и животных наступает нарушение нормального кроветворения в костном мозгу, приводящее к заболеванию — анемии; поэтому витамин В12 называют антианемическим.
Механизм действия витамина В12 сводится к тому, что некоторые его формы являются коферментами и, соединяясь с различными апоферментами, обеспечивают возникновение семейства кобамидных ферментов, ускоряющих важнейшие реакции азотистого, углеводного, нуклеинового и липидного обмена. Так, при посредстве метилкобаламина в качестве кофермента ускоряются реакции переноса метальных групп и осуществляется, например, биосинтез метионина. В этой реакции витамин В12 действует в паре с витамином Вc. Аденозилкобаламин входит в состав ферментов, обеспечивающих внутримолекулярный перенос атомов Н и различных химических групп (гидроксильные, аминные, карбонилтиоэфирные и др.), в соответствии со схемой:
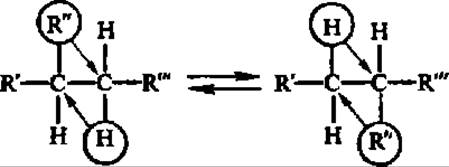
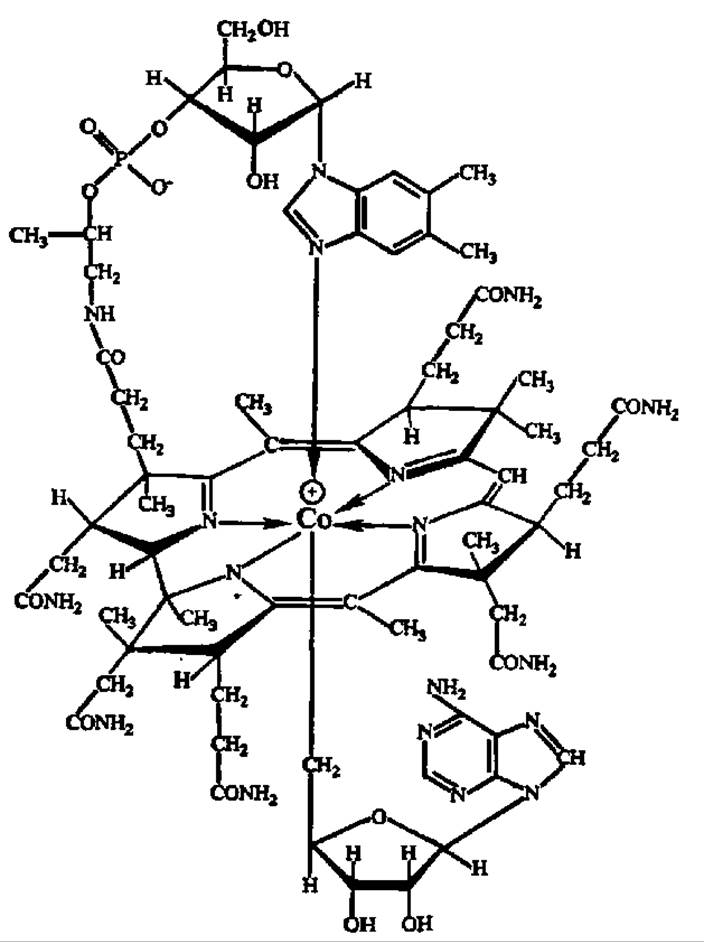
Рис. 62. Пространственная конфигурация молекулы витамина В12
Примеры таких ферментативных процессов будут рассмотрены ниже.
Депо витамина В12 у человека находится в печени, где он накапливается в количестве нескольких миллиграммов. В переносе витамина В12через кишечную стенку принимает участие соединение белковой природы, специфически связывающее витамин, — так называемый внутренний фактор. Поэтому нарушение синтеза этого фактора приводит к В12-авитаминозу даже при наличии достаточного количества последнего в пище. Часть витамина В12 по ступает в организм человека и животных в результате деятельности микробов — симбионтов кишечного тракта. Растения не содержат витамина В12, поэтому его источниками для человека служат мясо, молоко, яйца, но синтезируется он только микроорганизмами.
Витамин В12 находит очень широкое практическое применение в животноводстве. Так, добавление его к корму свиней и птицы увеличивает привесы на 15%. У птицы возрастает также яйценоскость. В нашей стране разработан дешевый способ производства витамина В12 путем микробиологического синтеза (метановое брожение на отходах ацетонобуталового производства). Налажено также производство кристаллического витамина В12 для медицинских целей. Часть кристаллического витамина В12 экспортируется.
Витамин В15 (пангамовая кислота). В 1950 г. Т. Томияма обнаружил в экстракте печени быка соединение, которое назвал витамином В15. В 1951 г. было найдено (Е. Кребс с сотр.) аналогичное вещество в водной вытяжке из ядер косточек абрикосов и названо пангамовой кислотой. Позже указанное соединение было выделено в кристаллическом состоянии из проростков риса, пивных дрожжей, печени и других источников. Оказалось, что этот витамин очень широко распространен в природе и всегда представлен в семенах растений, откуда и произошло его название (от греч. пан — всё и гами — семя). Химический состав и строение пангамовой кислоты выяснены и подтверждены синтезом:
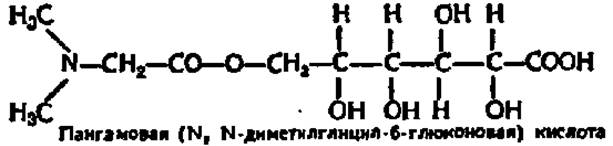
Пангамовая кислота — гигроскопичный, кристаллический белый порошок, хорошо растворимый в воде, но не растворимый в эфире, хлороформе и бензоле.
Пангамовая кислота оказывает положительное влияние на переносимость кислородного голодания (аноксия) и может быть охарактеризована как антианоксический витамин. Кроме того, она предохраняет от жирового перерождения печени. Однако до сих пор неизвестно, синтезируется пангамовая кислота в организме или она должна обязательно поступать извне.
Механизм действия пангамовой кислоты состоит в каталитическом ускорении реакций переноса метальных групп. В частности, она обеспечивает нормальный ход биосинтеза холина, метионина, креатина и креатинфосфата. Так как последний активно разрушается при функциональной перегрузке сердца, пангамат кальция применяют для лечения предынфарктного и послеинфарктного состояний.
Витамин Вс (птероилглутаминовая кислота). Первые сведения о существовании витамина Вс были получены в 1940 г. в опытах на цыплятах (отсюда индекс с — от англ. chicken — цыпленок). К 1945 г. была установлена идентичность витамина Вс с фолиевой кислотой, выделенной из листьев шпината и полученной синтетически. Этот витамин более известен под названием фолиевой кислоты, так как он содержится в значительных количествах в листьях (от лат. folium — лист). Однако фолиевых кислот было выделено несколько, и сейчас каждому представителю этой группы витаминов дают точное название в соответствии с его химической структурой. Структура одной из фолиевых кислот, птероилмоноглутаминовой, такова:
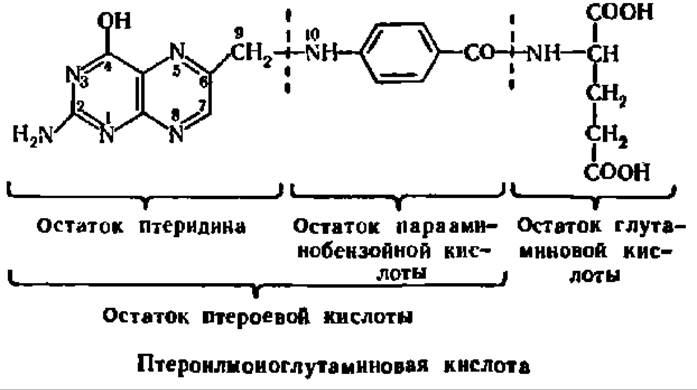
Остальные фолиевые кислоты отличаются от птероилмоноглутаминовой кислоты наличием большего или меньшего числа (от 3 до 6) остатков глутаминовой кислоты, Присоединенных к концевому остатку глутаминовой кислоты в виде у-глутамилпептида.
Фолиевая кислота представляет собой игольчатые кристаллы желтого цвета, содержащие два моля кристаллизационной воды на один моль кислоты. Они стабильны на воздухе, не могут быть охарактеризованы по температуре плавления, так как разлагаются при 250° С. Ограниченно растворимы в воде (25 мг/л), ледяной уксусной кислоте и спиртах, не растворимы в эфире, ацетоне, хлороформе. При длительном освещении фолиевая кислота разрушается.
В экспериментах установлено, что если в пище животных (например, цыплят) недостает фолиевой кислоты, у них задерживается рост и нарушается кроветворение. Очень чувствительны к недостатку витамина Вс молочнокислые бактерии, для которых он является незаменимым ростовым фактором. Человек редко страдает от Вс-авитаминоза, так как фолиевая кислота синтезируется микрофлорой желудочно-кишечного тракта и всегда поступает в организм в достаточном количестве, но в случае развития этого авитаминоза у человека он может быть охарактеризован как анемия; вместе с тем развиваются множественные нарушения деятельности органов пищеварения.
Фолиевая кислота, будучи коферментом ряда ферментов, переносит одноуглеродные фрагменты при биосинтезе многих соединений: метальную группу при биосинтезе метионина и тимина, оксиметилъную (—СН2ОН) — при биосинтезе серина, формильную
![]()
Так как указанные соединения играют ведущую роль в обмене белков и нуклеиновых кислот (недостаток метионина и серина лимитирует биосинтез белковых тел, отсутствие тимина и соответствующего ему нуклеотида — биосинтез ДНК, дефицит пуриновых оснований — новообразование ДНKи всех видов РНК), вполне понятны те нарушения жизнедеятельности, которые наблюдаются при Вс-авитаминозе.
Фолиевая кислота переносит перечисленные выше фрагменты, находясь в восстановленном состоянии, в виде 5,6,7,8-тетрагидрофолиевой кислоты. Присоединение фрагментов вдет по атому N, находящемуся в 5-м положении, при участии трифункционального фермента — формил-метенил-метилентетрагидрофолат-синтетазы (М фермента из разных источников от 150000 до 225000). Примером может служить перенос формильной группировки при биосинтезе формилметионил-тРНК (с ее присоединения к рибосоме начинается биосинтез белка — см. с. 290) в соответствии с уравнением
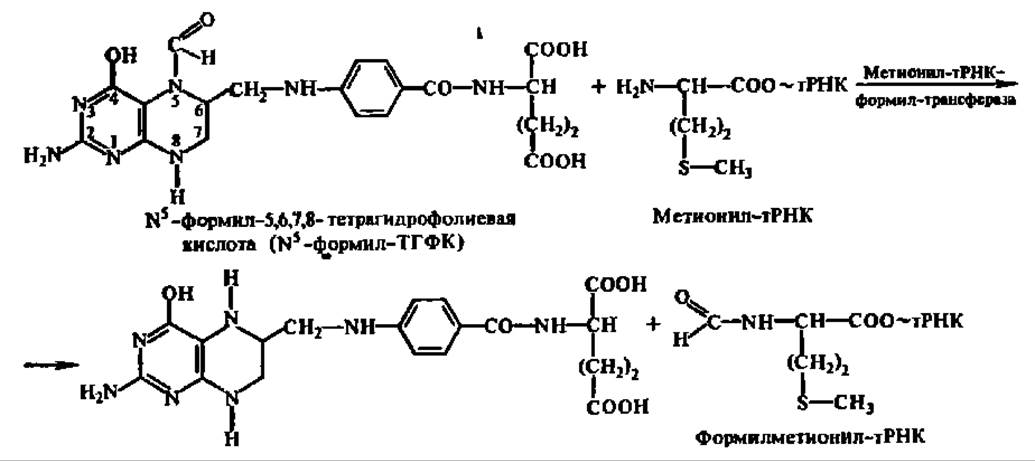
При переносе метального радикала ТГФК взаимодействует с витамином В12.
Источниками фолиевых кислот для человека являются многие продукты, в том числе шпинат, цветная капуста, печень животных, хлеб. Особенно высоко содержание фолиевой кислоты в пивных и пекарских дрожжах.
Витамин ВТ (карнитин). В 1948 г. был открыт (Г. Френкель и сотр.) особый витамин, необходимый для нормального развития и осуществления линьки у насекомых. Характерное действие этого витамина было выявлено на мучном хрущаке (Tenebrio molitor), поэтому в наименовании витамина использован соответствующий индекс.
По химической природе витамин ВТ оказался ß-окси-у-триметиламиномасляной кислотой:
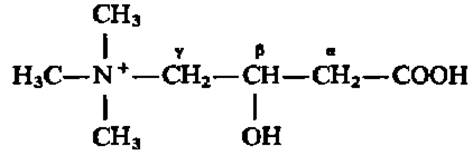
При его отсутствии в пище у ряда насекомых приостанавливается рост и наблюдается гибель во время линьки. Хотя точных исследований механизма действия карнитина нет, полагают, что он участвует у насекомых в переносе метальных групп. Такая его функция не исключена и у позвоночных, у которых он принимает также активное участие в переносе ацильных радикалов через клеточные мембраны, т. е. в конечном счете в реакциях окисления и синтеза высших жирных кислот.
Холин. Это соединение выделено из желчи более столетия тому назад. Однако только в последнее время ему приписывают функцию витамина:
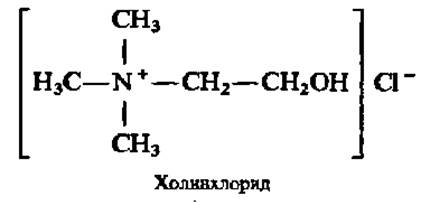
Холинхлорид — бесцветные гигроскопические кристаллы, хорошо растворимые в воде и спиртах.
Хотя холин и синтезируется в организме животных, тем не менее в определенных условиях создается его дефицит и развиваются симптомы холинавитаминоза, которые выражаются в жировом перерождении печени, кровоизлияниях в почках и других органах, сокращении объема синтеза протромбина, изменении условно-рефлекторной деятельности.
Механизм действия холина хорошо выяснен. С одной стороны, он является партнером соответствующих акцепторов в реакциях переноса метальных групп при биосинтезе ряда важнейших соединений: метионина, пуриновых и пиримидиновых оснований и т. п.; с другой стороны, холин входит в качестве составной части в активную группу биокатализатора, ускоряющего синтез фосфолипидов (см. с. 409). Кроме того, он представляет компонент ацетилхолина, участвующего в проведении нервного импульса.
Много холина содержится в желтке куриного яйца, печени и почках животных, капусте, рыбных продуктах.
Витамин С (аскорбиновая кислота). Первые сведения о существовании особого органического вещества, наличие которого в пище предохраняет от цинги (скорбута), относятся к 1885 г., когда В. В. Пашутин отверг распространенное в то время мнение, что цинга является инфекционным заболеванием, и выдвинул идею об авитаминозе как ее причине. В 1920 г. антицинготный фактор получил название витамина С, двумя годами позже он был получен в чистом виде, а в 1927 г. окончательно расшифрована его природа и дано химическое название — аскорбиновая кислота. В 1932 г. был осуществлен синтез витамина С.
Аскорбиновую кислоту можно рассматривать как производное углевода L-гулозы; поэтому его называют также у-лактоном 2,3-дегйдро-b-гулоновой
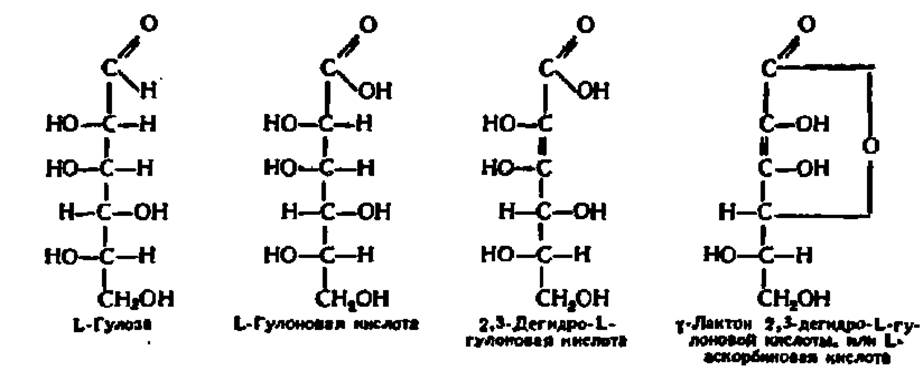
Кислотные свойства аскорбиновой кислоты, не имеющей, как видно из формулы, свободной карбоксильной группы, зависят от диссоциации водорода гидроксильной группы, расположенной у 3-го углеродного атома.
Витамин С — бесцветные кристаллы (tпл. = 192° C), кислые на вкус, хорошо растворимые в воде и спирте, но не растворимые в бензоле, хлороформе, эфире и других растворителях жиров. В бескислородной среде кристаллы аскорбиновой кислоты можно хранить годами, но в присутствии кислорода или в растворе, особенно щелочном, витамин С быстро разрушается. Разрушению способствуют ионы Fe и Сu.
Аскорбиновая кислота легко отдает два атома Н, переходя при этом в дегидроаскорбиновую кислоту, и наоборот. Это важнейшее свойство лежит в основе механизма действия аскорбиновой кислоты в организме: она является участником окислительно-восстановительных систем и обеспечивает, следовательно, нормальное протекание жизненно важных процессов в тканях.
Окисление L-аскорбиновой кислоты в L-дегидроаскорбиновую кислоту сопровождается потерей двух протонов и двух электронов:
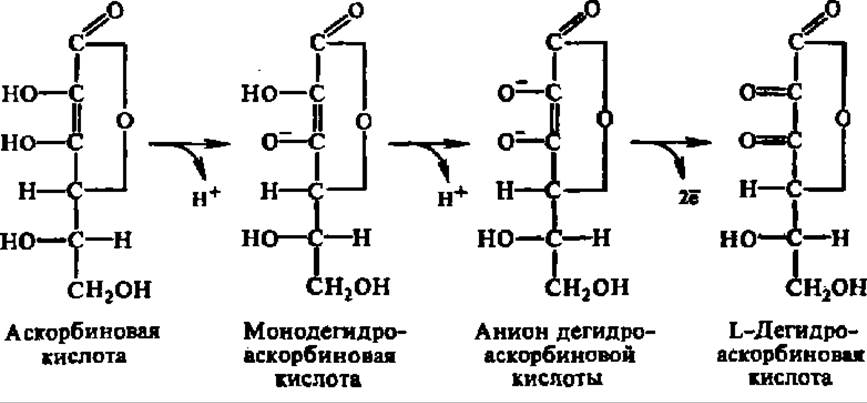
Промежуточные продукты, особенно свободный радикал монодегидроаскорбиновой кислоты, исключительно реакционноспособны и взаимодействуют со многими другими коферментами оксидоредуктаз: глутатионом, НАДН, ФАД, цитохромами и т. п. Непосредственно процесс окисления аскорбиновой кислоты ускоряется аскорбатоксидазой (см. с. 414).
Аскорбиновая кислота очень широко распространена в природе, присутствуя буквально во всех тканях и органах животных, растений, а также в микроорганизмах. Чаще всего она находится в окисленной форме, а в растениях — в виде связанной аскорбиновой кислоты, так называемого аскорбигена, возникающего при ее взаимодействии с 3-оксйметилиндолом. Аскорбиген отличается несколько более слабым физиологическим действием, но более устойчив к тем или иным физико-химическим воздействиям.
При недостаточном поступлении витамина С с пищей у человека, обезьян и морских свинок развивается специфическое заболевание — цинга. Болезнь выражается в повышении проницаемости и хрупкости кровеносных сосудов, вследствие чего возникают спонтанные кровоизлияния и характерные изменения костей и зубов: зубы быстро разрушаются, расшатываются и выпадают. В основе этих явлений лежат нарушения синтеза склеивающего межклеточного белка — коллагена вследствие ослабления его посттрансляционной модификации (см. гл. VII), выражающейся в торможении окисления радикалов пролина и лизина в радикалы оксипролина и оксилизина соответственно. В результате синтезируется нефибриллярный коллаген. Это и вызывает патологические изменения сосудистых стенок и опорных тканей. Биосинтез аскорбиновой кислоты не происходит также у некоторых птиц (семейство воробьиных) и у ряда видов летучих мышей.
При оценке механизма действия аскорбиновой кислоты в настоящее время большое значение придают возможному ее участию в предохранений от окисления активных HS-групп белков, в том числе белков, обладающих биокаталитической активностью. Эту функцию выполняет восстановленная форма аскорбиновой кислоты. Естественно, что нарушение этого процесса серьезным образом сказывается на состоянии организма. Недавно показано также, что аскорбиновая кислота является активной группой фермента,
ускоряющего гидролиз некоторых тиогликозидов, например синигрина, содержащегося в семенах горчицы и хрена:
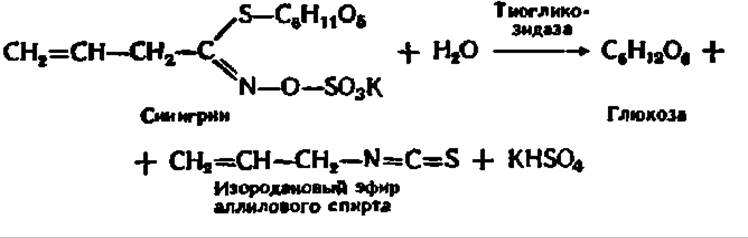
Аскорбиновая кислота выполняет также роль парного донора в некоторых монооксигеназных реакциях (см. гл. X).
Источником витамина С для человека служат самые разнообразные продукты растительного происхождения. Особенно много его содержат плоды шиповника, черная смородина, облепиха, рябина, красный перец, лимоны, капуста.
Витамин Р (рутин). В 1936 г. из кожуры лимона было выделено (А. Сцент-Дьердьи и сотр.) вещество, улучшающее состояние капилляров, и названо витамином Р (от лат. реrmео — проникать). Витамин Р, который в последнее время условно обозначают как рутин, представляет семейство веществ, близких по химической структуре. В основе всех их лежит скелет флавона:
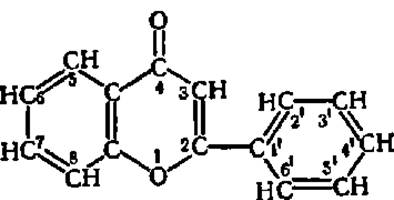
В настоящее время известно свыше десятка соединений, обладающих Р-витаминным действием. Их называют биофлавоноидами. Они отличаются различной степенью гидроксилирования бензольных колец, входящих в состав флавонового ядра, а также различными гликозидными группировками, присоединяющимися по 3-му углеродному атому пиранового цикла. В качестве примера приведем структурную формулу рутина, содержащего в своем составе остаток дисахарида — рутинозы (С12Н21O9):
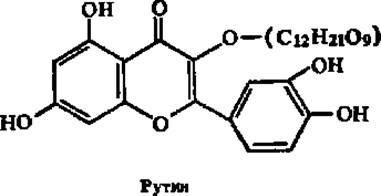
Химически чистые препараты витаминов P-группы представляют собой кристаллические вещества желтой или оранжевой окраски, труднорастворимые в воде.
При отсутствии витамина Р в пище у животных и человека повышается проницаемость капилляров, что сопровождается внезапными кровоизлияниями после сдавливания ткани, болью в конечностях, общей слабостью и быстрой утомляемостью.
Предполагают, что витамины группы Р участвуют в окислительно-восстановительных реакциях, обеспечивая таким образом нормальный ход процессов биологического окисления в организме. Действие витаминов Р и С взаимосвязано: каждый из них в присутствии другого обладает гораздо более высоким терапевтическим эффектом, чем в одиночку. Видимо, эти витамины функционируют в окислительно-восстановительных процессах вместе, образуя парное звено в соответствующей системе.
Источником витамина Р для человека являются те же продукты, в которых много витамина С, например черная смородина и лимоны. Кроме того, витамин Р содержится в значительных количествах в бруснике, чернике, клюкве, сливе, вишне, винограде и других фруктах, а также в гречихе и перце.
Витамин Н (биотин). Витаминные свойства биотина стали известны еще в 20-е годы, но только в 1936 г. удалось выделить из 250 кг яичного желтка 1,1 мг кристаллического препарата, названного биотином. В 1942 г. была установлена его структура, а годом позже осуществлен химический синтез:
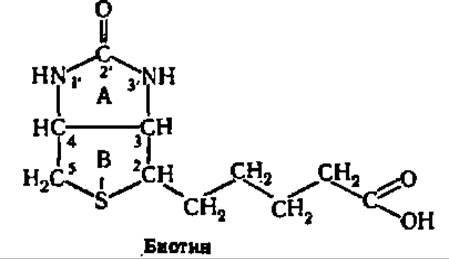
Гетероциклическая часть молекулы состоит из имидазольного (А) и тиофенового (B) циклов, а боковая цепь представлена остатком валериановой кислоты.
Бесцветные, игольчатые кристаллы биотина (fпл. = 220° С) хорошо растворяются в воде, ограниченно — в спиртах и трудно — в серном эфире. Биотин устойчив к действию молекулярного кислорода и H2SО4, но разрушается под влиянием Н2О2, бромной воды, HCl, HNО3и щелочей.
Необходимость биотина для нормальной жизнедеятельности отражена в самом его названии (от греч. биос — жизнь). При недостатке этого витамина у человека наступает ряд патологических изменений: воспаление кожных покровов, выпадение волос, усиленное выделение жира сальными железами кожи (себоррея). Защита от возникновения себорреи (от лат. sebum — сало и rheo — теку) и послужило основанием назвать биотин антисеборрейным витамином.
Механизм действия биотина, вероятно, многообразен. Полагают, что главная его роль состоит в том, что в качестве кофермента он входит в состав ферментов, ускоряющих реакции карбоксилирования.
Так, громадное значение для нормального хода биохимических процессов имеет карбоксилирование ацетил-коэнзима А, открывающее цикл реакций биосинтеза высших жирных кислот (см. с. 397). Биотин участвует не только в фиксации СО2, но и осуществляет реакции транскарбоксилирования, т.е. передачу карбоксильной группы от одного соединения к другому:
![]()
Использование биотина как кофермента в реакциях карбоксилирования и транскарбоксилирования важно для синтеза пуриновых оснований, превращения пировиноградной кислоты в щавелевоуксусную, а затем — в аспарагиновую кислоту и для осуществления ряда других реакций.
Источником витамина Н для человека являются печень и почки крупного рогатого скота, куриные яйца, молоко, томаты, соя, морковь, картофель, горох, овсяная крупа. Возможно также поступление биотина в организм за счет микробов-симбионтов; так, жвачные животные полностью обеспечиваются биотином в результате деятельности симбионтов.
Витамин U. В 1942 г. Г. Чиней на основании опытов с цыплятами, у которых вызвали язву скармливанием алкалоида цинкофена, высказал предположение, что ускоренное заживление язвы при добавлении в корм свежей зелени, некипяченого молока и сырой печени объясняется присутствием неизвестного фактора, который он назвал витамином U (от лат. ulcus — язва). В 1954 г. Р. Макрори и сотр. идентифицировали природный витамин U, выделенный ими из сока капусты в виде кристаллического бромида, с полученным синтетическим бромидом метил-метионинсульфония. Стало ясно, что витамин U является S-метилметионином:
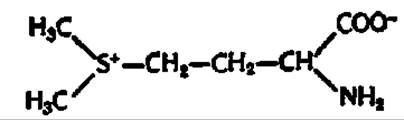
В СССР В. Н. Букин и сотр. синтезировали в 1969 г. хлорид метилметионинсульфония, нашедший широкое применение в качестве противоязвенного средства. Он представляет собой белый кристаллический порошок сладковатосолоноватого вкуса со слабым запахом капусты, хорошо растворимый в воде и водно-спиртовых смесях, но не растворимый в этаноле, глицерине и серном эфире.
Механизм лечебного действия хлорида метилметионинсульфония объясняется тем, что он является макроэргическим соединением (см. гл. V) и активным поставщиком метильных групп для химических процессов, связанных с регенерацией слизистых оболочек органов пищеварения.
Источниками витамина U для человека являются спаржа, капуста, томаты, сельдерей и зеленый чай.