Химия и биология белков - Ф. Гауровитц 1953
Сложные белки
Соединения белков с порфиринами и желчными пигментами
Количество порфиринов в жидкостях организма в норме очень невелико, при некоторых же патологических состояниях их содержание может, однако, значительно возрастать. Порфирины, как правило, соединены с альбуминами плазмы крови [230]. Зеленый пигмент хлором (пигмент лимфатических опухолей костного мозга) представляет собой протопорфирин [231]. Этот пигмент связан с нерастворимыми белками и поэтому не может быть извлечен диэтиловым эфиром.
Билирубин, увеличение содержания которого в плазме крови служит симптомом желтухи, связан с сывороточным альбумином [232]. Каждая молекула сывороточного альбумина способна связывать 3 молекулы билирубина [233].
Электрофоретические исследования показали, что не только прямой билирубин, но и так называемый непрямой билирубин движется вместе с альбуминовой и a-глобулиновой фракцией [234]. Непрямой билирубин реагирует с диазобензолсульфоновой кислотой только после предварительного прибавления к его раствору этилового спирта.
Темнокоричневая окраска сыворотки крови и испражнений, которая наблюдается в сравнительно редких случаях миодистрофии, обусловлена миобилином — сложным белком, содержащим мезобилифусцин [235]. Последний представляет собой дипиррилметан, образующийся при распаде гемоглобина или его производных.
Сложные белки, содержащие производные билирубина, были найдены также в красных водорослях (Erythrophyceae). При их обработке щелочным раствором метилового спирта получается мезобилирубин и мезобиливердин [236]. В результате распада гемоглобина in vivo образуются хромопротеиды, имеющие зеленую окраску. Первым промежуточным продуктом при распаде гемоглобина является холеглобин, состоящий из глобина и простетической группы, которая представляет собой соединение окисного железа с биливердином [237]. Билирубин содержит четыре пирроловых кольца, линейно соединенных друг с другом. В нижеследующей формуле М обозначает метальную группу (—СН3), V — винильную (—СН=СН2), Р — пропионовую кислоту (—СН2СН2СООН):
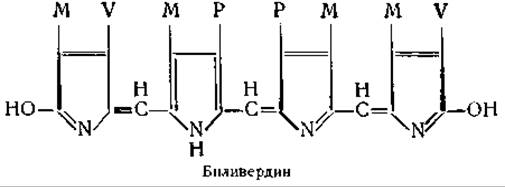
При денатурации холеглобина образуется холегемохромоген — комплекс денатурированного глобина и соединения биливердина с окисным железом [237]. При действии кислот биливердин отщепляется. Подобные же зеленые хромопротеиды, представляющие собой открытые цепи из тетрапирроловых колец, можно получить in vitro при действии на гемоглобин цианистыми солями и перекисью водорода. Эти соединения получили название вердоглобинов и псевдогемоглобинов, и их часто можно обнаружить в организме людей, принимающих сульфамиды [238]. В то время как в порфириновом кольце гемоглобина железо связано настолько крепко, что не отщепляется даже при воздействии соляной кислоты, железо, входящее в состав вердоглобинов, легко отщепляется при воздействии разведенной соляной кислоты. «Неактивный» гемоглобин, присутствующий в небольших количествах в нормальной крови, идентичен, вероятно, свердоглобином. Концентрация его составляет приблизительно 1,3% [239]. Концентрация вердоглобина в крови может быть определена при помощи спектрофотометрии [240]. Небольшие количества зеленого пигмента, сходного с холеглобином, были найдены в узелках корешков бобовых растений [241].