ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 1. ОСНОВЫ БИОХИМИИ СТРОЕНИЕ И КАТАЛИЗ - 2011
ЧАСТЬ I. СТРОЕНИЕ И КАТАЛИЗ
8. НУКЛЕОТИДЫ И НУКЛЕИНОВЫЕ КИСЛОТЫ
8.4. Другие функции нуклеотидов
Кроме роли нуклеотидов в качестве мономеров нуклеиновых кислот они имеют ряд других функций в каждой клетке: служат в качестве переносчиков энергии, компонентов кофакторов ферментов и химических сигнальных молекул.
Нуклеотиды переносят химическую энергию в клетке
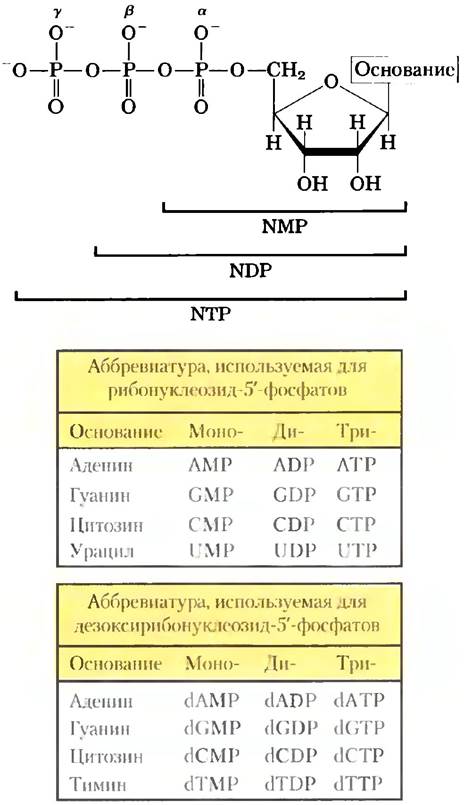
К фосфатной группе, ковалентно соединенной с 5'-гидроксильной группой рибонуклеотида, могут присоединиться одна или две дополнительных фосфатные группы. Образующиеся молекулы называются нуклеозидмоно-, нуклеозидди- или нуклеозидтрифосфатами (рис. 8-36). Считая от рибозы, три фосфата обычно обозначаются α, β, и y. При гидролизе нуклеозидтрифосфатов выделяется химическая энергия, необходимая для осуществления широкого набора клеточных реакций. Чаще всего для этой цели в клетке используется аденозин-5'- трифосфат (АТР), но в некоторых реакциях в качестве источника энергии служит UTP, GTP, или СТР. Нуклеозидтрифосфаты также используются в качестве активированных предшественников в синтезе ДНК и РНК, как описано в гл. 25 и 26.
Рис. 8-36. Нуклеозидфосфаты. Общая структура нуклеозид-5'-моно, нуклеозидди- и нуклеозидтрифосфатов (NMP, NDP и NTP) и их стандартные аббревиатуры. В дезоксирибонуклеозидфосфатах (dNMP, dNDP, dNTP) пентозой является 2'-дезокси-D-рибоза.
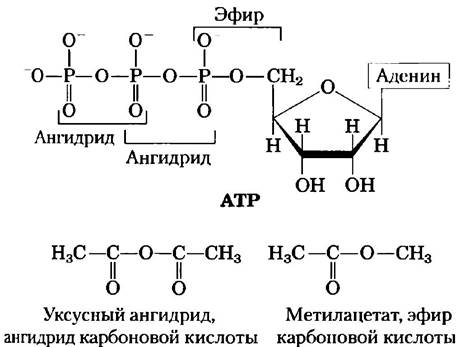
Высвобождение энергии в реакции гидролиза АТР и других нуклеозидтрифосфатов объясняется строением трифосфатной группы. Рибоза и α-фосфат соединены между собой эфирной связью. Фосфатные группы α и β, β и y соединены между собой фосфоангидридной связью (рис. 8-37). В стандартных условиях при гидролизе эфирной связи выделяется около 14 кДж/моль энергии, в то время как при гидролизе каждой фосфоангидридной связи — около 30 кДж/моль. Гидролиз АТР часто играет важную термодинамическую роль в процессах биосинтеза. Когда гидролиз АТР сопряжен с реакцией, изменение свободной энергии которой больше нуля, он сдвигает весь процесс в сторону образования продуктов (вспомните связь между константой равновесия и изменением свободной энергии (уравнение 6-3 на с. 276)).
Рис. 8-37. Фосфоэфирная и фосфоангидридные связи в молекуле АТР. При гидролизе ангидридной связи выделяется больше энергии, чем при гидролизе эфирной связи. Для сравнения показаны ангидрид карбоновой кислоты и эфир карбоновой кислоты.
Адениновые нуклеотиды входят в состав многих кофакторов ферментов
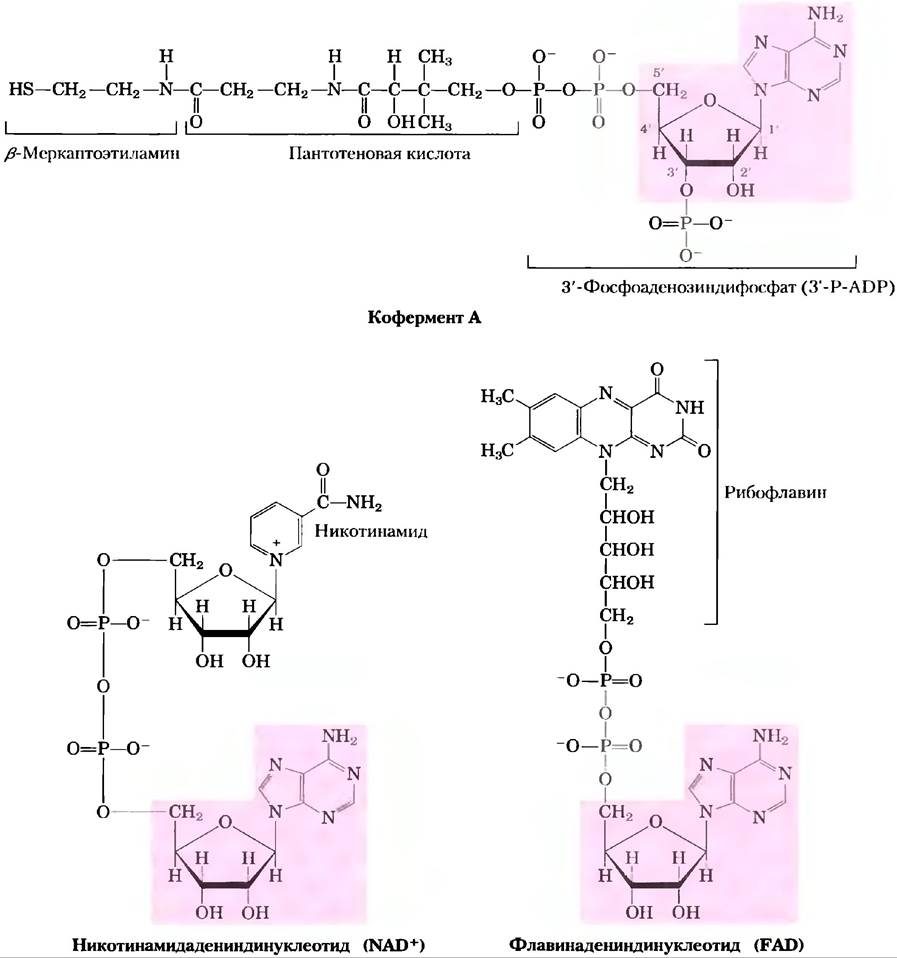
Аденозин входит в состав ряда кофакторов ферментов, которые участвуют в широком диапазоне разнообразных реакций (рис. 8-38). Структурно они не похожи друг на друга, за исключением присутствия общего компонента — аденозина. Ни в одном из этих кофакторов аденозиновая часть молекулы не принимает непосредственного участия в реакции, но при его удалении значительно уменьшается активность кофактора. Например, удаление аденинового нуклеотида (3'-фосфоаденозиндифосфата) из ацетоацетил- СоА, производного кофермента А и ацетоацетата, уменьшает его реакционную способность в качестве субстрата для β-кетоацил-СоА- трансферазы (фермент, участвующий в метаболизме липидов) в 106 раз. Хотя точно неизвестно, зачем необходим аденозин, считается, что он влияет на энергию связывания субстрата (или кофактора) с ферментом, которая влияет и на катализ, и на стабилизацию фермент-субстратного комплекса (гл. 6). В случае р-кетоацил-СоА- трансферазы нуклеотидная часть кофермента А выполняет роль «руки», которая помогает субстрату (ацетоацетил-СоА) попасть в активный центр. Похожую функцию выполняют нуклеозидные компоненты других нуклеотидсодержащих кофакторов.
Рис. 8-38. Некоторые коферменты, в состав которых входит аденозин. Аденозиновая группа выделена розовой рамкой. Кофермент А (СоА) функционирует в качестве переносчика ацильных групп; ацильная группа (такая как ацил или ацетоацетил) присоединена к СоА через тиоэфирную связь с β-меркаптоэтиламиновым фрагментом. NAD+участвует в переносе водорода, a FAD, активная форма витамина Вг (рибофлавин), — в переносе электронов. Другой аденозинсодержащий кофермент — это 5'-дезоксиаденозилкобаламин, активная форма витамина В12 (см. доп. 17-2), который участвует во внутримолекулярных перегруппировках между соседними атомами углерода.
Почему в этих структурах используется аденозин, а не какая-нибудь другая большая молекула? Одно из возможных объяснений этого может основываться на эволюционной экономии. Аденозин, конечно же, не уникальное соединение в смысле вклада потенциальной энергии в связывание между молекулами. Важность аденозина, возможно, состоит нс столько в некоторых необычных химических характеристиках, сколько в эволюционном преимуществе, связанном с использованием одного соединения для выполнения многих задач. Когда-то молекула АТР стала универсальным источником химической энергии, системы синтеза АТР стали более распространены, чем системы синтеза других нуклеотидов; широкое распространение аденозина привело к его включению в различные молекулы. Экономия распространяется и на строение белков. Для связывания аденозина разнообразными ферментами необходим всего один белковый домен, который обладает необходимыми свойствами. Такой домен, названный нуклеотидсвязывающим мотивом, найден во многих ферментах, которые связывают АТР и нуклеотидные кофакторы.
Некоторые нуклеотиды могут быть сигнальными молекулами
Клетки реагируют на условия окружающей среды, воспринимая сигналы от гормонов или других внешних химических раздражителей. Взаимодействие между этими внеклеточными химическими веществами («первичными мессенджерами») с рецепторами на поверхности клетки всегда ведет к образованию вторичных мессенджеров внутри клетки, которые в свою очередь приводят к адаптационным изменениям внутри клетки (гл. 12). Часто роль вторичного мессенждера играет нуклеотид (рис. 8-39). Один из наиболее распространенных — это циклический 3',5'-аденозинмонофосфат (циклический АМР, сАМР), образующийся из АТР в реакции, катализируемой аденилатциклазой, ферментом, связанным с внутренней поверхностью плазматической мембраны. Циклический АМР обладает регуляторными функциями практически в каждой клетке, кроме клеток растений. Циклический 3',5'-гуанозинмонофосфат (cGMP) встречается во многих клетках и также выполняет регуляторные функции.
Рис. 8-39. Три сигнальных нуклеотида.
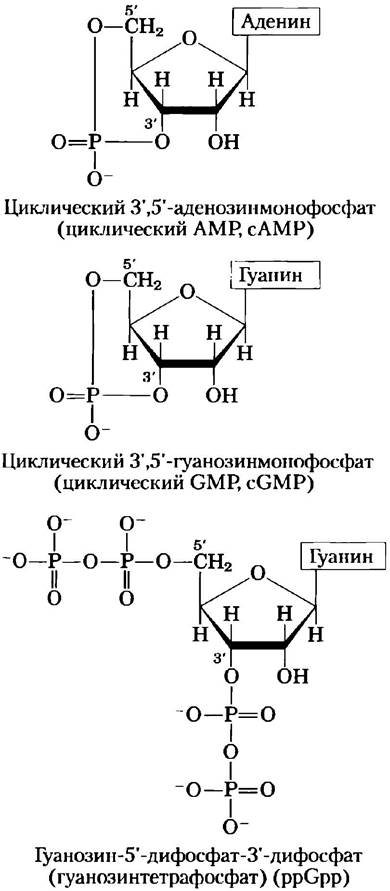
Другой сигнальный нуклеотид, ppGpp (рис. 8-39), образуется в клетках бактерий в ответ на снижение скорости синтеза белка в условиях нехватки аминокислот. Этот нуклеотид ингибирует синтез молекул рРНК и тРНК (см. рис. 28-24), необходимых для синтеза белков, что предотвращает ненужное образование нуклеиновых кислот.
Краткое содержание раздела 8.4 Другие функции нуклеотидов
■ Молекула АТР играет центральную роль в процессах переноса химической энергии в клетках. Аденозин также может обеспечивать потребности в энергии, необходимой для образования химических связей, когда входит в состав некоторых кофакторов ферментов.
■ Циклический АМР, образованный из АТР в реакции, катализируемой аденилатциклазой, служит типичным вторичным мессенджером, синтезируемым клеткой в ответ на гормоны и другие внешние химические сигналы.