ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 2. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ - 2014
ЧАСТЬ II. БИОЭНЕРГЕТИКА И МЕТАБОЛИЗМ
19. ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ И ФОТОФОСФОРИЛИРОВАНИЕ
19.3. Регуляция окислительного фосфорилирования
Основные количества необходимого АТР в аэробных клетках синтезируется в процессе окислительного фосфорилирования. На каждую молекулу глюкозы, полностью окисленную до СO2, образуется от 30 до 32 молекул АТР (табл. 19-5). При полном окислении пальмитоил (16:0)-СоА, которое также протекает в митохондриальном матриксе, образуется 108 молекул АТР на одну молекулу пальмитоил-СоА (см. табл. 17-1). Аналогичные расчеты выхода АТР можно произвести для процессов окисления каждой из аминокислот, что подробно обсуждается в гл. 18. Для сравнения при гликолизе в анаэробных условиях, т. е. при молочнокислом брожении, на каждую окисленную молекулу глюкозы образуется только 2 молекулы АТР. Эти примеры показывают, что эволюционное развитие процесса окислительного фосфорилирования привело к резкому увеличению энергетической эффективности процессов катаболизма. Процессы окисления в аэробных клетках включают перенос электронов по дыхательной митохондриальной цепи и сопровождаются окислительным фосфорилированием, и исключительно важное значение имеет возможность определения количества образующегося АТР, а также понимание механизма регулирования процесса его образования в соответствии с меняющимися нуждами клетки.
Таблица 19-5. Выход АТР при полном окислении глюкозы
Процесс |
Прямой продукт |
Выход АТР |
Гликолиз |
2 NADH (в цитозоле) 2 АТР |
3 или 5* 2 |
Окисление пирувата (2 мол. на 1 мол. глюкозы) |
2 NADH (в митохондриальном матриксе) |
5 |
Окисление ацетил-СоА |
6 NADH (в митохондриальном матриксе) |
15 |
в цикле лимонной кислоты |
2 FADH2 |
3 |
(2 мол. на 1 мол. глюкозы) |
2 АТР или 2 GTP |
2 |
Суммарный выход АТР |
30 или 32 |
* Число образовавшихся молекул АТР зависит от типа челночной системы, переносящей восстановительные эквиваленты в митохондриях.
Образование АТР при окислительном фосфорилировании регулируется энергетическими потребностями клетки
Интенсивность дыхания митохондрий, т. е. скорость потребления O2, регулируется в клетках с высокой точностью. В общем случае скорость потребления кислорода ограничена концентрацией ADP, в результате фосфорилирования которого в митохондриях образуется АТР. Зависимость скорости потребления кислорода от концентрации ADP— акцептора фосфата — называют акцепторным контролем дыхания. Коэффициент акцепторного контроля — отношение максимального потребления кислорода в присутствии ADP к его потреблению в состоянии покоя, и в различных тканях животных это отношение равно или больше 10.
Одной из характеристик энергетического состояния клеток служит внутриклеточная концентрация ADP, которую можно выразить через отношение действующих масс системы ATP-ADP: [АТР] / [ADP] [Pi]. Обычно это отношение очень велико, т. е. система ATP-ADP почти полностью фосфорилирована. Если скорость любых клеточных процессов, например, синтез белков, требующих затрат энергии (расходования АТР), возрастает, то увеличивается скорость расщепления клеточного АТР до ADP и фосфата, в результате чего отношение действующих масс уменьшается. Увеличение концентрации ADP автоматически приведет теперь к повышению скорости переноса электронов и окислительного фосфорилирования, а, следовательно, к усилению регенерации АТР из ADP. Это будет продолжаться до тех пор, пока отношение действующих масс не вернется к своему нормальному высокому значению; в этот момент дыхание снова замедлится. Скорость окисления клеточного «топлива» регулируется обычно с такой чувствительностью и точностью, что в большинстве тканей отношение [АТР] / [ADP] [Pi] колеблется в очень узких пределах, даже когда потребность в энергии меняется. Иными словами, АТР образуется со скоростью, как раз достаточной для того, чтобы компенсировать его расход в процессах, требующих затраты энергии.
При гипоксии гидролиз АТР в клетках блокируется белковым ингибитором
Как показано в предыдущих разделах (см. рис. 11-39), фермент ATP-синтазу можно считать насосом по выкачиванию протонов из митохондриального матрикса в межмембранное пространство, работающим за счет энергии АТР и катализирующим процесс, обратный синтезу АТР. Если клетка находится в состоянии гипоксии, т. е. лишена кислорода, как это бывает при сердечном приступе или инсульте, поступление электронов на кислород по дыхательной цепи митохондрий прекращается, и, следовательно, приостанавливается выкачивание протонов из матрикса. Протон-движущая сила при этом исчезает. Казалось бы, в этих условиях фермент АТР-синтаза должен катализировать обратную реакцию — гидролиз АТР, чтобы поставлять энергию для выкачивания протонов из матрикса. Но это привело бы к уменьшению концентрации АТР в клетке до гибельного уровня. Поэтому никакого гидролиза АТР не происходит — АТРазная (гидролизующая) активность АТР-синтазы в этих условиях блокируется небольшим белковым ингибитором IF1, состоящим из 84 аминокислот (рис. 19-31). Ингибитор IF1 образует связи одновременно с двумя молекулами АТР-синтазы. Активность IF1 проявляется при pH <6,5, когда он существует в виде димера. Без доступа кислорода АТР образуется в клетках главным образом путем гликолиза, в процессе которого выделяются также пировиноградная и молочная кислоты, понижающие pH цитозоля и митохондриального матрикса. Таким образом, при прекращении доступа кислорода в клетки в них создаются условия для образования димерной формы белка IF1, которая блокирует гидролизующую активность АТР-синтазы, в результате чего предотвращается бесполезный расточительный гидролиз АТР. При возобновлении аэробных метаболических процессов концентрация пировиноградной кислоты уменьшается, pH в цитозоле увеличивается, вследствие чего димер белкового комплекса IF1 распадается и восстанавливаются функции фермента АТР-синтазы.
Рис. 19-31. Строение комплекса регуляторного белка IF1 с F1-АТРазой, выделенной из клеток быка (PDB ID 10НН). Белковый ингибитор IF1 (красная спираль) соединяется с двумя молекулами фермента Fx (его структуру см. на рис. 19-25, г) через центры связывания, расположенные между соседними α,β-субъединицами, α-ADP- и β-ADP- конформации (соответственно) в «головке» F1. Светлые спирали — части ингибитора IF1, которые легко выделяются из кристаллов изолированного IF1, но не могут быть получены из кристаллов его комплекса с ферментом F1. Комплекс IF1 с ферментом F1 существует только при низких pH в цитозоле, т. е. при гликолитических процессах образования АТР. При возобновлении аэробных метаболических процессов pH в цитозоле увеличивается, действие ингибитора прекращается и функции АТР-синтазы восстанавливаются.
Гипоксия приводит к образованию АФК и некоторым адаптационным реакциям
В условиях гипоксии в клетках нарушается баланс между поступлением электронов от оксиления топливных молекул в митохондриальном матриксе и переносом электронов к молекулярному кислороду, в результате чего происходит усиленное образование активных форм кислорода (АФК). Наряду с глутатионпероксидазой (рис. 19-18) в клетках есть две другие линии защиты от радикалов кислорода (рис. 19-32). Первая из них заключается в регуляции фермента пируватдегидрогеназы (РDН), поставляющей в цикл лимонной кислоты ацетил-СоА (гл. 16). В условиях гипоксии киназа пируватдегидрогеназы фосфорилирует митохондриальную РDН, инактивируя ее и замедляя поставку FАDН2 и NАDН из цикла лимонной кислоты в дыхательную цепь. Второй путь, предотвращающий образование АФК, состоит в замене одной субъединицы комплекса IV, известной как цитохром-с-оксидаза 4-1 (СОХ4-1), на другую субъединицу — цитохром-с-оксидазу 4-2 (СОХ4-2), которая лучше приспособлена к условиям гипоксии. Каталитические свойства комплекса IV, содержащего СOX4-1, оптимальны для дыхания в условиях нормальной концентрации кислорода, а при наличии СОХ4-2 комплекс IV оптимизирован для условий гипоксии.
Рис. 19-32. Индуцируемый гипоксией фактор НIF-1 регулирует экспрессию генов, уменьшающих образование активных форм кислорода (АФК). При недостатке кислорода (гипоксии) НIF-1 синтезируется в больших количествах и действует как фактор транскрипции, усиливающего синтез переносчика глюкозы, гликолитических ферментов, киназы пируватдегидрогеназы, лактатдегидрогеназы, субъединицы цитохром-с-оксидазы СOХ4-2 и протеазы, разрушающей субъединицу цитохром-с-оксидазы СOХ4-1. Эти изменения препятствуют образованию АФК путем снижения синтеза NАDH и FАDН2, а также с помощью оптимизации действия цитохром-с-оксидазы комплекса IV. Толстыми серыми стрелками обозначены реакции, стимулируемые НIF-1, тонкими штриховыми стрелками — реакции, ингибируемые НIF-1.
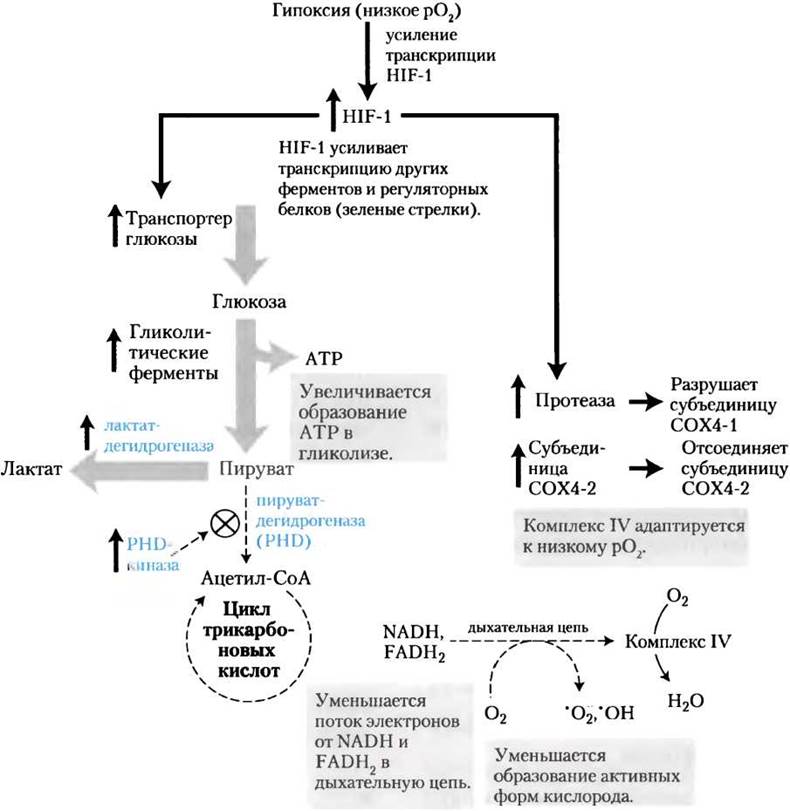
Изменение активности PDH и замена СOХ4-1 на СОХ4-2 в составе комплекса IV происходят при участии индуцируемого гипоксией фактора HIF-1 (от англ. hypoxia-induciblefactor-1). При гипоксии это вещество накапливается в клетках и действует как фактор транскрипции, усиливает синтез киназы пируватдеги- дрогеназы, СОХ4-2 и протеиназ, разрушающих СOХ4-1. Напомним, что HIF-1 также опосредует изменения транспорта глюкозы и гликолитических ферментов, что приводит к эффекту Пастера (уменьшению скорости потребления глюкозы и прекращению накопления лактата в присутствии кислорода; см. доп. 14-1).
Если перечисленных механизмов защиты от АФК оказывается недостаточно (что может быть связано с генетическими мутациями одного из защитных белков или с чрезвычайно высокими скоростями образования АФК), функционирование митохондрий нарушается. Возможно, нарушения работы митохондрий вносят свой вклад в процесс старения организма, в развитие болезней сердца, некоторых редких форм диабета (см. ниже) и некоторых наследуемых по материнской линии генетических заболеваний, поражающих нервную систему. ■
Все стадии синтеза АТР при катаболизме углеводов координируются взаимосвязанными регуляторными механизмами
Главные стадии катаболизма имеют собственные взаимосвязанные регуляторные механизмы, благодаря которым все стадии катаболизма функционируют в едином экономичном и саморегулируемом режиме. Взаимосвязанно протекают процессы образования АТР и некоторых промежуточных продуктов, используемых в качестве предшественников в реакциях биосинтеза других клеточных компонентов. Относительные концентрации АТР и ADP, иными словами, отношение действующих масс в системе ATP-ADP, определяют не только скорость переноса электронов и окислительногофосфорилирования, но и скорость цикла лимонной кислоты, окисления пирувата и процесса гликолиза (рис. 19-33). При увеличении расхода АТР, т. е. уменьшении его концентрации, возрастает концентрация ADP и фосфата и увеличивается скорость переноса электронов и скорость окислительного фосфорилирования. Одновременно повышается скорость окисления пирувата через цикл лимонной кислоты, таким образом, усиливается приток электронов в дыхательную цепь. Эти события в свою очередь приводят к увеличению скорости гликолиза, обеспечивая усиленное образование пирувата. Когда же концентрация ADP вследствие превращения его в АТР устанавливается на низком уровне, перенос электронов и окислительное фосфорилирование замедляются. Цикл лимонной кислоты и гликолиз при этом тоже замедляются, потому что АТР действует как аллостерический ингибитор ферментов фосфофруктокиназы-1 (см. рис. 15-14) и пируватдегидрогеназы (см. рис. 16-18).
Рис. 19-33. Регуляция путей образования АТР. Взаимозависимая регуляция гликолиза, окисления пирувата, цикла лимонной кислоты и окислительного фосфорилирования, определяемая относительными концентрациями ATP, ADP, АМР и NADH. При высокой концентрации АТР и, соответственно, при низких концентрациях ADP и АМР, скорости гликолиза, окисления пирувата, цикла лимонной кислоты и окислительного фосфорилирования минимальны. Если расходование АТР в клетке резко усиливается и, значит, концентрации ADP, АМР и фосфата возрастают, все эти четыре процесса ускоряются. Взаимосвязь гликолиза и цикла лимонной кислоты, осуществляемая через цитрат, подавляющий гликолиз, дополняет регуляторное действие адениннуклеотидной системы. Кроме того, при повышении концентрации NADH и ацетил-СоА подавляется процесс окисления пирувата до ацетил-СоА, а при высоком значении отношения [АТР] / [ADP] подавляются дегидрогеназные реакции в цикле лимонной кислоты (см. рис. 16-18).
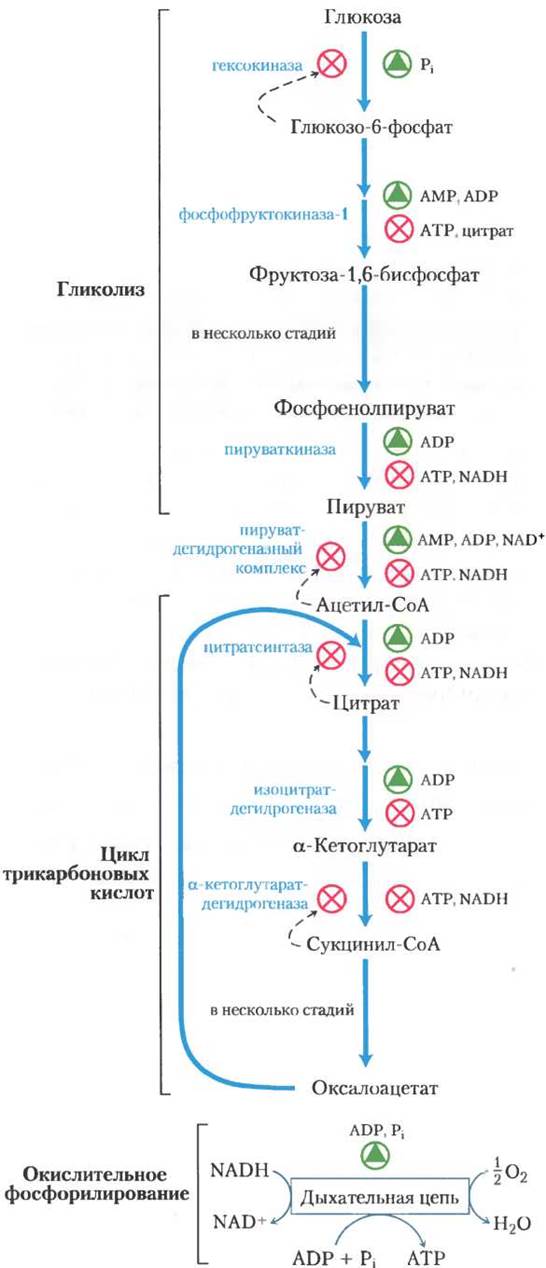
Фосфофруктокиназа-1 также ингибируется цитратом — первым промежуточным продуктом цикла лимонной кислоты. Во время «холостого» цикла цитрат накапливается в митохондриях и затем выбрасывается в цитозоль. Когда концентрации АТР и цитрата начинают превышать их обычный уровень, они, действуя согласованно, вызывают аллостерическое ингибирование фосфофруктокиназы-1, причем эффект от такого двойного ингибирования оказывается большим, чем сумма индивидуальных эффектов.
Краткое содержание раздела 19.3 Регуляция окислительного фосфорилирования
■ Окислительное фосфорилирование регулируется энергетическими потребностями клетки. Концентрация ADP внутри клеток и отношение действующих масс [АТР] / [ADP] [Pi]отражают энергетическое состояние клеток.
■ При гипоксии, т. е. при недостаточном поступлении кислорода в клетки, белковый ингибитор блокирует фермент АТР-синтазу, которая в таких условиях вызывает гидролиз АТР, в результате чего предотвращается понижение концентрации АТР до опасного для клеток уровня.
■ Адаптация к условиям гипоксии, опосредованная действием HIF-1, заключается в замедлении передачи электронов по дыхательной цепи и оптимизации комплекса IV для работы в условиях недостатка кислорода.
■ Скорости гликолиза, цикла лимонной кислоты и процесса окислительного фосфорилирования согласованы между собой. Эта согласованность обеспечивается взаимосвязанными регуляторными механизмами, реагирующими на концентрации АТР и ADP