Основы биохимии Том 2 - А. Ленинджер 1985
Биоэнергетика и метаболизм
Перенос электронов, окислительное фосфорилирование и регуляция синтеза АТР
Каким образом окислительно-восстановительная энергия переноса электронов передается АТР-синтетазе?
В предыдущих разделах этой главы мы рассмотрели процесс переноса электронов и познакомились со структурой АТР-синтетазы. Теперь пришло время задать главный вопрос: каким же образом цепь переноса электронов взаимодействует с ATP-син гетазой и как при этом происходит окислительное фосфорилирование ADP с образованием АТР? Это один из самых увлекательных и вместе с тем самых трудных вопросов в биохимии и цитологии. Хотя нам сегодня известно уже немало об утилизации энергии АТР в биосинтетических реакциях, тем не менее точные молекулярные механизмы генерирования АТР в процессе окислительного фосфорилирования остаются неясными. Одна из причин этого состоит в том, что ферменты переноса электронов и окислительного фосфорилирования очень сложны и к тому же встроены во внутреннюю мембрану митохондрий, чем сильно затрудняется изучение их взаимодействия. Постулировано три возможных механизма передачи энергии от процесса переноса электронов процессу синтеза АТР.
Гипотеза химического сопряжения предполагает, что перенос электронов сопряжен с синтезом АТР через определенную последовательность реакций; в ходе этих реакций некий высокоэнергетический ковалентный промежуточный продукт, образовавшийся в результате переноса электронов, расщепляется и отдает содержащуюся в нем энергию на образование АТР. Это предположение перекликается с уже известным нам примером участия 3-фосфоглицероилфосфата в качестве общего промежуточного продукта при синтезе АТР в процессе гликолиза (разд. 15.7,6).
Гипотеза конформационного сопряжения предполагает, что перенос электронов по дыхательной цепи вызывает конформационные изменения в белковых компонентах внутренней митохондриальной мембраны и тем самым переводит их в высокоэнергетическую форму. Конформационные изменения передаются молекуле F0F1-АТРазы и активируют ее. Релаксация активированной F0F1-ATPaзы, т. е. ее возвращение к обычной конформации, высвобождает запасенную в ней энергию, которая используется для синтеза АТР и для отделения новосинтезированного АТР от молекулы фермента.
Хемиосмотическая гипотеза, сформулированная английским биохимиком Питером Митчеллом, исходит из совершенно иного, нового принципа. Постулируется, что перенос электронов сопровождается выкачиванием ионов Н+ из матрикса через внутреннюю митохондриальную мембрану в наружную водную среду. Вследствие этого между двумя сторонами внутренней митохондриальной мембраны возникает градиент концентрации ионов Н+ (трансмембранный градиент). Синтез АТР, требующий затраты энергии, осуществляется именно за счет осмотической энергии, присущей этому градиенту. Можно думать, что именно хемиосмотическая теория наиболее точно отражает организующий принцип окислительного фосфорилирования. Рассмотрим некоторые характерные особенности этого процесса, свидетельствующие в пользу хемиосмотической гипотезы.
а. Никакие «высокоэнергетические» промежуточные продукты, связывающие перенос электронов с синтезом АТР, не обнаружены
Многолетние интенсивные исследования, направленные на поиск таких гипотетических промежуточных продуктов, не дали результатов: обнаружить их не удалось.
б. Окислительное фосфорилирование требует целостности внутренней митохондриальной мембраны
Окислительное фосфорилирование может происходить лишь в том случае, если целостность внутренней митохондриальной мембраны не нарушена, т. е. если эта мембрана представляет собой полностью замкнутое образование. Любые разрывы и трещины во внутренней митохондриальной мембране лишают ее способности к окислительному фосфорилированию, хотя перенос электронов от субстрата к кислороду и в этих условиях может продолжаться.
в. Внутренняя митохондриальная мембрана непроницаема для ионов Н+, ОН-, К+ и Cl-
Эго свойство мембраны также имеет отношение к окислительному фосфорилированию. Если мембрана повреждена или если она в результате какого-нибудь воздействия стала вдруг легко проницаемой для этих или для некоторых других ионов, то окислительное фосфорилирование происходить не будет. Эти наблюдения показывают, что разница в ионном составе или в концентрации между двумя сторонами внутренней митохондриальной мембраны играет важную роль в синтезе АТР.
г. Окислительное фосфорилирование можно предотвратить с помощью разобщающих агентов
Некоторые химические вещества, например 2,4-динитрофенол (рис. 17-17), подавляют фосфорилирование ADP до АТР, не влияя при этом на перенос электронов в митохондриях. Они разобщают перенос электронов и синтез АТР, разрушая необходимую связь между этими процессами. Такие вещества называются поэтому разобщающими агентами. В их присутствии свободная энергия, выделяемая при переносе электронов, переходит в тепло, а не запасается в виде АТР. Разобщающие агенты резко повышают проницаемость внутренней митохондриальной мембраны для ионов Н+. Это липофильные вещества, обладающие способностью связывать ионы Н+ по одну сторону мембраны и переносить их через мембрану на другую сторону, туда, где их концентрация ниже.
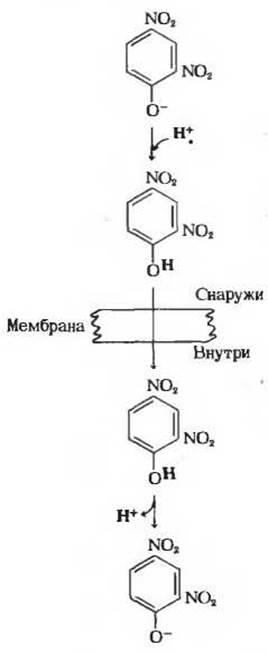
Рис. 17-17. Действие типичною разобщающею агента 2,4-динитрофенола. При pH 7 этот агент существует главным образом в виде аниона, не обладающего способностью растворяться в липидах. В протонированной форме 2,4-динитрофенол растворим в липидах и потому может проходить сквозь мембрану перенося с собой протон. По другую сторону мембраны перенесенный протон отщепляется. Действуя таким образом, разобщающие агенты препятствуют возникновению градиента концентрации ионов Н+ между двумя сторонами мембраны. Подобные разобщающие агенты, переносящие ионы Н+, называют протонофорами.
Одно время пытались использовать некоторые разобщающие агенты для борьбы с ожирением за счет понижения эффективности синтеза АТР. Оказалось, однако, что эти вещества крайне токсичны, и потому от такого их применения пришлось отказаться.
д. Некоторые ионофоры также способны подавлять окислительное фосфорилирование
Ионофорами (т.е. «переносчиками ионов») называют жирорастворимые вещества, способные связывать определенные ионы и переносить их через мембрану. От разобщающих агентов они отличаются тем, что переносят через мембрану не ионы Н+, а какие-нибудь другие катионы. Например, токсичный антибиотик валиномицин (рис. 17-18) образует жирорастворимый комплекс с ионами К+, легко проходящий через внутреннюю мембрану митохондрий, тогда как в отсутствие валиномицина ионы К+ проникают сквозь нее с большим трудом. Ионофор грамицидин облегчает проникновение через мембрану не только К+, но и N+, а также некоторых других одновалентных катионов. Таким образом, разобщающие агенты и ионофоры подавляют окислительное фосфорилирование, увеличивая проницаемость мембраны для ионов Н+, К+ или Na+.
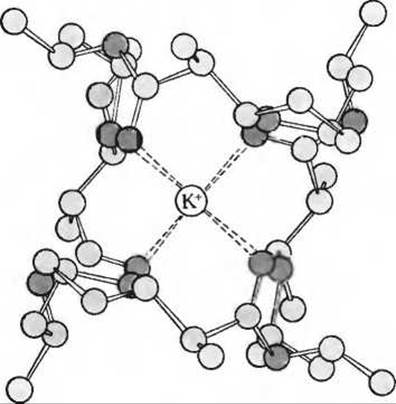
Рис. 17-18. Валиномицин - токсичный антибиотик, стимулирующий перенос ионов К+ через мембрану Этот ионофор, переносящий ионы К+. состоит из остатков L- и D-валина, лактата и гидроксиизовалерата, соединенных в кольцеобразную структуру. Валиномицин образует специфический комплекс с ионом К+ (показан красным цветом), который располагается в его гидрофильной внутренней части. Благодаря растворимой в липидах наружной части молекулы валиномицина (показана серым цветом) комплекс валиномицин—К+ легко проходит через митохондриальную мембрану.
е. Поток электронов вынуждает ионы Н+ выходить из дышащих митохондрий наружу
Энергия, выделяемая при переносе электронов по дыхательной цепи от субстрата на кислород, может при определенных условиях вызвать перенос ионов Н+ из митохондриального матрикса в среду. В результате pH митохондриального матрикса повышается, а pH среды понижается, т.е. матрикс становится более щелочным, а среда, окружающая митохондрии, более кислой. Во внутренней митохондриальной мембране имеются, следовательно, какие-то «насосы» для ионов Н+; эти насосы используют свободную энергию потока электронов для перекачивания ионов Н+ наружу против градиента концентрации. Выкачивание ионов Н+ из митохондрий приводит к появлению мембранного электрического потенциала, потому что вследствие выхода этих ионов из матрикса в среду наружная сторона мембраны становится более электроположительной, а внутренняя -более электроотрицательной. Таким образом, перенос электронов создает электрохимический градиент ионов Н+, включающий два компонента; мембранный потенциал вносит больший вклад в энергию этого градиента:

В этом уравнении величина Z представляет собой коэффициент для перевода единиц pH в милливольты, т.е. в те единицы, в которых выражают обычно ∆μн и ∆ψ. Вклад мембранного потенциала составляет приблизительно 75% всего электрохимического Н+ -градиента, создаваемого переносом электронов.