ОСНОВЫ БИОХИМИИ ЛЕНИНДЖЕРА - ТОМ 3. ПУТИ ПЕРЕДАЧИ ИНФОРМАЦИИ - 2017
ЧАСТЬ III. ПУТИ ПЕРЕДАЧИ ИНФОРМАЦИИ
28. РЕГУЛЯЦИЯ ЭКСПРЕССИИ ГЕНОВ
28.3. Регуляция экспрессии генов у эукариот
Инициация транскрипции — ключевая точка в регуляции экспрессии генов в любых организмах. Несмотря на то что у эукариотов и бактерий некоторые механизмы регуляции одинаковые, регуляция транскрипции у них принципиально различается.
Можно определить базовый уровень транскрипции как активность промоторов и всего механизма транскрипции in vivo в отсутствие регуляторных последовательностей. Бактериальная РНК-полимераза обычно имеет доступ к любому промотору и может связываться с ним и инициировать транскрипцию с некоторой эффективностью без помощи активаторов и репрессоров; следовательно, транскрипция носит пермиссивный характер. Однако обычно у эукариот сильные промоторы in vivo неактивны в отсутствие регуляторных белков, т. е. это непермиссивная транскрипция. Это принципиальное различие является причиной, как минимум, четырех важных особенностей регуляции экспрессии эукариотических генов.
Во-первых, у эукариот доступ к промоторам ограничен строением хроматина, и активация транскрипции связана со многими изменениями структуры хроматина в транскрибируемом участке. Во-вторых, хотя у эукариотических клеток есть как положительные, так и отрицательные регуляторные механизмы, положительные механизмы преобладают во всех охарактеризованных до сих пор системах. Таким образом, с учетом непермиссивного характера транскрипции, чтобы прошла транскрипция любого эукариотического гена, нужна активация. В-третьих, по сравнению с бактериями эукариоты имеют более крупные и сложно устроенные регуляторные белки, как правило, состоящие из нескольких субъединиц. Наконец, в-четвертых, транскрипция в ядрах эукариот отделена от трансляции в цитоплазме как во времени, так и в пространстве.
Как мы увидим далее, в эукариотических клетках схемы регуляции очень сложны. Мы завершим этот раздел описанием одной из наиболее подробно исследованных схем регуляции — схемы регуляторного каскада, который контролирует развитие дрозофилы.
Транскрипционно активный хроматин по структуре отличается от неактивного хроматина
Влияние структуры хромосом на регуляцию генов эукариот не имеет очевидной аналогии в клетках бактерий. В клеточном цикле эукариот интерфазные хромосомы на первый взгляд кажутся дисперсными и аморфными (см. рис. 12-43 в т. 1, рис. 24-25). Тем не менее в таких хромосомах можно обнаружить несколько форм хроматина. В типичной эукариотической клетке около 10% хроматина находится в более конденсированной форме, чем остальной хроматин. Это транскрипционно неактивный гетерохроматин. Гетерохроматин обычно связан со специальными структурами хромосомы, например, с центромерами. Остальной менее конденсированный хроматин называется эухроматином.
Транскрипция эукариотических генов внутри гетерохроматина подавлена. Напротив, некоторая часть эухроматина (но не весь) активно транскрибируется. Транскрипционно активные области хромосом характеризуются не только более свободной структурой хроматина, но также наличием нуклеосом особого состава и вида. В транскрипционно активном хроматине обычно содержится меньше гистона H1, который связывается с линкерной ДНК между нуклеосомами, но больше вариантов Н3.3 и H2AZ (см. доп. 24-2).
Гистоны из транскрипционно активного хроматина и гетерохроматина также отличаются по характеру ковалентной модификации. Гистоны из ядра нуклеосомной частицы (Н2А, Н2В, Н3, Н4; см. рис. 24-27) модифицируются путем метилирования остатков Lys, фосфорилирования остатков Ser или Thr, ацетилирования (см. ниже), убиквитинирования (см. рис. 27-47) или сумоилирования. Все гистоны нуклеосомного ядра имеют два разных структурных домена. Центральный домен участвует во взаимодействии между гистонами и в оборачивании ДНК вокруг нуклеосомы. Второй, богатый лизином N-концевой домен обычно располагается ближе к внешней стороне, собранной нуклеосомной частицы; ковалентным модификациям подвергаются специфические аминокислотные остатки именно этого домена. Характер модификаций позволяет предполагать существование гистонового кода, с помощью которого эти модификации узнаются ферментами, изменяющими структуру хроматина. Модификации, связанные с активацией транскрипции (главным образом, метилирование и ацетилирование), могли бы узнаваться ферментами, которые делают хроматин более доступным для транскрипции. И в самом деле некоторые из этих модификаций необходимы для взаимодействия с белками, выполняющими важные функции при транскрипции.
Для эукариотической ДНК характерно метилирование остатков цитозина в последовательностях CpG по пятому положению (с. 419 в т. 1), но ДНК из транскрипционно активного хроматина часто слабо метилирована. Кроме того, сайты CpG в определенных генах слабее метилированы в клетках тех тканей, где эти гены экспрессируются, чем там, где они не экспрессируются. Таким образом, подготовка хроматина к транскрипции происходит путем удаления возможных структурных преград.
Хроматин ремоделируется путем ацетилирования и перемещения нуклеосом
Связанные с транскрипцией изменения в структуре хроматина происходят в процессе ремоделирования хроматина. В ремоделировании участвуют ферменты, которые катализируют процессы модификации. Некоторые ферменты ковалентно модифицируют гистоны нуклеосомы. Другие ферменты используют химическую энергию АТР для перестановки нуклеосом на ДНК (табл. 28-2); третьи изменяют состав гистонов в нуклеосомах.
Ацетилирование и деацетилирование гистонов играет очень важную роль в процессах активации хроматина. Как отмечалось выше, N-концевые домены гистонов в ядре нуклеосомы обычно обогащены остатками Lys и Arg. В ходе транскрипции гистон Н3 метилируется (под действием специфических гистонметилаз) по остатку Lys4 в нуклеосоме вблизи 5’-конца кодирующей области и по остатку Lys36внутри кодирующей области. Метилирование облегчает связывание гистонацетилтрансфераз (HAT — от англ. histone acetyltransjerases), которые ацетилируют определенные остатки лизина. Цитоплазматические HAT (тип В) ацетилируют вновь синтезированные гистоны до того, как они поступают из цитоплазмы в ядро. Последующее встраивание гистонов в хроматин после репликации облегчается шаперонами гистонов: CAF1 для Н3 и Н4 и NAP1 для Н2А и Н2В (см. табл. 24-2).
В тех участках, где хроматин активируется для транскрипции, гистоны нуклеосом далее ацетилируются под действием ядерных HAT (тип А). Ацетилирование многочисленных остатков Lys в N-концевых доменах гистонов Н3 и Н4 может уменьшать сродство к ДНК всей нуклеосомы. Ацетилирование специфических остатков Lys играет ключевую роль во взаимодействиях нуклеосом с другими белками. Когда транскрипция гена больше не нужна, в ходе общего процесса сайленсинга (отключения) генов, который возвращает хроматин в транскрипционно неактивное состояние, под действием гистондеацетилазной (HDAC — от англ. histone deacetylases) активности ацетилирование нуклеосом в этом участке ослабевает. Наряду с удалением определенных ацетильных групп происходит новая ковалентная модификация гистонов, которая маркирует хроматин как транскрипционно неактивный. Например, часто в гетерохроматине остаток Lys9гистона Н3 метилирован.
Таблица 28-2. Некоторые ферментные комплексы, катализирующие связанные с транскрипцией структурные изменения хроматина
Ферментный комплекса |
Олигомерная структура (количество полипептидов) |
Источник |
Функции |
Модификация гистонов GCN5-ADA2-ADA3 |
3 |
Дрожжи |
GCN5 имеет активность HAT (тип А) |
SAGA PCAF |
>20 |
Эукариоты |
Включает GCN5-ADA2-ADA3; ацетилирует остатки в Н3 и Н2В |
NuA4 |
не менее 12 |
Эукариоты |
Компонент Esal имеет активность HAT; ацетилирует Н4, Н2А и H2AZ |
Перемещение и замена гистонов (с затратой АТР) SWI /SNF |
≥6; общая Мr = 2 • 106 |
Эукариоты |
Ремоделирование нуклеосом; активация транскрипции |
Семейство ISWI |
Различная |
Эукариоты |
Ремоделирование нуклеосом; подавление транскрипции; в некоторых случаях активация транскрипции (NURF) |
Семейство SWR1 |
~12 |
Эукариоты |
Связывание H2AZ |
Шапероны гистонов, которым не требуется АТР HIRA |
1 |
Эукариоты |
Связывание Н3.3 в ходе транскрипции |
d Смысл сокращенных названий эукариотических генов и белков гораздо менее очевиден, чем генов бактерий. Комплекс белков GCN5 (от англ. general conrol nonderepressible) и ADA (alteration/deficiency actuation) был открыт при изучении генов метаболизма азота в дрожжах. Эти белки могут быть частью более крупного дрожжевого комплекса SAGA (SPF ADA2,3; GCN5; acetyltransferase). Человеческий эквивалент SAGA — PCAF (р300/СВР- associated factor). NuA4 (nucléosome acetyltransf erase H4) - нуклеосомная ацетилтрансфераза H4, ESA1 (essential SAS2-related acetyltransf erase) ацетилтрансфераза, родственная SAS2. Белковый фактор SWI (switching) необходим для экспрессии определенных генов, участвующих в переключении типа спаривания у дрожжей, a SNF (sucrose nonfermenting) - регулятор экспрессии дрожжевого гена сахаразы. Впоследствии были обнаружены многочисленные белки SWI и SNF, действующие в комплексе. Комплекс SWI/SNF играет роль в экспрессии широкого круга генов; он обнаружен у многих эукариот, включая человека. ISWI (imitation SWI) имитация SWI, NURF (nuclear remodeliпц/actor) ядерный ремоделирующий фактор, SWR1 (Swi2/Snf2-relatedATPase 1) связанная с Swi2 Snf2 АТРаза 1; HIRA (histone regulator А) регулятор гистонов A.
Известно пять семейств ферментных комплексов, которые активным образом перемещают нуклеосомы при гидролизе АТР; три из них играют важную роль в активации транскрипции (табл. 28-2). Комплекс SWI/SNF, обнаруженный во всех эукариотических клетках, содержит не менее шести центральных полипептидов, которые вместе перестраивают хроматин таким образом, что нуклеосомы располагаются менее регулярно, и стимулируют связывание факторов транскрипции. В состав комплекса вблизи С-конца активной АТРазной субъединицы входит специализированный белковый домен, называемый бромодоменом, который взаимодействует с ацетилированными гистоновыми «хвостами». Комплекс SWI/SNF требуется для транскрипции не всех генов. Комплекс NURF из семейства также перестраивает хроматин, дополняя и перекрывая активность SWI/SNF. Эти два ферментных комплекса играют ключевые роли в подготовке участка хроматина к активной транскрипции. Некоторые представители третьего семейства комплексов, SWR1, участвуют в связывании варианта гистона Н2АZ с транскрипционно активным хроматином.
Некоторые представители других семейств преобразующих хроматин ферментов осуществляют перегруппировку нуклеосом в хроматине в процессе сайленсинга (отключения) генов. Общий результат перестройки хроматина — повышение доступности участка хромосомы и его «мечение» (химическая модификация) для облегчения связывания и действия транскрипционных факторов, регулирующих экспрессию гена (или генов) в этой области.
Многие эукариотические промоторы подвергаются положительной регуляции
Как уже отмечалось, эукариотические РНК-полимеразы имеют небольшое сродство к своим промоторам (или не имеют его совсем), поэтому инициация транскрипции почти всегда зависит от действия многочисленных активаторных белков. Одна важная причина явного доминирования положительной регуляции кажется очевидной — сохранение ДНК внутри хроматина обеспечивает недоступность большинства промоторов, поэтому в отсутствие других регуляторных механизмов гены не экспрессируются. Структура хроматина делает одни промоторы более доступными, чем другие, и репрессоры, которые связываются с ДНК и предотвращают доступ РНК-полимеразе (отрицательная регуляция) просто не нужны. Использование положительной регуляции объясняется и другими факторами, главным образом, двумя: гигантским размером эукариотического генома и более высокой эффективностью положительной регуляции по сравнению с отрицательной регуляцией.
В крупных геномах высших эукариот неспецифическое связывание регуляторных белков с ДНК становится серьезной проблемой. Кроме того, с увеличением размера генома повышается вероятность того, что отдельные специфические последовательности случайно могут оказаться в ненадлежащем месте. Специфичность активации транскрипции может быть повышена, если каждый белок-регулятор сначала связывает специфическую последовательность ДНК, а затем уже образует активационный комплекс с другими белками. В многоклеточном организме среднее число регуляторных участков для каждого гена, по-видимому, не менее пяти. Необходимость связывания нескольких регуляторных белков со специфическими последовательностями ДНК значительно снижает вероятность случайного функционального совпадения всех задействованных участков связывания. В принципе подобная стратегия может реализоваться и для многочисленных элементов отрицательной регуляции, но тут играет роль вторая причина преимущественного использования положительной регуляции. Эта вторая причина — более высокая эффективность положительной регуляции. Для отрицательной регуляции -29 000 генов человеческого генома каждая клетка должна была бы постоянно синтезировать такое же количество различных репрессоров (или намного больше, если каждый промотор регулируется несколькими элементами) в достаточно высокой концентрации, чтобы обеспечить специфичное связывание каждого «ненужного» гена. При положительной регуляции большинство генов обычно находится в неактивном состоянии (т. е. РНК-полимеразы не связываются с промоторами), и клетка синтезирует только белки-активаторы, необходимые для транскрипции группы генов, необходимых в данное время. Несмотря на эти аргументы, в эукариотах (от дрожжей до человека) все-таки встречаются примеры отрицательной регуляции, как мы увидим в дальнейшем.
ДНК-связывающие активаторы и коактиваторы способствуют сборке основных факторов транскрипции
Продолжая наше исследование регуляции экспрессии генов эукариот, рассмотрим взаимодействия между промоторами и РНК-полимеразой II (Pol II), ответственной за синтез эукариотических мРНК. Хотя многие (но не все) промоторы Pol II содержат ТАТА-бокс и Inr (инициатор) в стандартных позициях (см. рис. 26-9), они сильно различаются и по числу, и по расположению дополнительных последовательностей, необходимых для регуляции транскрипции. В высших эукариотах эти дополнительные регуляторные последовательности называют энхансерами, а в дрожжах — активирующими последовательностями UAS (от англ. upstream activator sequences). Типичный энхансер может находиться на сотни или даже тысячи пар оснований выше точки начала транскрипции, а иногда и ниже, т. е. в самом гене. Энхансер, связанный с соответствующими регуляторными белками, усиливает транскрипцию с соседних промоторов независимо от его ориентации в ДНК. Последовательности UAS в дрожжах действуют аналогичным образом, хотя обычно они располагаются на несколько сотен пар оснований выше точки начала транскрипции. Промотор Pol II может находиться под влиянием до полудюжины (в среднем) регуляторных последовательностей такого рода: часто встречаются и еще более сложные промоторы (см., например, рис. 15-23).
Успешное связывание активного холофермента РНК-полимеразы II на одном из его промоторов обычно обеспечивают дополнительные белки (рис. 28-29) четырех типов: (1) активаторы транскрипции, которые связываются с энхансерами или UAS и способствуют транскрипции: (2) описанные выше белки модификации и ремоделирования хроматина; (3) ко-активаторы; и (4) основные факторы транскрипции (см. рис. 26-10. табл. 26-2). Ко-активаторы действуют не напрямую (т. е. они не связываются с ДНК) и требуются для координации связи между активаторами и комплексом из Pol II и основных факторов транскрипции. Кроме того, во взаимодействие между PHК-полимеразой и активаторами могут вмешиваться разнообразные белки-репрессоры, что приводит к подавлению транскрипции (рис. 28-29. б). Далее мы подробнее рассмотрим белковые комплексы, изображенные на рис. 28-29, и их взаимодействия в процессе активации транскрипции.
Рис. 28-29. Эукариотические промоторы и регуляторные белки. РНК-полимераза II и ассоциированные с ней основные факторы транскрипции образуют преинициаторный комплекс на последовательностях ТАТА-бокса и Inr в соответствующем промоторе; этому процессу способствуют активаторы транскрипции, действующие через медиатор, а — промотор с элементами типичных последовательностей и белковыми комплексами, существующими как в дрожжах, так и в высших эукариотах. С-концевой домен (CTD) Pol II (см. рис. 26-10) — важный участок взаимодействия с медиатором и другими белковыми комплексами. Ферменты модификации гистонов катализируют метилирование и ацетилирование; ферменты ремоделирования изменяют состав и расположение нуклеосом. ДНК-связывающие домены активаторов транскрипции изображены зеленым цветом, активирующие домены — розовым. Взаимодействия, обозначенные голубыми стрелками, обсуждаются в тексте. б — репрессоры транскрипции эукариот действуют посредством нескольких механизмов. Некоторые напрямую связываются с ДНК, вытесняя необходимый для активации белковый комплекс; другие предотвращают активацию, взаимодействуя с различными частями транскрипционных или активаторных комплексов. Возможные участки взаимодействия показаны красными стрелками.
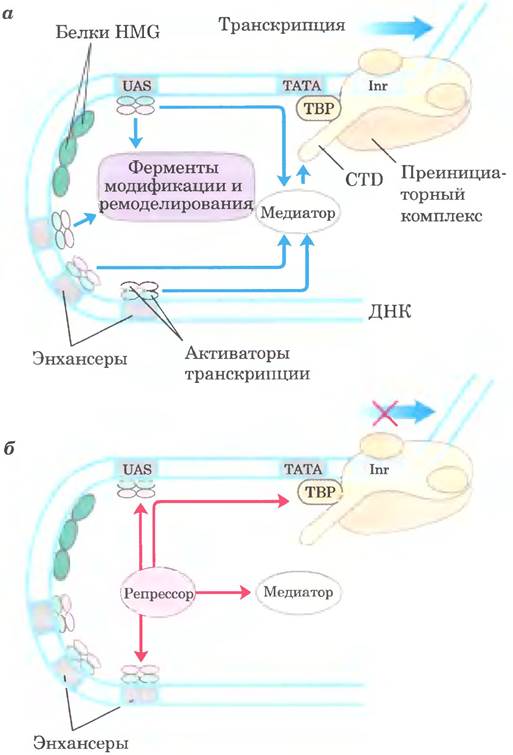
Активаторы транскрипции.
Разные промоторы сильно различаются по своим потребностям в активаторах. Известно несколько активаторов, которые способствуют транскрипции с сотен промоторов, но большинство специфично лишь к некоторым промоторам. Многие активаторы зависят от связывания сигнальных молекул, что позволяет активировать или подавить транскрипцию при изменении условий. Некоторые связывающиеся с активаторами энхансеры находятся далеко от ТАТА-бокса промотора. Как
действуют такие активаторы? В большинстве случаев, по-видимому, расположенная между этими последовательностями ДНК образует петлю, в результате чего различные белковые комплексы приходят в непосредственный контакт. Образованию петли способствуют некоторые негистоновые белки, которые в большом количестве содержатся в хроматине и неспецифическим образом связываются с ДНК. Эта группа белков с высокой электрофоретической подвижностью в полиакриламидном геле (HMG — от англ. high mobility group; рис. 28-29) играет важную роль в ремоделировании хроматина и активации транскрипции.
Ко-активаторные белковые комплексы.
В большинстве случаев для протекания транскрипции требуются дополнительные белковые комплексы. Были проведены биохимические и генетические исследования некоторых важных комплексов регуляторных белков, которые взаимодействуют с Pol II. Эти ко-активаторные комплексы действуют как посредники между активаторами и комплексом Pol II.
Эукариотический ко-активатор состоит из 20-30 или более полипептидов, собранных в белковый комплекс, называемый медиатором (рис. 28-29). Многие из 20 полипептидов сердцевины этого комплекса высококонсервативны у разных видов организмов от грибов до человека. Дополнительный комплекс из четырех субъединиц может взаимодействовать с медиатором и подавлять инициацию транскрипции. Медиатор прочно связывается с С-концевым доменом (CTD) самой крупной субъединицы Pol II. Медиаторный комплекс необходим как для базовой, так и для регулируемой транскрипции с промоторов полимеразы II; он также стимулирует фосфорилирование CTD под действием основного транскрипционного фактора TFIIH. Активаторы транскрипции взаимодействуют с одним или несколькими компонентами медиа- торного комплекса, причем в строго определенных местах, различных для разных активаторов. Ко-активаторные комплексы функционируют в области ТАТА-бокса или поблизости.
Описаны и другие ко-активаторы, способствующие транскрипции одного или нескольких генов. Некоторые функционируют в паре с медиатором, а другие в системах без медиаторов.
ТАТА-связывающий белок.
При сборке пре- инициаторного комплекса (PIC — от англ. preinitiation complex) в области ТАТА-бокса типичного промотора Pol II первым присоединяется ТАТА-связывающий белок (ТВР — от англ. ТАТА-binding protein). В полный комплекс входят основные факторы транскрипции TFIIB, TFIIE, TFIIF, TFIIH, Pol II и, возможно, TFIIA. Однако этого минимального преинициаторного комплекса часто недостаточно для инициации транскрипции, если же промотор скрыт внутри хроматина, преинициаторный комплекс обычно вообще не образуется. Положительную регуляцию, приводящую к началу транскрипции, оказывают активаторы и ко-активаторы.
Согласованный механизм активации транскрипции.
Теперь мы можем воссоздать всю последовательность событий активации транскрипции на типичном промоторе Pol II (рис. 28-30). Порядок связывания некоторых компонентов может различаться; представленная на рис. 28-30 модель отражает общие принципы активации на примере одного типичного варианта сборки. Многие активаторы транскрипции обладают значительным сродством к своим участкам связывания, даже если те находятся в области конденсированного хроматина. Связывание активаторов обычно приводит к активации промотора. Связывание одного активатора может облегчить связывание других, что постепенно приводит к вытеснению нескольких нуклеосом.
Рис. 28-30. Элементы, необходимые для активации транскрипции. Активаторы сначала могут связываться с ДНК. Затем они вовлекают в процесс медиатор и комплексы модификации гистонов/перестройки нуклеосом. Медиатор облегчает связывание ТВР и TFIIB, а также других основных факторов транскрипции, после чего связывается Pol II. Фосфорилирование С-концевого домена (CTD) Pol II приводит к инициации транскрипции (не показано).
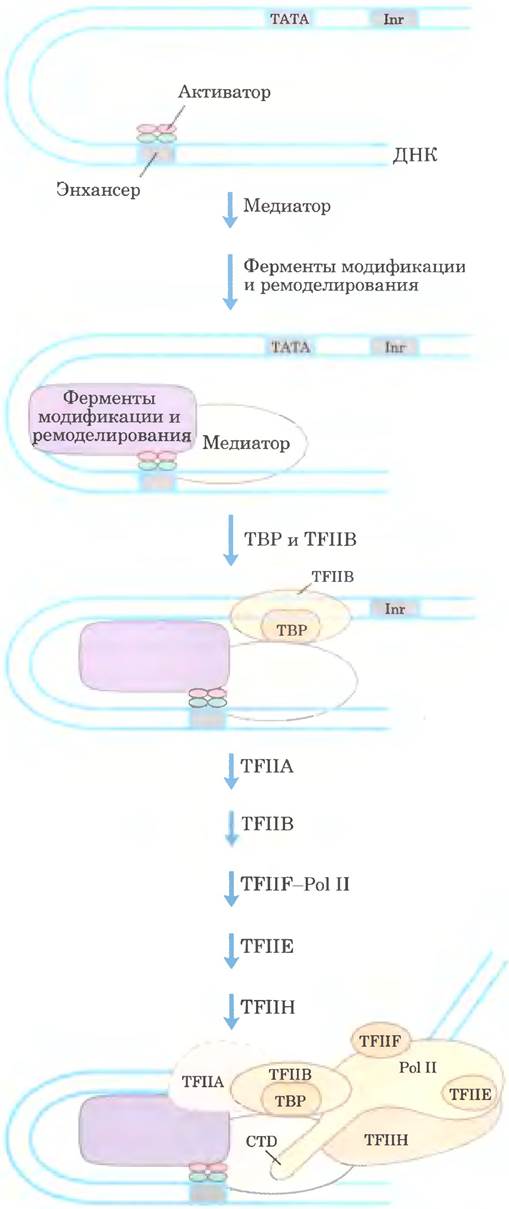
Далее происходит последовательное ремоделирование хроматина, чему способствует взаимодействие активаторов с HAT или с ферментными комплексами, такими как SWI/SNF (или и с теми, и с другими). Таким образом, связанный активатор может вовлекать другие компоненты, необходимые при дальнейшем ремоделировании хроматина для транскрипции специфических генов. Связанные активаторы взаимодействуют с большим медиаторным комплексом. В свою очередь медиатор обеспечивает поверхность для связывания сначала ТВР (TFIID), затем TFIIB и других компонентов преинициаторного комплекса, включая РНК-полимеразу II. Медиатор стабилизирует связывание Pol II и соответствующих транскрипционных факторов и значительно облегчает формирование преинициаторного комплекса. Сложность таких регуляторных схем с многочисленными активаторами транскрипции скорее правило, чем исключение.
Детали процесса могут различаться для разных промоторов, но большинству промоторов для начала транскрипции требуется строго упорядоченная сборка всех компонентов. Процесс сборки не всегда проходит быстро. Для некоторых генов он может длиться минуты, а для некоторых генов высших эукариот — даже сутки.
Обратимость активации транскрипции.
Хотя и редко, некоторые эукариотические регуляторные белки, которые связывают промоторы Pol II, могут действовать как репрессоры, ингибируя образование активных преинициаторных комплексов (рис. 28-29, 6). Некоторые активаторы могут находиться в различных конформациях, что позволяет им быть либо активаторами, либо репрессорами транскрипции. Например, рецепторы некоторых стероидных гормонов (см. ниже) действуют в ядре как активаторы, стимулирующие транскрипцию определенных генов в присутствии определенного стероидного гормона. Когда же гормон отсутствует, рецепторные белки возвращаются в конформацию репрессора, предотвращая образование преинициаторных комплексов. В некоторых случаях в репрессии участвуют гистондеацетилазы и другие белки, которые помогают вернуть хроматин в транскрипционно неактивное состояние. Если медиатор содержит субъединицы с ингибиторной функцией, он тоже способен блокировать инициацию транскрипции. Возможно, этот механизм обеспечивает упорядоченную сборку преинициаторного комплекса (благодаря отсрочке активации транскрипции до тех пор, пока не соберутся все необходимые факторы) или помогает инактивировать промоторы, когда транскрипция не требуется.
Гены метаболизма галактозы в дрожжах подвергаются и положительной, и отрицательной регуляции
Некоторые из описанных выше общих принципов можно проиллюстрировать на примере одной хорошо изученной схемы регуляции в клетках эукариот (рис. 28-31). Ферменты дрожжей, необходимые для доставки и метаболизма галактозы, кодируются генами, разбросанными по нескольким хромосомам (табл. 28-3). Каждый из генов GAL транскрибируется отдельно, поскольку в клетках дрожжей, в отличие от бактерий, нет оперонов. Однако промоторы всех генов GAL похожи и координированно регулируются общим набором белков. Промоторы генов GAL состоят из ТАТА-бокса и последовательности Inr, а также активирующей последовательности UASG, распознаваемой активатором транскрипции Gal4p. Регуляция экспрессии генов галактозой происходит через взаимодействие между Gal4p и двумя другими белками Gal80p и Gal3p (рис. 28-31). Белок Gal80p образует комплекс с Gal4p, что не позволяет Gal4p действовать в качестве активатора промоторов GAL. Если имеется галактоза, она связывается с белком Gal3p, который затем взаимодействует с Gal80p, а Gal4p может действовать в качестве активатора на различных промоторах GAL.
Рис. 28-31. Регуляция транскрипции генов метаболизма галактозы в дрожжах. Галактоза доставляется в клетку и превращается в галактозо-6-фосфат при участии шести ферментов, гены которых расположены на трех хромосомах (см. табл. 28-3). Транскрипция этих генов регулируется совместным действием белков Gal4p, Gal80p и Gal3p, причем Gal4p играет центральную роль активатора транскрипции. Комплекс Gal4p-Gal80p неактивен. Связывание галактозы с Gal3p и взаимодействие Gal3p с Gal80p вызывает изменение конформации Gal80p. Затем комплекс Gal3p-Gal80p выходит из ядра, что позволяет Gal4p связать медиатор и SAGA и участвовать в активации транскрипции.
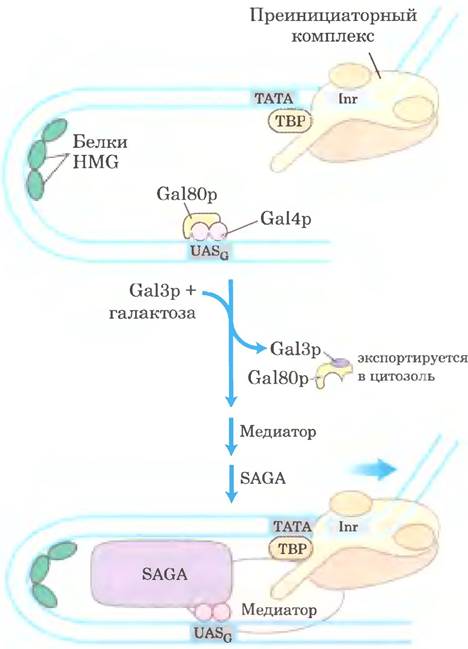
В активации транскрипции генов GAL участвуют и другие белковые комплексы. Это комплекс SAGA для ацетилирования гистонов, комплекс SWI/SNF для ремоделирования нуклеосом и медиаторный комплекс. Когда Gal4p не связан с Gal880p, он привлекает эти дополнительные факторы, необходимые для инициации транскрипции. Оценить сложность белковых взаимодействий в процессе активации транскрипции в клетках эукариот можно, если обратиться к рис. 28-32.
Таблица 28-3. Гены метаболизма галактозы в дрожжах
Размер белка (число остатков) |
Относительный на разных |
уровень источниках |
экспрессии углерода |
|||
Ген |
Функция белка |
Хромосома |
Глюкоза |
Глицерин |
Галактоза |
|
Регулируемые гены GAL1 |
Галактокиназа |
II |
528 |
+++ |
||
GAL2 |
Галактозопермеаза |
XII |
574 |
- |
- |
+++ |
PGM2 |
Фосфоглюкомутаза |
XIII |
569 |
+ |
+ |
++ |
GAL7 |
Галактозо-1 -фосфат- уридилилтрансфераза |
II |
365 |
- |
- |
+++ |
GALIO |
UDР-глюкозо-4-эпимераза |
II |
699 |
- |
- |
+++ |
MEL1 |
α-Галактозидаза |
II |
453 |
- |
+ |
++ |
Регуляторные гены GAL3 |
Индуктор |
IV |
520 |
- |
+ |
++ |
GAL4 |
Активатор транскрипции |
XVI |
881 |
+/- |
+ |
+ |
GAL80 |
Ингибитор транскрипции |
XIII |
435 |
+ |
+ |
++ |
Дрожжи, как и бактерии, предпочитают использовать в качестве источника углерода глюкозу. В присутствии глюкозы происходит репрессия большинства генов GAL, независимо от наличия галактозы. Описанная выше система регуляции GAL эффективно подавляется сложной системой катаболитной репрессии, в которой участвует несколько белков (не показаны на рис. 28-32).
Рис. 28-32. Белковые комплексы, участвующие в активации транскрипции группы родственных эукариотических генов. Система GAL иллюстрирует сложность этого процесса, причем нам известны еще не все беловые комплексы, которые влияют на транскрипцию генов GAL. Обратите внимание, что многие комплексы (SWI/SNF, GCN5-ADA2- ADA3 и медиатор) влияют на транскрипцию множества генов. Сборка комплексов происходит последовательно, в несколько стадий, как показано на рис. 28-30.
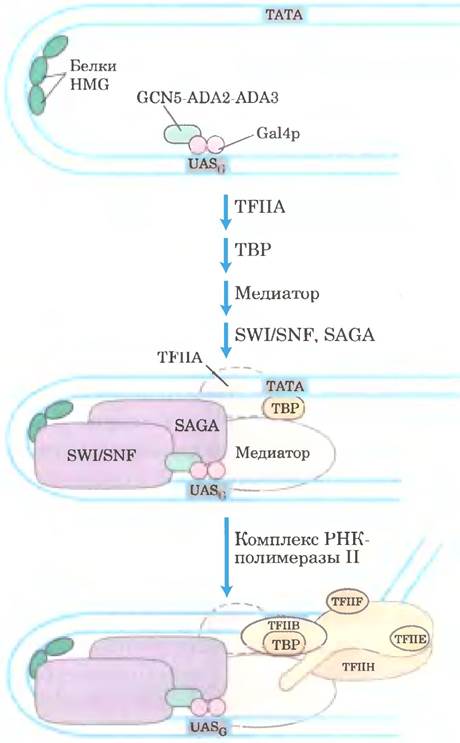
Активаторы транскрипции имеют модульное строение
Типичные активаторы транскрипции содержат хорошо выраженный структурный домен для специфического связывания ДНК и один или несколько дополнительных доменов для активации транскрипции или для взаимодействия с другими регуляторными белками. Взаимодействие двух регуляторных белков часто опосредовано доменами, содержащими лейциновые молнии (рис. 28-14) или мотивы спираль-петля спираль (рис. 28-15). Мы рассмотрим три примера активаторов транскрипции, содержащих разные активирующие домены (рис. 28-33, а): Саl4р, Sр1 и СТF1.
Рис. 28-33. Активаторы транскрипции, а — типичные активаторы, такие как CTF1, Gal4p и Sp1, содержат ДНК- связывающий и активирующий домены. Природа активирующего домена показана символами: «- - -» — кислый; «QQQ» — богатый глутамином; «РРР» — богатый пролином. Эти белки обычно активируют транскрипцию при помощи ко-активаторных комплексов, таких как медиатор. Обратите внимание, что изображенные здесь участки связывания не всегда расположены вместе у одного гена. б — химерный белок, содержащий ДНК-связывающий домен Spl и активирующий домен CTF1; белок активирует транскрипцию при наличии GC-бокса в ДНК.
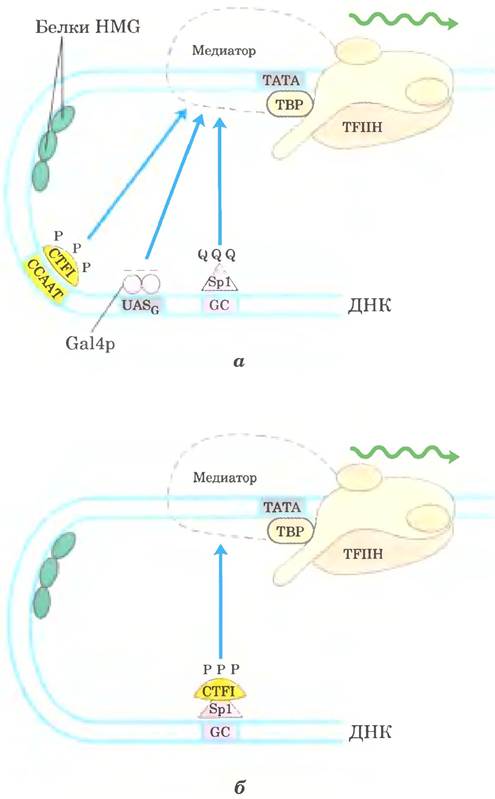
В ДНК-связывающем домене белка Gаl4р вблизи N-конца содержится структура типа цинкового пальца; здесь находятся шесть остатков Сys, координирующие два иона Белок функционирует в виде гомодимера (димеризация обусловлена взаимодействием двух суперспиралей) и связывается с UASG - палиндромной последовательностью ДНК длиной около 17 п. н. Белок Gаl4р имеет отдельный активирующий домен, содержащий множество остатков кислых аминокислот. Вариации последовательности в этом кислом активирующем домене Gаl4р в экспериментальных условиях позволяют предположить, что кислая природа домена принципиально важна для его работы, но сама последовательность может значительно изменяться.
Белок Sр1 (Мr = 80 000) активирует транскрипцию большого числа генов высших эукариот. Его ДНК-связывающий GС-бокс (консенсусная последовательность GGGСGG) обычно располагается в непосредственной близости от ТАТА-бокса. ДНК-связывающий домен белка Sр1 находится рядом с С-концом и содержит три цинковых пальца. Два других домена Sр1 участвуют в активации и замечательны тем, что на 25% состоят из глутамина. Такой богатый глутамином домен есть и во многих других белках-активаторах.
ССААТ-связывающий фактор транскрипции 1 (СТF1) относится к семейству активаторов транскрипции, которые связываются с последовательностью, называемой ССААТ-участком (консенсусная последовательность ТGGN6GССАА, где N — любой нуклеотид). ДНК-связывающий домен СТF1 содержит множество остатков основных аминокислот, а связывающий участок, по-видимому, представляет собой α-спираль. Этот белок не содержит мотивов спираль петля спираль или цинковых пальцев, и механизм его связывания с ДНК пока не ясен. Фактор СТF1 содержит богатый пролином активирующий домен, в котором доля пролиновых остатков превышает 20% общего числа аминокислот.
Домены активации и связывания ДНК в регуляторных белках часто действуют независимо, что было продемонстрировано в экспериментах по замене доменов. С помощью генно-инженерных методов (гл. 9 в т. 1) богатый пролином домен CTF1 был соединен с ДНК-связывающим доменом Sp1, в результате чего получился белок, который подобно нормальному Sp1 связывался с GС-боксом в ДНК и активировал транскрипцию с соседнего промотора (как на рис. 28-33, б). Аналогичным образом ДНК-связывающий домен Gal4p был заменен ДНК-связывающим доменом репрессора LexA из Е. coli (системы SOS-ответа; рис. 28-22). Этот химерный белок не связывался с последовательностью UASG и не активировал гены GAL дрожжей (как сделал бы нормальный белок Gal4p), если только последовательность UASG в ДНК не заменяли участком узнавания LexA.
Экспрессия эукариотических генов может регулироваться внеклеточными и внутриклеточными сигналами
Действие стероидных гормонов (а также тиреоидных и ретиноидных гормонов, действующих сходным образом) — это еще один хорошо изученный пример модуляции действия эукариотических регуляторных белков путем прямого взаимодействия с сигнальными молекулами (см. рис. 12-29 в т. 1). В отличие от гормонов других типов стероидные гормоны не связываются с рецепторами цитоплазматической мембраны. Они могут взаимодействовать с внутриклеточными рецепторами, которые сами являются активаторами транскрипции. Стероидные гормоны (например, эстроген, прогестерон и кортизол) слишком гидрофобные и плохо растворяются в крови, поэтому их доставку от места синтеза к тканям- мишеням осуществляют специфические белки- переносчики. В тканях гормоны проходят через цитоплазматическую мембрану путем простой диффузии и связываются со специфическими рецепторными белками в ядре. Комплекс гормона с рецептором с высокой специфичностью связывается с последовательностями ДНК, называемыми гормон-чувствительными элементами (HRE — от англ. hormone response elements), влияя на экспрессию генов. Связывание гормонов вызывает конформационные изменения рецепторных белков, так что они приобретают способность взаимодействовать с дополнительными факторами транскрипции. Связанный гормон-рецепторный комплекс может либо усиливать, либо подавлять экспрессию соседних генов.
Таблица 28-4. Гормон-чувствительные элементы (НRЕ), с которыми связываются рецепторы стероидных гормонов
Рецептор гормона Связываемая консенсусная последовательность« |
|
Андроген |
GG(А/Т)АСАN2ТGТТСТ |
Глюкокортикоид |
GGТАСАN3GТТСТ |
Ретиноевая кислота |
АGGTСАN5АGGТСА |
Витамин D |
АGGТСАN3АGGТСА |
Тиреоидный гормон |
АGGТСАN3АGGТСА |
RXб |
АGGТСАNАGGТСАNАGGТСАNАGGТСА |
а N - любой нуклеотид.
б Образует димер с рецептором ретиноевой кислоты или рецептором витамина D
Последовательности HRЕ, с которыми связываются комплексы разных стероидных гормонов с рецепторами, похожи по длине и структуре, но имеют разный нуклеотидный состав. Каждому рецептору соответствует консенсусная последовательность HRЕ (табл. 28-4), с которой гормон-рецепторный комплекс связывается более эффективно. Каждая такая последовательность состоит из двух шестинуклеотидных фрагментов, которые либо соприкасаются, либо разделены тремя нуклеотидами и расположены в виде тандема или палиндрома. Рецепторы содержат высококонсервативный ДНК-связывающий домен с двумя цинковыми пальцами (рис. 28-34). Гормон-рецепторный комплекс связывается с ДHК в виде димера, при этом домены с цинковыми пальцами каждого мономера узнают по одному шестинуклеотидному фрагменту. Способность конкретного гормона изменять экспрессию специфического гена, действуя через гормон-рецепторный комплекс, зависит от нуклеотидной последовательности HRE, ее расположения относительно гена и количества последовательностей HRE, связанных с этим геном.
Рис. 28-34. Типичные рецепторы стероидных гормонов. Эти рецепторные белки содержат участок связывания с гормоном, ДНК-связывающий домен и участок, активирующий транскрипцию регулируемого гена. Высококонсервативный ДНК-связывающий домен содержит два цинковых пальца. Здесь показана последовательность рецептора эстрогена, но остатки, выделенные жирным шрифтом, являются общими для всех рецепторов стероидных гормонов.
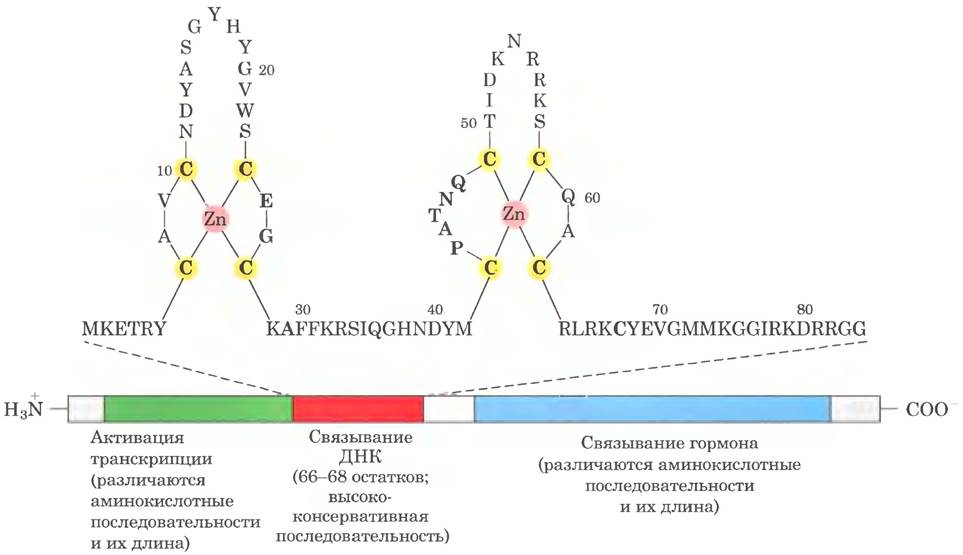
В отличие от ДНК-связывающего домена лиганд-связывающий участок рецепторного белка (всегда расположенный на С-конце белка) весьма специфичен к конкретному рецептору. Лиганд-связывающий участок глюкокортикоидного рецептора имеет лишь 30% сходства с рецептором эстрогена и 17% — с рецептором тиреоидного гормона. Размеры лиганд-связывающих участков рецепторов сильно варьируют: в рецепторе витамина D это всего 25 аминокислотных остатков, тогда как в рецепторе минералокортикоидов — 630 остатков. Мутации, в результате которых происходит замена только одного аминокислотного остатка в этом участке, могут привести к исчезновению реакции на специфический гормон. Мутации такого типа встречаются у людей, нечувствительных к кортизолу, тестостерону, витамину D или тироксину.
Некоторые рецепторы гормонов, включая человеческий рецептор прогестерона, активируют транскрипцию при помощи необычного ко- активатора — РНК-активатора стероидного рецептора (steroid receptor RNA activator, SRA). Эта последовательность РНК длиной -700 нуклеотидов действует как часть рибонуклеопротеинового комплекса, но для ко-активации транскрипции нужен именно его РНК-компонент. Подробности взаимодействия SRA с другими компонентами систем регуляции данных генов еще предстоит выяснить.
Регуляция может осуществляться путем фосфорилирования ядерных факторов транскрипции
В гл. 12 (т. 1) мы рассказывали о том, что влияние инсулина на экспрессию генов происходит через каскад реакций, в конечном итоге приводящих к активации протеинкиназы в ядре, которая фосфорилирует специфические ДНК-связывающие белки и тем самым изменяет их способность действовать в качестве факторов транскрипции (см. рис. 12-6). По такому механизму действуют многие нестероидные гормоны. Например, β-адренергический путь, ведущий к повышению уровня цитоплазматического сАМР, выполняющего функцию вторичного мессенджера и у эукариот, и у бактерий (см. рис. 12-4, в т. 1 и рис. 28-18), также влияет на транскрипцию некоторых генов, расположенных рядом со специфической последовательностью ДНК, называемой сАМР-чувствительным элементом (CRE - от англ. сАМР response element). Каталитическая субъединица протеинкиназы А, которая высвобождается при повышении концентрации сАМР (см, рис. 12-6), проникает в ядро и фосфорилирует ядерный белок CREB (CRE-связывающий белок). Фосфорилированный CREB связывается с элементами CRE рядом с определенными генами и действует как фактор транскрипции, запуская экспрессию этих генов.
Трансляция многих эукариотических мРНК подавляется
В клетках эукариот регуляция экспрессии на уровне трансляции играет гораздо более важную роль, чем в клетках бактерий, и происходит в целом ряде ситуаций. В отличие от бактерий, в которых транскрипция и трансляция непосредственно связаны, транскрипты, образующиеся в эукариотических ядрах, до начала трансляции должны пройти процессинг и попасть в цитоплазму. Все это может значительно затормозить синтез белка. Когда клетке требуется быстро увеличить продукцию белка, находящаяся в цитоплазме мРНК, трансляция которой подавлена, может быть быстро активирована для трансляции. Регуляция на уровне трансляции особенно важна для экспрессии некоторых очень протяженных эукариотических генов (некоторые гены состоят из миллионов пар оснований), транскрипция и процессинг мРНК которых могут длиться много часов. Некоторые гены регулируются как на стадии транскрипции, так и на стадии трансляции, причем последний механизм служит для тонкой настройки концентрации клеточных белков. В некоторых безъядерных клетках, таких как ретикулоциты (незрелые эритроциты), контроль на уровне транскрипции
невозможен, поэтому решающую роль играет контроль трансляции уже синтезированной мРНК. Как будет рассказано далее, контроль трансляции играет важную роль в процессе развития многоклеточного организма, когда путем регуляции трансляции ранее синтезированной мРНК создается локальный градиент белка.
У эукариот реализуется, как минимум, четыре основных механизма регуляции трансляции.
1. Факторы инициации трансляции подвергаются фосфорилированию протеинкиназами, Фосфорилированные формы обычно менее активны и вызывают общее замедление трансляционных процессов в клетке.
2. Некоторые белки связываются непосредственно с мРНК, многие — со специфическими участками в 3'-нетранслируемой области (3'UТR) и действуют как репрессоры трансляции. Связанные в этом участке белки взаимодействуют с другими факторами инициации трансляции, связанными с мРНК или с 40S-субъединицей рибосомы, и предотвращают инициацию трансляции (рис. 28-35, ср. с рис. 27-27).
Рис. 28-35. Регуляция трансляции эукариотической мРНК. Один из самых важных механизмов регуляции трансляции в клетках эукариот заключается в связывании репрессоров трансляции (РНК-связывающих белков) со специфическими участками в 3'-нетранслируемой области (3'-UTR) мРНК. Эти белки взаимодействуют с эукариотическими факторами инициации или с рибосомами (см. рис. 27-27), что предотвращает или замедляет трансляцию.
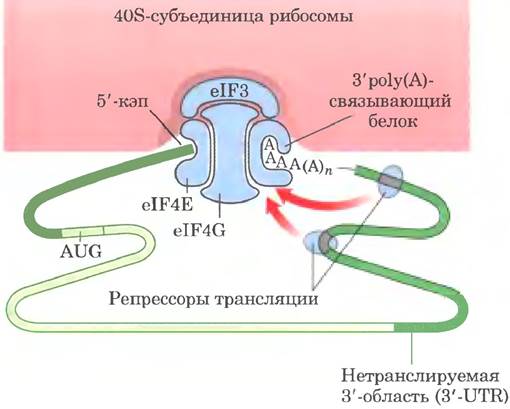
3. Некоторые белки, имеющиеся у всех эукариот — от дрожжей до млекопитающих, нарушают взаимодействия между eIF4E и eIF4G (см. рис. 27-27). Соответствующие белки млекопитающих называют 4Е-ВР (белки, связывающие eIF4E). Когда клетка растет медленно, эти белки ограничивают трансляцию, связываясь с участком на eIF-4E, который в норме взаимодействует с eIF4G. Когда клеточный рост возобновляется или ускоряется в ответ на сигнал факторов роста или на другие стимулы, связывающие белки инактивируются фосфорилированием под действием протеинкиназ.
4. Регуляция экспрессии генов, опосредованная РНК, которую мы обсудим чуть позже, обычно заключается в подавлении трансляции.
Разнообразие механизмов регуляции трансляции обеспечивает гибкость при осуществлении подавления трансляции — замедление трансляции может касаться лишь нескольких мРНК или же охватить глобальную регуляцию всего процесса трансляции в клетке.
Хорошо изучен процесс регуляции трансляции в ретикулоцитах. В этих клетках в регуляции трансляции участвует фактор инициации eIF2, который связывается с инициаторной тРНК и подводит ее к рибосоме. Когда Met-тРНК связывается в P-сайте, с eIF2 связывается фактор eIF2B и высвобождает его за счет связывания и гидролиза GTP. В ходе созревания ретикулоцитов ядро клеток разрушается, и все пространство внутри плазматической мембраны оказывается заполненным гемоглобином. Матричная РНК, накопленная в цитоплазме до исчезновения ядра, позволяет поддерживать запасы гемоглобина. Когда ретику- лоциты испытывают дефицит железа или гема, происходит остановка трансляции мРНК глобинов. Активируется протеинкиназа HCR (от англ. hemin-conrolled repressor — репрессор, контролируемый гемином), которая фосфорилирует eIF2. Фосфорилированный eIF2 образует стабильный комплекс с eIF2B, что делает невозможным участие eIF2 в трансляции. Так ретикулоциты координируют синтез глобина с наличием гема.
При изучении развития многоклеточных организмов было выявлено множество других примеров регуляции трансляции, что подробнее обсуждается ниже.
Посттранскрипционный сайленсинг гена опосредован РНК
В клетках высших эукариот, в том числе нематод, плодовых мушек, растений и млекопитающих, выключение (сайленсинг) многих генов опосредуют малые молекулы РНК, названные микро-РНК. Эти РНК функционируют путем взаимодействия с молекулами мРHК (часто в области 3’UTR), приводя либо к деградации мРНК, либо к подавлению трансляции. В любом случае мРНК, а значит и ген, с которого она образована, отключается («молчит»). Этот механизм регуляции генов контролирует порядок событий в ходе развития некоторых организмов. Такая регуляция также используется для защиты от заражения РНК-вирусами (что особенно важно для растений, у которых нет иммунной системы) и для контроля активности транспозонов. Кроме того, малые молекулы РНК могут играть важную (но пока еще неопределенную) роль в образовании гетерохроматина.
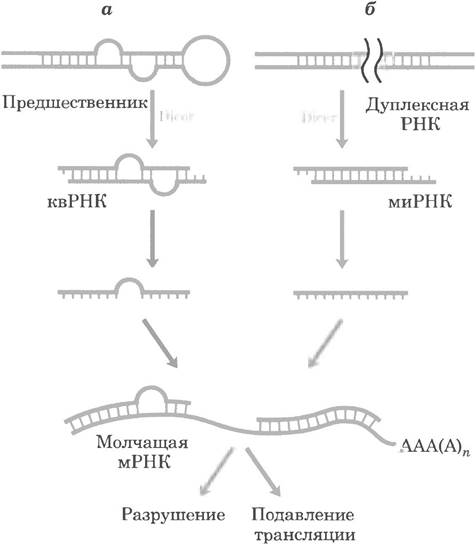
Многие микро-РНК существуют только на определенных этапах развития, и иногда их относят к малым временным РНК (мвРНК). В высших эукариотах идентифицированы тысячи различных микро-РНК, которые могут влить на регуляцию трети всех генов млекопитающих. Они транскрибируются в виде РНК-предшественников длиной около 70 нуклеотидов с внутренними комплементарными последовательностями, которые образуют структуры типа шпильки (см. рис. 26-28). Эти предшественники расщепляются эндонуклеазами, такими как Drosha и Dicer, с образованием коротких дуплексов длиной 20-25 нуклеотидов. Одна цепь процессированной микро-РНК связывается с мРНК-мишеныо (или с РНК вируса или транспозона), что приводит к подавлению трансляции или к деградации РНК (рис. 28-36). Некоторые микро-РНК связываются с мРНК одного вида, управляя экспрессией единственного гена. Другие взаимодействуют со многими мРНК, являясь ключевым элементом регулона и координируя экспрессию множества генов.
Этот механизм регуляции генов имеет интересную и очень полезную практическую сторону. Если ввести в организм PHК-дуплекс, последовательность которого соответствует фактически любой мРНК, эндонуклеаза Dicer расщепляет эти дуплексы на короткие фрагменты, называемые малыми интерферирующими РНК
(миРНК). Они связываются с мРНК и вызывают их сайленсинг (рис. 28-36, б). Этот процесс называют интерференцией РНК. В растениях фактически любой ген может быть эффективно выключен таким способом. Нематоды способны поглощать функциональные РНК целиком, и поэтому простое добавление дуплексной РНК в их корм позволяет очень эффективно отключать гены-мишени. Такой метод быстро стал важным инструментом в изучении функций генов, так как он позволяет отключить ген без создания мутантного организма. Этот подход может оказаться полезным и при лечении человека. Искусственно синтезированные миРНК позволяют блокировать распространение ВИЧ и полиовирусной инфекции в культурах клеток человека примерно в течение недели Быстрый прогресс в этой области позволяет надеяться на внедрение методов интерференции РНК в медицину в будущем.
Рис. 28-36. Сайленсинг генов в результате интерференции РНК. а — малые временные РНК (мвРНК) образуются под действием эндонуклеазы Dicer из более длинных предшественников, которые содержат дуплексные участки. Затем эти мвРНК связываются с мРНК, приводя к разрушению мРНК или подавлению трансляции, б — двухцепочечные РНК можно искусственно сконструировать и ввести в клетку. Dicer превращает дуплексные РНК в малые интерферирующие РНК (миРНК), которые взаимодействуют с мРНК-мишенью. В этом случае происходит либо расщепление мРНК, либо ингибирование ее трансляции.
У эукариот реализуется несколько вариантов РНК-опосредованной регуляции экспрессии генов
У эукариот к РНК со специфическими функциями относят описанные выше микроРНК, мяРНК, участвующие в сплайсинге РНК (см. рис. 26-16), а также мяРНК, участвующие в модификации рРНК (см. рис. 26-26). Все не кодирующие белок РНК, включая рРНК и тРНК, имеют общее название — некодирующие РНК (нкРНК). Вероятно, в геномах млекопитающих содержится больше некодирующих, чем кодирующих РНК (см. доп. 26-4). Неудивительно, что до сих пор появляются новые функциональные классы некодирующих РНК.
Многие из недавно обнаруженных некодирующих РНК взаимодействуют не с РНК, а с белками, и изменяют свойства связанных белков. Один из примеров — белок SRA, который выступает в роли ко-активатора генов, реагирующих на действие стероидных гормонов; он влияет на активацию транскрипции. Еще один пример — белки теплового шока. Фактор теплового шока-1 (HSF-1) — это белок-активатор, который в обычных условиях существует в виде мономера, связанного с шапероном Hsp90. При стрессе HSF-1 высвобождается из комплекса с Hsp90 и тримеризуется. Тример HSF-1 связывается с ДНК и активирует транскрипцию генов, продукты которых необходимы для реакции на стресс. Некодирующая РНК фактора HSR1 (от англ. heat shock RNA 1; - 600 нуклеотидов) стимулирует образование тримеров HSF-1 и связывание ДНК. Фактор HSR1 действует не в одиночку, а в комплексе с фактором элонгации трансляции eEF1A.
Вспомогательные РНК влияют на ход транскрипции многими способами. Наряду с участием в сплайсинге (см. рис. 26-17) мяРНК U1 прямо связывается с фактором транскрипции TFIIH. Функция мяРНК U1 в этом комплексе не совсем понятна; возможно, она регулирует активность TFIIH и/или влияет на сопряжение процессов транскрипции и сплайсинга. Еще одна РНК с неопределенной функцией, названная 7SK, состоит из 331 нуклеотида; она содержится в большом количестве в клетках млекопитающих, связывается с фактором элонгации транскрипции p-TEFb (см. табл. 26-2) и подавляет удлинение транскрипта. Другая нкРНК, В2 (~178 нуклеотидов) напрямую связывается с Pol II при тепловом шоке и подавляет транскрипцию. Связанная с В2 полимераза II образует стабильный преинициаторный комплекс, но транскрипция при этом блокирована. Таким способом при тепловом шоке РНК В2 подавляет транскрипцию многих генов, однако существует неизвестный пока механизм, позволяющий чувствительным к HSF-1 генам экспрессироваться в присутствии В2.
Представления о роли нкРНК в экспрессии генов и во многих других клеточных процессах быстро развиваются. Одновременно с этим интересы биохимиков, изучающих регуляцию генов, все больше смещаются от белков в сторону РНК.
Развитие контролируется каскадами регуляторных белков
По сложности схем регуляции генов процесс превращения зиготы в многоклеточное животное или растение не имеет себе равных. В ходе развития происходят изменения морфологии и белкового состава, которые зависят от точной координации изменений в экспрессии генома. В ранний период развития экспрессируется больше генов, чем в любой другой период жизненного цикла. Например, ооцит морского ежа содержит около 18 500 различных мРНК, а типичная дифференцированная ткань — около 6000. Матричные РНК ооцита дают начало каскаду событий, которые регулируют экспрессию многих генов во времени и в пространстве.
Некоторых животных особенно удобно использовать в качестве модельных систем для изучения развития, поскольку их легко содержать в лабораторных условиях, и они достаточно быстро размножаются. К таким животным относятся нематоды, плодовые мушки, рыбки-данио, мыши и растения Arabidopsis. В этом разделе мы сосредоточим внимание на развитии плодовых мушек. Мы достаточно далеко продвинулись в понимании молекулярных событий, происходящих в ходе развития Drosophila melanogaster, и имеющуюся информацию можно использовать для иллюстрации общих схем и принципов.
Развитие дрозофилы идет с полным метаморфозом на пути от эмбриона к взрослой особи (рис. 28-37). Самые важные характеристики эмбриона — это полярность (передний и задний конец животного легко различимы, также как спинная и брюшная стороны) и метамерия (тело эмбриона составлено из наборов повторяющихся сегментов с характерными признаками). В процессе развития эти сегменты превращаются в голову, грудь и брюшко. Каждый грудной сегмент взрослого насекомого содержит разный набор придатков. Реализация этого сложного плана развития находится под генетическим контролем. Уже известно множество генов, регулирующих этот процесс и удивительным образом влияющих на формирование тела животного.
Рис. 28-37. Жизненный цикл плодовой мушки Drosophila melanogaster. Развитие дрозофилы протекает с полным метаморфозом, т. е. взрослое насекомое кардинальным образом отличается от промежуточных форм; такая трансформация требует множества изменений в ходе развития. К поздней эмбриональной стадии уже сформированы сегменты, содержащие специализированные структуры, из которых впоследствии развиваются различные придатки и другие структуры взрослой мухи.
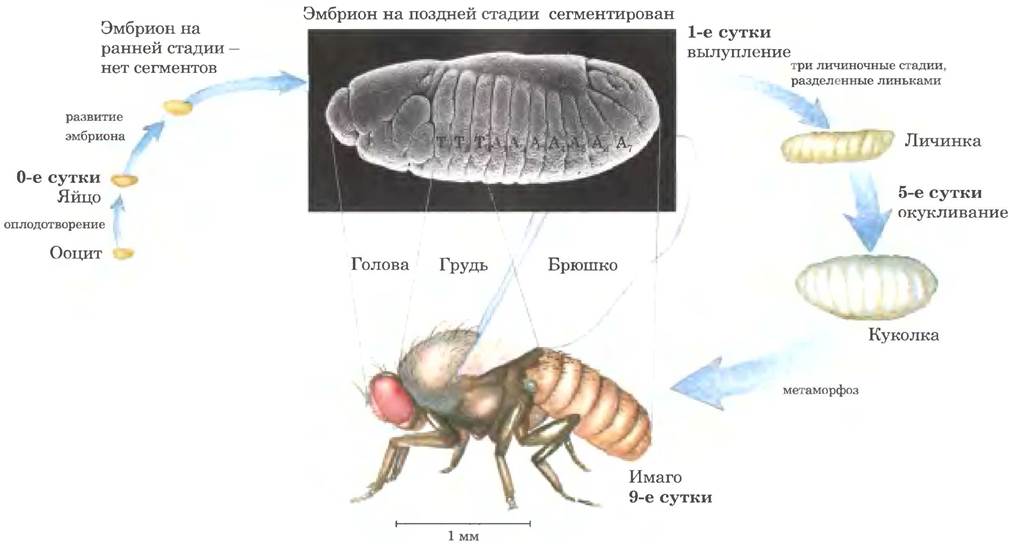
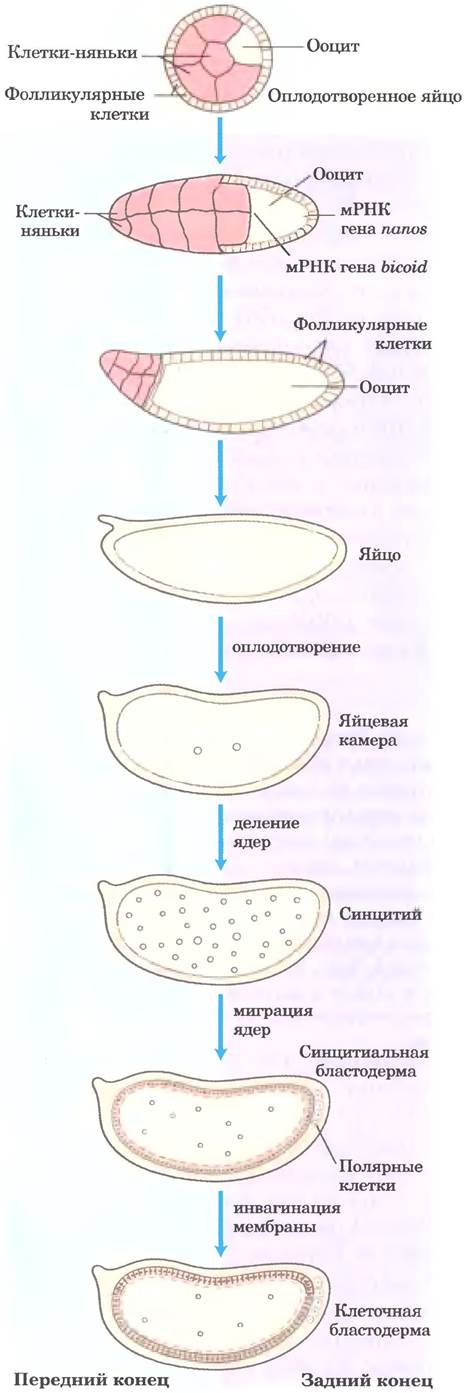
Яйцеклетка дрозофилы и 15 клеток-нянек окружены слоем фолликулярных клеток (рис. 28-38). По мере развития яйцеклетки (до оплодотворения) мРНК и белки, происходящие из клеток-нянек и фолликулярных клеток, откладываются в яйцеклетке, и некоторые из них играют определяющую роль в развитии. В определенное время самка откладывает оплодотворенное яйцо, которое делится, и дочерние клетки продолжают синхронно делиться каждые 6 10 минут. Вокруг образующихся ядер нет плазматической мембраны, они распределяются внутри цитоплазмы яйца, формируя синцитий. Между восьмым и одиннадцатым делением ядра мигрируют к периферии яйца, образуя монослой, окружающий общую насыщенную желтком цитоплазму: это синцитиальная бластодерма. После еще нескольких дополнительных делений мембрана образует выпячивания, которые окружают ядра, в результате чего возникает слой клеток, формирующих клеточную бластодерму. На этой стадии митотические циклы в различных клетках перестают синхронизироваться. Дальнейшее развитие каждой клетки определяется мРНК и белками, запасенными клетками- няньками и фолликулярными клетками на самой ранней стадии.
Белки, которые путем изменения локальной концентрации или активности заставляют окружающую ткань принимать определенную форму или структуру, иногда называют морфогенами; они являются продуктами генов, регулирующих строение тела. Как установили Кристиана Нюсляйн- Фольхард, Эдвард Б. Льюис и Эрик Ф. Вишаус, три главных класса генов, регулирующих строение тела, — материнские гены, гены сегментации и гомеотические гены — действуют на последовательных стадиях развития, точно определяя основные структуры тела эмбриона дрозофилы. Материнские гены экспрессируются в неоплодотворенном яйце, и образующиеся материнские мРНК остаются спящими до оплодотворения. Они кодируют большинство белков, необходимых на самых ранних стадиях развития — до образования клеточной бластодермы. Некоторые белки, кодируемые материнскими мРНК, управляют пространственной организацией развивающегося зародыша на ранних стадиях, устанавливая его полярность. Гены сегментации, транскрибируемые после оплодотворения, задают точное число сегментов тела. На последовательных стадиях действуют, как минимум, три подкласса генов сегментации: гены пробела (gap-гены) делят развивающийся зародыш на несколько обширных областей; гены парного
правила (pair-rule) вместе с генами полярности сегментов определяют 14 полос, которые станут 14 сегментами тела нормального эмбриона. Гомеотические гены экспрессируются еще позже; они определяют, какие органы и придатки разовьются в каждом сегменте тела.

Рис. 28-38. Ранние стадии развития дрозофилы. В процессе развития яйца материнские мРНК (включая транскрипты генов bicoid и nanos, которые обсуждаются в тексте) и белки синтезируются клетками-няньками и фолликулярными клетками и откладываются в развивающемся ооците (неоплодотворенной яйцеклетке). После оплодотворения два ядра оплодотворенного яйца синхронно делятся внутри общей цитоплазмы (синцитий), а затем мигрируют к периферии. Складки мембраны окружают ядра, формируя монослой клеток на периферии (стадия клеточной бластодермы). Во время первых делений ядер несколько ядер на заднем конце становятся полярными клетками, которые позднее станут клетками зародышевой линии.
Множество регуляторных генов из этих трех классов отвечает за появление взрослой мушки с головой, грудью и брюшком, с надлежащим числом сегментов и с нужными придатками в каждом сегменте. Хотя полный эмбриогенез занимает около суток, все эти гены активируются в течение первых четырех часов развития. Некоторые мРНК и белки появляются лишь на несколько минут в определенных фазах этого периода развития. Некоторые гены кодируют транскрипционные факторы, которые влияют на экспрессию других генов, — возникает каскад генетических событий. Регуляция осуществляется и на уровне трансляции: многие регуляторные гены кодируют репрессоры трансляции, большинство из которых связываются с нетранслируемой областью на 3’-конце мРНК (рис. 28-35). Так как многие мРНК накапливаются в яйце задолго до того, как потребуется их трансляция, репрессия трансляции оказывается очень важным механизмом регуляции развития
Материнские гены.
Некоторые материнские гены экспрессируются внутри клеток-нянек и фолликулярных клеток, другие — в самом яйце В неоплодотворенном яйце дрозофилы продукты материнских генов формируют две оси тела — переднезаднюю и спинно-брюшную; тем самым определяется, какие области радиально симметричного яйца образуют голову и брюшко, а также в верх и низ тела взрослой мухи. Ключевым событием на самых ранних стадиях развития является установление градиентов мРНК и белков вдоль осей тела. Некоторые материнские мРНК кодируют белковые продукты, которые диффундируют через цитоплазму и распределяются в яйце несимметричным образом. В результате клетки клеточной бластодермы наследуют разные количества этих белков, что направляет клетки по разным путям развития. Среди продуктов материнских мРНК есть активаторы и репрессоры транскрипции, а также репрессоры трансляции; все они регулируют экспрессию других генов, регулирующих строение тела. Возникающие специфические схемы и последовательности экспрессии генов различаются в разных линиях клеток, что в конечном итоге определяет развитие каждой структуры взрослой особи.
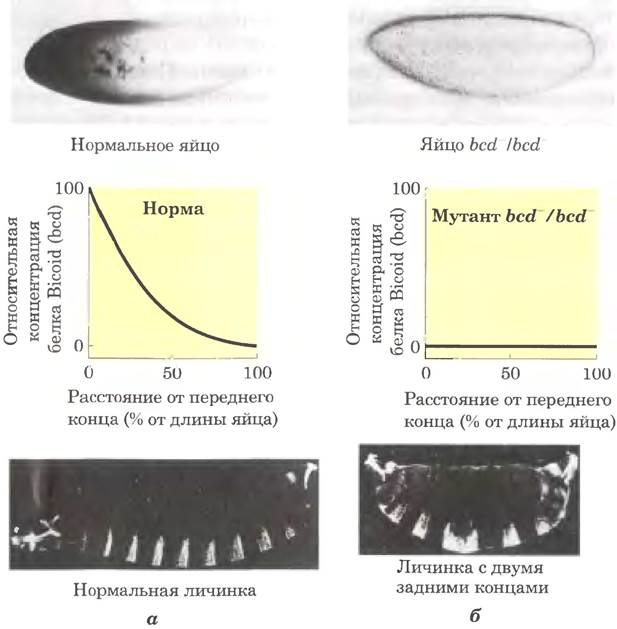
Формирование переднезадней оси зародыша дрозофилы в значительной степени определяется продуктами генов bicoid и nanos. Продукт гена bicoid - главный морфоген переднего конца тела, а продукт гена nanos — главный морфоген заднего конца. Матричная РНК гена bicoid синтезируется клетками-няньками и откладывается в неоплодотворенном яйце вблизи переднего конца. Нюсляйн-Фольхард обнаружила, что эта мРНК транслируется вскоре после оплодотворения, и белок Bicoid распределяется в клетке, создавая к седьмому клеточному делению градиент концентрации, расходящийся радиально от переднего полюса (рис. 28-39, а). Белок Bicoid - фактор транскрипции, активирующий экспрессию ряда генов сегментации; этот белок содержит гомеодомен (рис, 28-13). Кроме того, Bicoid является репрессором трансляции и инактивирует определенные мРНК. Количество белка Bicoid в различных частях зародыша влияет на последующую экспрессию других генов, причем транскрипция генов активируется или их трансляция подавляется, только если концентрация белка Bicoid превышает определенный порог. Форма градиента концентрации белка Bicoid оказывает очень сильное влияние на строение тела мухи. Отсутствие белка Bicoid приводит к развитию эмбриона с двумя брюшками, но без головы и грудного отдела (рис. 28-39. б). Однако не имеющий белка Bicoid эмбрион развивается нормально, если в соответствующий конец яйца ввести достаточное количество мРНК bicoid. Ген nanos играет аналогичную роль, но его мРНК сосредоточена в заднем конце яйца и максимум переднезаднего градиента белка достигается на заднем полюсе. Белок Nanos подавляет трансляцию.
Рис. 28-39. Распределение продукта материнского гена в яйце дрозофилы, а — микрофотография яйца, окрашенного с помощью антител, демонстрирует распределение продукта гена bicoid (bed). Графики отражают интенсивность окраски. Такое распределение необходимо для нормального развития структур передней части животного. б — если у матери ген bed не экспрессируется (мутант bсd-/bсd-). мРНК bicoid не накапливается в яйце, и в результате формируется нежизнеспособный эмбрион с двумя задними частями.
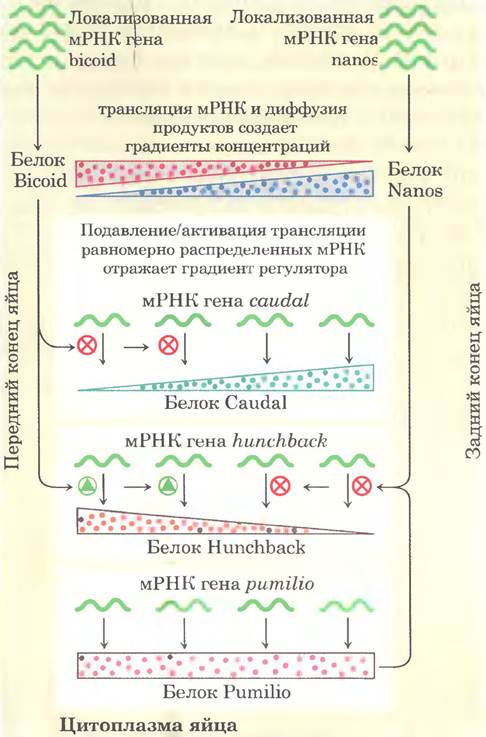
Если взглянуть на действие материнских генов в целом, можно обнаружить общую схему развития. Кроме асимметрично расположенных мРНК bicoid и nanos, в цитоплазме равномерным образом распределены другие материнские мРНК. Три из этих мРНК кодируют белки Pumilio, Hunchback и Caudal, находящиеся под влиянием nanos и bicoid (рис. 28-40). Белки Caudal и Pumilio участвуют в развитии заднего конца мушки: Caudal - активатор транскрипции с гомеодоменом, Pumilio — репрессор трансляции. Белок Hunchback играет важную роль в развитии переднего конца и регулирует транскрипцию многих генов: в некоторых случаях — положительно, в других — отрицательно. Белок Bicoid подавляет трансляцию гена caudal на переднем конце и активирует транскрипцию гена hunchback в клеточной бластодерме. Поскольку экспрессия hunchback происходит и с материнских мРНК, и с генов развивающегося яйца, его можно рассматривать и как материнский ген, и как ген сегментации. В результате активности Bicoid концентрация Hunchback на переднем конце яйца увеличивается. Белки Nanos и Pumilio являются репрессорами трансляции гена hunchback, подавляя синтез этого белка на заднем конце яйца. Белок Pumilio не функционирует в отсутствие белка Nanos, и градиент экспрессии nanos ограничивает активность обоих белков на заднем конце. Репрессия трансляции гена hunchback приводит к деградации мРНК hunchback в задней части. Однако отсутствие на заднем конце белка Bicoid приводит к экспрессии гена caudal. В результате белки Hunchback и Caudal распределены в яйце асимметричным образом.
Рис. 28-40. Схема формирования переднезадней оси в яйце дрозофилы. Матричные РНК bicoid и nanos откладываются вблизи переднего и заднего концов яйца соответственно; мРНК caudal, hunchback и pumilio равномерно распределены в цитоплазме. Градиенты белков Bicoid (Bed) и Nanos приводят к накоплению белка Hunchback на переднем конце, а белка Caudal на заднем конце яйца. Белок Pumilio функционирует только на заднем конце яйца поскольку для его активности в качестве репрессора трансляции гена hunchback требуется белок Nanos.
Гены сегментации.
На последовательных стадиях эмбрионального развития дрозофилы активируются три подкласса генов сегментации: гены пробела (gap), парного правила (pair-rule) и полярности сегмента. Обычно экспрессия генов gap регулируется продуктами одного или нескольких материнских генов. Некоторые гены gap кодируют транскрипционные факторы, которые влияют на экспрессию других генов сегментации или (позднее) гомеотических генов.
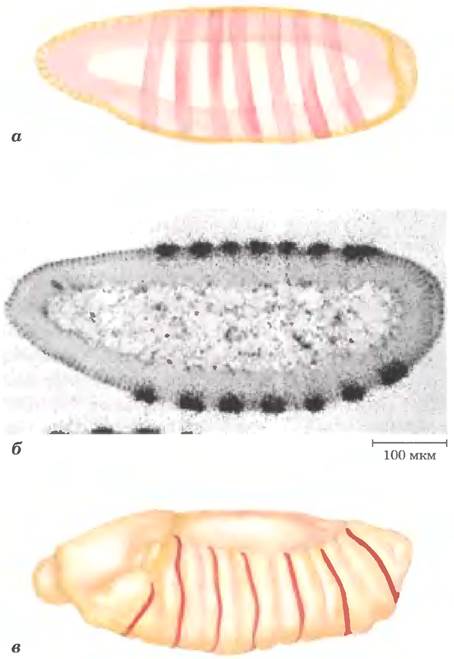
Примером хорошо охарактеризованного гена сегментации является ген fushi tarazu (ftz) из подкласса генов pair-rule. При делении гена ftz у эмбриона появляется только семь сегментов вместо положенных 14, причем каждый сегмент вдвое шире нормы. Белок Fushi tarazu (Ftz) — активатор транскрипции, обладающий гомеодоменом. Матричная РНК и белки, синтезированные на основе нормального гена ftz. образуют удивительный рисунок в виде семи полос, опоясывающих эмбрион в задних двух третях его тела (рис. 28-41). Полосы указывают расположение формирующихся позже сегментов; если функция ftz нарушена, сегменты не образуются. Белок Ftz и еще несколько подобных регуляторных белков прямо или опосредованно регулируют экспрессию множества генов в каскаде развития.
Рис. 28-41. Распределение продукта гена fushi tarazu в раннем эмбрионе дрозофилы, а — в нормальном эмбрионе продукт гена можно обнаружить в семи полосах, охватывающих тело эмбриона (показаны схематично); б — на авторадиограмме продольного среза эмбриона эти полосы выглядят как темные пятна (радиоактивная метка); в — полосы определяют переднюю границу сегментов в позднем эмбрионе (обозначены красным цветом).
Гомеотические гены.
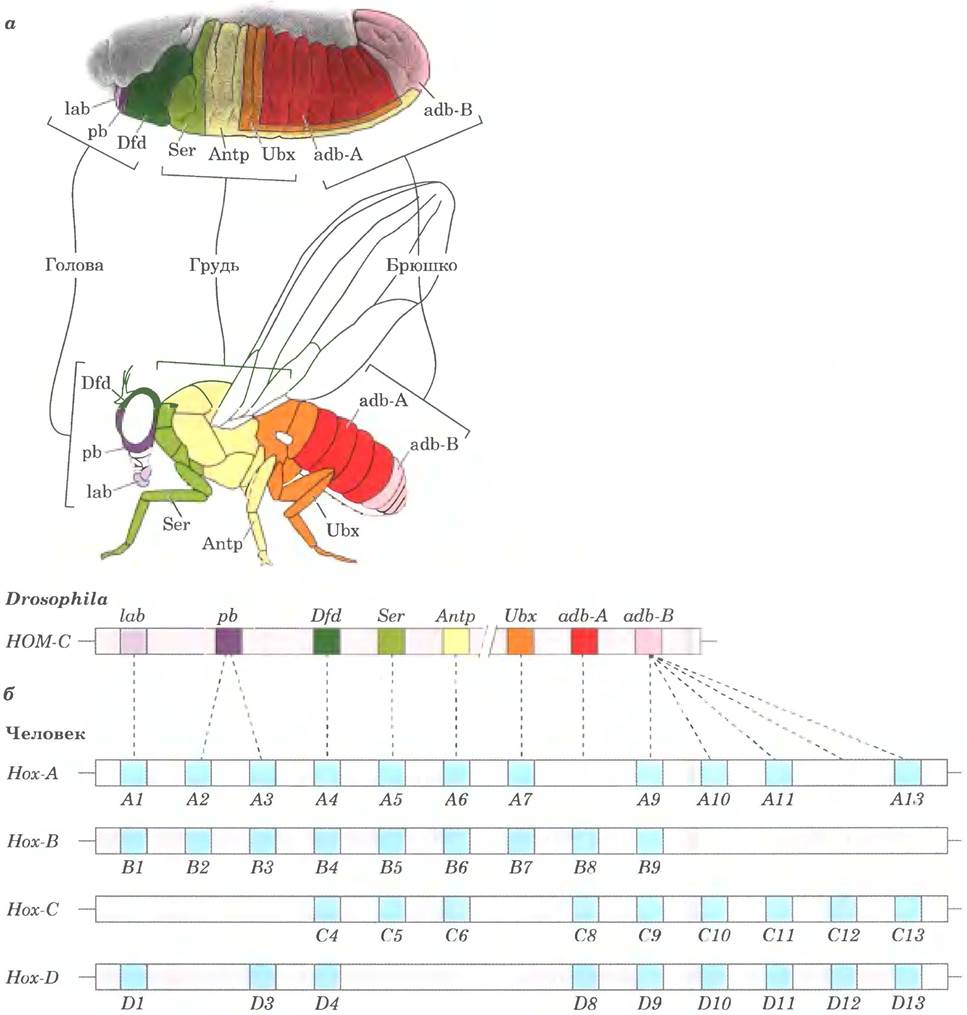
Группа из 8-11 гомеотических генов связан с развитием конкретных структур в определенных отделах тела. Эти гены теперь чаще называют Нох-генами; название происходит от слова «homeobox», обозначающего консервативную последовательность гена, кодирующую гомеодомен и присутствующую во всех этих генах. Однако следует учесть, что гомеодомен имеют не только белки, связанные с развитием структур организма (к примеру, описанный выше продукт гена bicoid тоже содержит гомеодомен); «Нох» подразумевает скорее функциональную, чем структурную классификацию. Гены Нох организованы в кластеры. У дрозофил есть один такой кластер, у млекопитающих их четыре (рис. 28-42). Гены в этих кластерах — от нематод до человека — удивительно похожи. У дрозофил каждый из генов Нох экспрессируется в определенном отделе зародыша и контролирует развитие соответствующей части тела. Терминология, использующаяся для обозначения генов Нох, достаточно запутанная. Названия генов дрозофилы сложились исторически (например, ultrabithorax), в то время как для обозначения генов млекопитающих применяют систему букв (А, В, С, D) и цифр (1, 2, 3,4).
Рис. 28-42. Гены кластера Нох и их роль в развитии организма, а — каждый ген Нох дрозофилы отвечает за развитие структур определенной части тела и экспрессируется в определенных участках зародыша, что показано с помощью разных цветов. б — дрозофила имеет один кластер генов Нох, в геноме человека таких кластеров четыре. У многоклеточных животных многие из этих генов обладают высоким уровнем консервативности. Эволюционные связи между генами кластера Нох дрозофилы и млекопитающих показаны пунктирными линиями. При выравнивании последовательностей аналогичные связи прослеживаются между четырьмя наборами генов Нох млекопитающих.
Утрата гомеотических генов в результате мутации или делеции приводит к развитию нормальных придатков или структур в неправильных местах. Важным примером является ген ultrabithorax (ubх). При потере функции Ubх первый брюшной сегмент развивается неправильно и приобретает структуру третьего грудного сегмента. Другие мутации гомеотических генов вызывают формирование дополнительной пары крыльев или двух ног вместо антенн на голове (рис. 28-43). Многие гены Нох весьма протяженные. Например, длина гена ubх, составляет 77 000 п. н. Более 73 000 п. н. в составе гена приходится на интроны, один из которых имеет длину 50 000 п. н. Транскрипция гена ubх занимает около часа. Полагают, что задержка экспрессии гена ubх, возникающая из-за длительной транскрипции, нужна для синхронизации процессов в общей временной регуляции последующих стадий развития. Многие гены Нох далее регулируются малыми интерферирующими РНК, закодированными между последовательностями генов внутри кластеров Нох. Все продукты генов Нох являются факторами транскрипции и регулируют экспрессию ряда генов на следующих стадиях развития. Эта цепочка взаимодействий все еще изучается.
Рис. 28-43. Результаты мутаций в гомеотических генах дрозофилы, а — нормальная голова. б — гомеотический мутант (antennapedia) с ногами вместо антенн, в — нормальное строение тела, г — гомеотический мутант (bithorax), у которого появился еще один грудной сегмент с дополнительной парой крыльев.

Многие из рассмотренных выше принципов развития справедливы и для других эукариот, от нематоды до человека. Во многих видах функционируют одни и те же белки. Например, продукты гена НОХА7 мыши и гена antennapedia дрозофилы различаются лишь одним аминокислотным остатком. Конечно, несмотря на сходство молекулярных механизмов регуляции, пути развития механизмов различны (у человека нет ни крыльев, ни антенн), что определяется генами-мишенями, контролируемыми генами Нох. Открытие структурных детерминант со специфическими молекулярными функциями — первый шаг к пониманию молекулярных событий, лежащих в основе развития. По мере идентификации новых генов и их белковых продуктов все больше проясняются биохимические аспекты этой гигантской головоломки.
При обсуждении регуляции развития мы сделали круг и вернулись к биохимическим началам — и фигурально, и буквально. Самые первые и самые последние рассуждения в данной книге относятся к теме эволюции. Если эволюция состоит в генерации изменений, приводящих к появлению различных видов организмов, она непременно должна затрагивать программу развития организма. Процессы эволюции и развития тесно связаны между собой (доп. 28-1). Биохимия как наука призвана помочь человечеству одновременно развиваться в будущем и понять собственное происхождение в прошлом.
Дополнение 28-1. О плавниках, крыльях и клювах
В Южной Америке обитает несколько видов вьюрков. Около 3 млн лет назад небольшая группа вьюрков одного вида вылетела с континентального берега Тихого Океана. Возможно, из-за шторма птицы потеряли ориентацию и пролетели около 1000 км. Такие мелкие птицы могли погибнуть в подобном путешествии, однако этим вьюркам повезло, и они долетели до недавно образовавшихся вулканических островов, которые теперь мы называем Галапагосским архипелагом. Здесь было обилие растений и насекомых, и птицы выжили. Со временем образовались новые острова, которые были заселены новыми растениями и насекомыми, а также вьюрками. Птицы использовали биоресурсы островов, и постепенно выделялись отдельные группы вьюрков и превращались в новые виды. В 1835 г. на этих островах побывал Чарльз Дарвин и обнаружил множество видов вьюрков*, питавшихся семенами, фруктами, насекомыми, пыльцой и даже кровью.
* Галапагосские, или дарвиновские, вьюрки - подсемейство семейства вьюрковых, к которому относятся 14 видов птиц, 13 из которых населяют Галапагосские острова, один вид обитает на о. Кокос. Прим. перев.
Разнообразие живых существ поражало человека задолго до того, как ученые начали исследовать его причины. Самая важная роль в этом исследовании принадлежит Дарвину, в частности, его наблюдениям за птицами Галапагосских островов. На основе теории Дарвина можно объяснить само существование организмов разного вида, но возникает вопрос о механизмах эволюционного процесса. Решение этой проблемы ученые стали находить во второй половине XX в. при изучении геномов и метаболизма нуклеиновых кислот и совсем недавно в связи с появлением нового раздела биологии эволюционной биологии развития (сокращенно еvo-devo), которая сочетает изучение процессов эволюции и развития.
В современном виде теория эволюции строится на двух основных положениях: мутации в популяции создают генетическое разнообразие; затем эта популяция подвергается естественному отбору, который благоприятствует распространению организмов с более полезным генетическим инструментарием и подавляет распространение остальных. В геноме каждого организма, в каждой клетке постоянно происходят мутации (см. гл. 8 в т. 1 и гл. 25). Мутации в одноклеточных организмах или в зародышевых клетках многоклеточных организмов могут наследоваться, причем вероятность наследования (т. е. передача мутации значительной части потомства) увеличивается, если такая мутация дает определенное преимущество. Это очевидная схема. Однако многие ученые сомневались в том, может ли такая схема объяснить, скажем, разнообразие формы клюва галапагосских вьюрков или разнообразие форм и размеров млекопитающих. До последних десятилетий существовало несколько широко распространенных гипотез эволюционного процесса. Считалось, что для появления новой физической структуры необходимо множество мутаций и новые гены, сложные организмы должны иметь более крупный геном и у сильно различающихся видов мало общих генов. Все эти предположения оказались ошибочными.
Современные исследования показали, что в геноме человека содержится меньше генов, чем предполагалось, — немного больше, чем в геноме дрозофилы, и меньше, чем в геноме некоторых земноводных. Геномы всех млекопитающих — от мыши до человека — удивительно похожи по числу, типу и хромосомному расположению генов. Однако эволюционная биология развития объясняет, как на таком генетическом базисе могут эволюционировать сложные и очень разнообразные создания.
В конце XIX в. английский биолог Уильям Бейтсон изучал различных мутантных животных, вроде тех, что изображены на рис. 28-43. На основании своих наблюдений он оспаривал утверждение Дарвина о том, что эволюционные изменения должны быть постепенными. Современные исследования генов, контролирующих развитие организма, подтвердили идеи Бейтсона. Незначительные изменения механизмов регуляции в ходе развития, возникающие в результате лишь одной или нескольких мутаций, могут привести к физическим изменениям и удивительно быстрой эволюции.
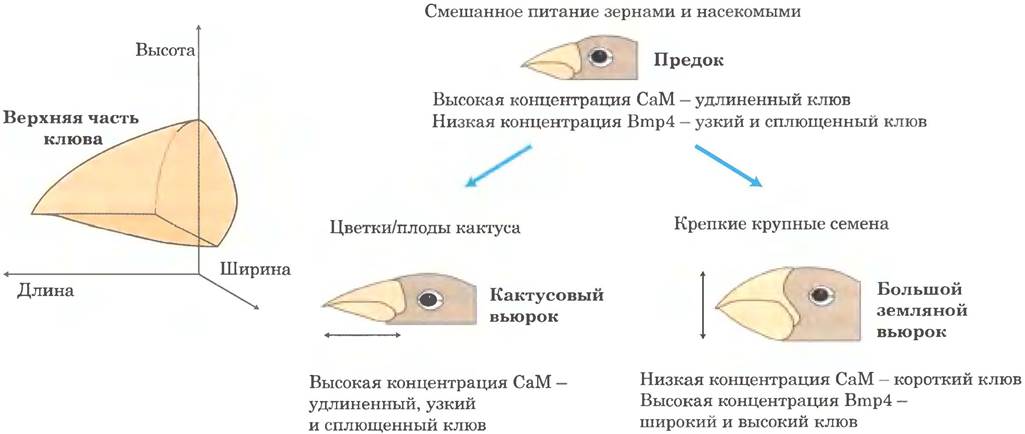
Галапагосские вьюрки — прекрасный пример, демонстрирующий связь между эволюцией и развитием. Существует 14 (некоторые специалисты называют 15) видов галапагосских вьюрков, основные различия между которыми заключаются в строении клювов. У земляных вьюрков, например, широкий тяжелый клюв, предназначенный для раскалывания крупных и прочных зерен. У кактусовых вьюрков клюв более длинный и тонкий, он идеально подходит для проникновения в плоды и цветки кактусов (рис. 1). Клиффорд Табин с коллегами тщательно проанализировали набор генов, экспрессирующихся в ходе развития головы птиц. Они идентифицировали единственный ген, Вmр4, уровень экспрессии которого коррелирует с образованием более мощного клюва у земляных вьорков. В экспериментальных условиях более высокий уровень экспрессии гена Втр4 в соответствующих тканях также вызывает образование более крепких клювов у зародышей кур, что подтверждает значение гена Втр4. В аналогичном исследовании было показано, что формирование более длинного и тонкого клюва коррелирует с экспрессией гена кальмодулина (см. рис. 12-11 вт. 1) в определенных тканях на определенной стадии развития Таким образом, значительные изменения формы и функций клюва могут быть вызваны небольшими изменениями экспрессии всего двух генов, участвующих в регуляции развития. Нужно лишь несколько мутаций, но они должны затрагивать механизмы регуляции. Новые гены не нужны.
Рис. 1. Эволюция строения клюва для приспособления к новым источникам пищи. Различие в строении клювов у двух видов галапагосских вьюрков (кактусового вьюрка и крупного земляного вьюрка), питающихся по-разному, в значительной степени объясняется небольшим числом мутаций, которые изменили время и уровень экспрессии всего двух генов — гена кальмодулина и гена Вmр4.
У всех позвоночных система регуляторных генов, ответственных за развитие, очень консервативна. Повышение уровня экспрессии Вmр4 в нужной ткани и в нужное время приводит к формированию более мощной челюсти у полосатых данио. Тот же ген играет ключевую роль в развитии зубов млекопитающих. Развитие глаз дрозофил и млекопитающих запускается экспрессией одного и того же гена. Рах6. Мышиный ген Рах6 запускает развитие нормальных глаз мушки у дрозофилы, а ген Рах6 дрозофилы запускает развитие мышиных глаз у мыши. В каждом организме эти гены являются частью сложного регуляторного каскада, который в конечном итоге приводит к образованию правильных структур в правильном месте в каждом организме. Это очень древний каскад. Например, описанные гены Нох участвовали в развитии многоклеточных эукариот на протяжении более 500 млн лет. Незначительные изменения регулярного каскада оказывают сильное влияние на развитие и, следовательно, на внешний вид организма. Эти же незначительные изменения могут стать толчком для необычайно быстрой эволюции. Например, от 400 до 500 известных видов цихлид (окуневых рыб), обитающих в озерах Малави и Виктория на Африканском континенте, происходят от одной или от небольшого числа популяций, населявших эти озера 100- 200 тыс. лет назад. Птицы Галапагосских островов прошли свой заключительный путь эволюции, который у других живых существ занял миллиарды лет.
Краткое содержание раздела 28.3 Регуляция экспрессии генов у эукариот
■ Для эукариотических генов более характерна положительная регуляция, чем отрицательная, и транскрипция сопровождается большими изменениями структуры хроматина.
■ Типичные промоторы Pol II содержат ТАТА- бокс и последовательность Inr, а также многочисленные участки связывания активаторов транскрипции. Последние иногда расположены за сотни или тысячи пар оснований от ТАТА-бокса; в дрожжах они называются активирующими последовательностями (UAS), а в высших эукариотах — энхансерами.
■ Для регуляции транскрипции обычно требуются крупные белковые комплексы. Влияние активаторов транскрипции на Pol II опосредовано ко-активаторными белковыми комплексами, такими как медиатор. Активаторы содержат отдельные домены, отвечающие за активацию и за связывание ДНК. Другие белковые комплексы, включая гистонацетилтрансферазы и ATP-зависимые комплексы, такие как SWI/SNF и NURF, обратимо перестраивают и модифицируют структуру хроматина.
■ Гормоны регулируют экспрессию генов одним из двух способов. Стероидные гормоны напрямую взаимодействуют с внутриклеточными рецепторами, которые являются ДНК- связывающими регуляторными белками; связывание гормона либо усиливает, либо ослабляет транскрипцию генов-мишеней. Нестероидные гормоны связываются с рецепторами на клеточной поверхности, запуская сигнальный путь, который может привести к фосфорилированию регуляторного белка и изменить его активность.
■ Регуляция экспрессии генов при участии молекул РНК играет важную роль в эукариотических клетках, причем число известных механизмов такой регуляции продолжает расти.
■ Развитие многоклеточного организма регулируется очень сложно. Судьба клеток в раннем эмбрионе определяется путем формирования переднезаднего и спинно-брюшного градиентов белков, которые действуют как активаторы транскрипции или репрессоры трансляции, регулируя экспрессию генов, необходимых для развития определенных структур в определенных частях тела. Группы регуляторных генов последовательно действуют во времени и пространстве, превращая отдельные зоны яйцеклетки в структуры взрослого организма.