Биохимия человека Том 1 - Марри Р. 1993
Структура и функции белков и ферментов
Ферменты: кинетика
Концентрация фермента
Во многих случаях бывает недостаточно знать, что данный фермент присутствует в системе, нужна еще информация о его количестве. При определенных условиях скорость ферментативной реакции прямо пропорциональна количеству фермента (гл. 7).
Это бывает не всегда, что можно проиллюстрировать на примере прямой реакции, идущей в равновесных условиях. Даже если мы знаем, что прямая реакция действительно идет, нам будет казаться, что скорость ее равна нулю, поскольку с такой же скоростью идет и обратная реакция. Когда же ферментативная реакция только начинается, продукт еще практически отсутствует и обратная реакция не идет.
Кроме того, на начальной стадии реакции концентрация субстрата соответствует его исходному количеству. Поэтому скорость в начале реакции, т. е. ее начальная скорость (г), будет прямо пропорциональна концентрации фермента [Enz] (гл. 7).
Фермент является реактантом, который соединяется с субстратом, образуя фермент-субстратный комплекс Enz — S, распадающийся на свободный фермент и продукт Р. В простейшей форме можно записать
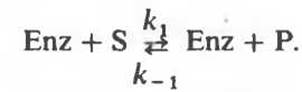
Отметим, что хотя в выражения для скоростей прямой и обратной реакций входит член [Enz]:
Скорость1 = k1[Enz][S],
Скорост-1 = k-1[Enz][P],
в выражении для константы равновесия [Enz] уже не содержится:
![]()
Таким образом, концентрация фермента не оказывает влияния на константу равновесия. Кeq не зависит от того, каким образом достигается равновесие — с участием фермента или без него (вспомним о величине ∆G°). Фермент меняет путь, по которому идет реакция, но не конечные (равновесные) концентрации реагентов и продуктов, от которых зависят Кeq и ∆G°.