Биохимия аминокислот - А. Майстер 1961
Промежуточный обмен аминокислот
Фенилаланин и тирозин
Прочие реакции обмена тирозина
Наряду с распадом тирозина путем описанных выше превращений он переходит в организме в ряд других соединений, например в адреналин, норадреналин, меланины и йодированные производные (тироксин и др.). Гурин и Деллюва [992] показали, что в теле крысы фенилаланин, меченный дейтерием или тритием, превращается в адреналин, причем исходная боковая цепь остается при окислении в ядре нетронутой. В дальнейшем было показано, что меченые фенилаланин и тирозин оба служат предшественниками адреналина надпочечников [993]. Юденфренд и Вайнгарден [994] нашли, что у крысы 3, 4-диоксифенилаланин, подобно тирозину и фенилаланину, превращается в адреналин и норадреналин, тогда как тирамин и фенилэтиламин этому превращению не подвергаются.
Первичным адренергическим веществом, согласно имеющимся данным, является норадреналин, а не адреналин [995]. В опытах in vivo на крысах методом изотопной индикации установлено, что 3,4-диоксифенилэтиламин также является предшественником адреналина надпочечников [1138]. Вероятный путь образования этих адренергических веществ следующий:
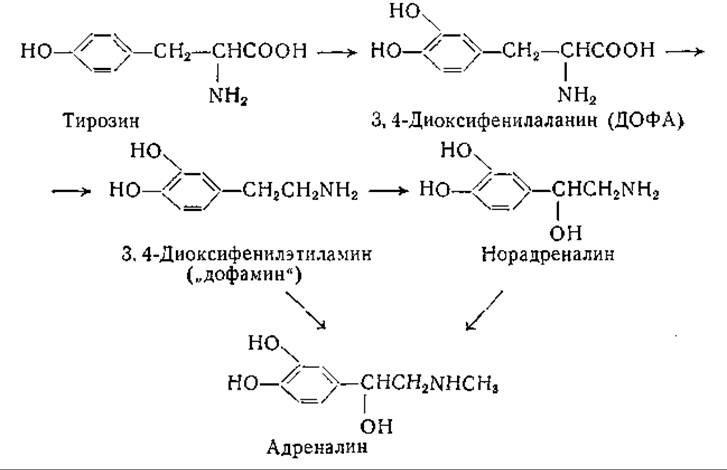
Окисление тирозина в ДОФА катализируется тирозиназой (996—998], которая имеется как в растительных, так и в животных тканях. Декарбоксилирование ДОФА имеет место в тканях животного и растительного происхождения. Реакция гидроксилирования тирозина в деталях не изучена. Известно, что метальная группа вводится в адреналин путем трансметилирования (стр. 370).
Схема, приведенная выше, еще не полностью подтверждена экспериментально. Были получены данные, указывающие на возможность существования других путей биосинтеза адреналина. Так, например, образование норадреналина наблюдали при инкубировании кашицы из почек морских свинок в анаэробных условиях с диоксифенилсерином [945].
Имеются указания на наличие в природе изопропилового аналога адреналина: опубликованы хроматографические данные, свидетельствующие о присутствии «изопреналина» в солевых экстрактах надпочечников обезьяны, кошки и человека [1139].
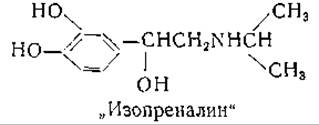
Тирозин через ДОФА и 5,6-диоксииндол переходит в меланин. Рейпер [996, 999] и Мейсон [997] обосновали следующий путь образования меланина:
На основе изучения полимеризации 5,6-диоксииндола высказаны предположения о механизме этой реакции [1000, 1001].
Тирозин играет роль предшественника при образовании тироксина, монойодтирозина, 3, 5-дийодтирозина и 3, 3', 5-трийодтиронина. Имеется множество данных о том, что меченый ион йодида переходит в организме в йод тироксина и 3, 5-дийодтирозина, но механизм йодирования не ясен. Джонсон и Тьюксбери [1002] и Харингтон [1003] изучали образование тироксина из дийодтирозина. Они предложили следующую схему превращения с образованием свободных радикалов:
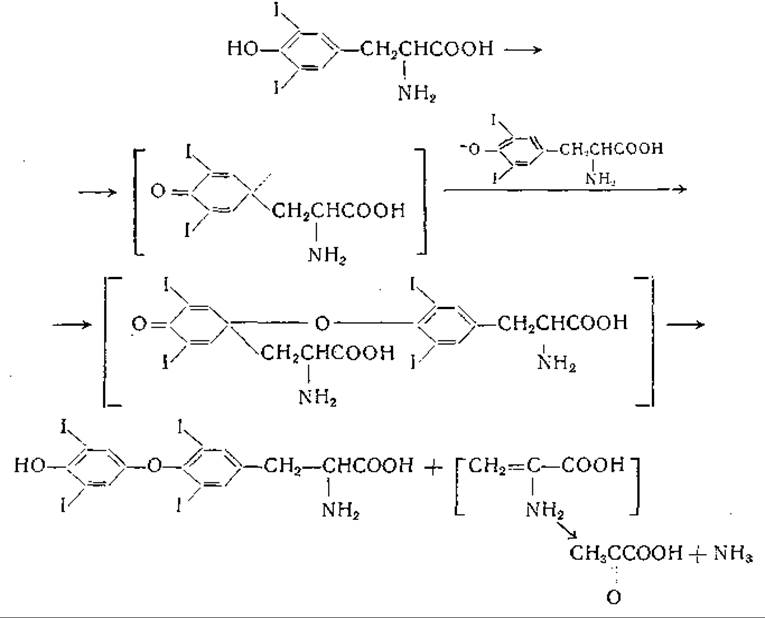
Механизм образования тироксина был предметом обширной дискуссии [966, 1004]. С открытием 3, 3', 5'-трийодтиронина [1005, 1006], физиологическая активность которого выше, чем у тироксина, снова встал вопрос о том, какова истинная природа гормона щитовидной железы. Механизм образования 3, 3', 5-трийодтиронина неизвестен; возможно, что он образуется из тироксина путем дейодирования [1007]. В щитовидной и подчелюстной железах найден фермент, названный «тирозиндейодиназа» [1008]. Этот фермент катализирует обратимую реакцию между тирозином и свободным йодом с образованием монойодтирозина.
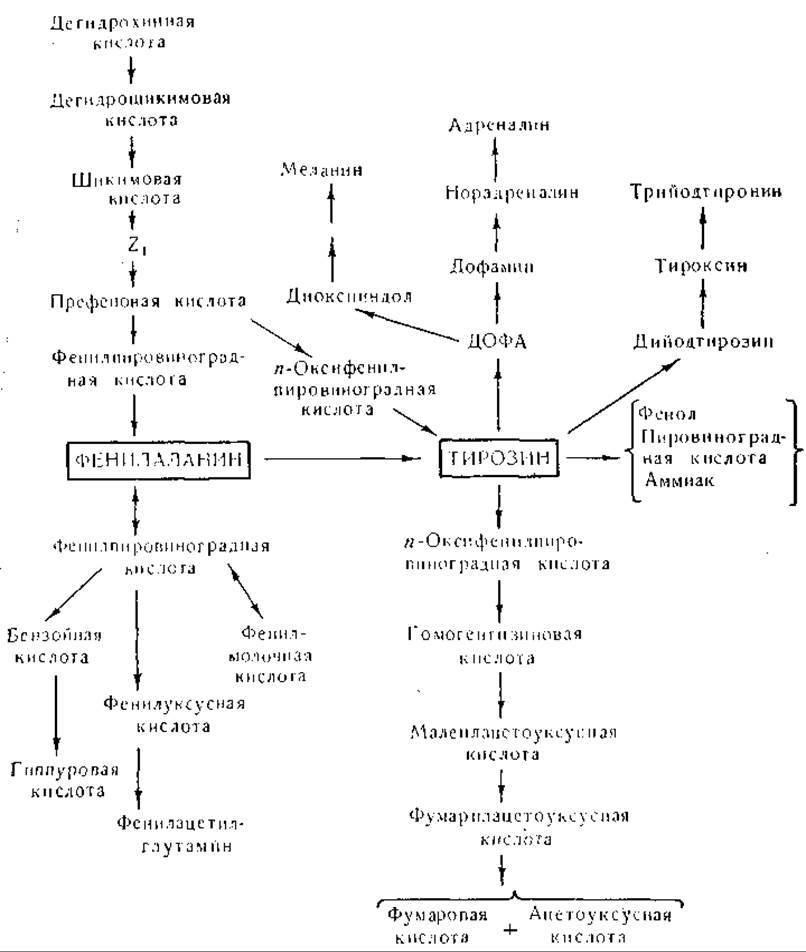
Фиг. 21. Сводная схема превращений фенилаланина и тирозина.
В печени и почках имеется сходная ферментная система, катализирующая дейодирование дийодтирозина и трийодтиронина [1140]. Возможно, что другие ферменты этого типа осуществляют взаимопревращение тироксина и трийодтиронина [1009, 1010]. Распад тироксина и трийодтиронина, по-видимому, протекает через реакции переаминирования (как это показано для 3, 5-дийодтирозина [1011]); образующиеся этим путем кетокислоты могли бы декарбоксилироваться [1012].
Бактерии осуществляют разложение тирозина путем ряда реакций, в результате которых образуются такие продукты, как фенол, n-крезол, n-оксибензойная кислота и др. [1013, 1014]. Превращение в фенол происходит под действием ß-тирозиназы1, отщепляющей боковую цепь [555].
Тирозин найден в нормальной моче человека в виде соответствующей фенолосерной кислоты (тирозин-О-сульфата) [1015]. Он встречается, по-видимому, в этой форме и в фибриногене [1016]. Механизм образования тирозин-О-сульфата и значение этого производного неизвестны.