Биохимия аминокислот - А. Майстер 1961
Общая биохимия и физиология аминокислотного обмена
Синтез пептидных связей
Синтез других соединений, содержащих -CONH-связи
Биосинтезу некоторых других низкомолекулярных соединений, обладающих —CONH-связями (например, карнозина, аспарагина, пенициллина, пантотеновой кислоты), посвящен ряд работ, но в общем об этих ферментных системах известно меньше, чем о ферментах, осуществляющих синтез глутатиона и глутамина. Найдено, что ферментная система, активирующая синтез глутамина, не катализирует синтез аспарагина из L-аспарагиновой кислоты, аммиака и аденозинтрифосфата. Описано образование аспарагина путем реакций переаминирования, т. е. путем переноса аминогруппы на ß-амид щавелевоуксусной кислоты (β-амид кетоянтарной кислоты) ([290]; стр. 223), а также путем переноса амидной группы от глутамина к аспарагиновой кислоте [573] Обсуждалась также возможность образования аспарагина из аспарагиновой кислоты, аммиака и аденозинтрифосфата при участии ферментной системы, отличающейся от той, которая синтезирует глутамин [574]. Найдено, что препараты из зародышей пшеницы катализируют образование ß-аспартилгидроксамовой кислоты из L-аспарагиновой кислоты и гидроксиламина в присутствии ионов магния и аденозинтрифосфата. Еще не ясно, катализирует ли система, участвующая в образовании ß-аспартилгидроксамовой кислоты, также образование аспарагина. В дрожжах путем аналогичной реакции катализируется образование ß-аспартилфосфата; последний, по-видимому, не служит предшественником аспарагина, но вместе с тем установлено, что он является промежуточным продуктом при образовании гомосерина из аспарагиновой кислоты (стр. 333). Для действия ферментной системы зародышей пшеницы, синтезирующей ß-аспартилгидроксамовую кислоту (в отличие от системы, синтезирующей глутамин), необходимы высокие концентрации аспарагиновой кислоты и гидроксиламина. Имеются данные о том, что система из зародышей пшеницы катализирует включение С14-аспарагиновой кислоты в аспарагин в присутствии аденозинтрифосфата, аммиака и ионов магния, однако остается неясным, происходит ли при этом реальный синтез аспарагина. Детальное рассмотрение механизма синтеза аспарагина следует отложить впредь до получения дополнительных сведений.
Образование карнозина из ß-аланина и гистидина было установлено в опытах со срезами печени. Для обнаружения синтеза карнозина был применен микробиологический способ определения гистидина; определения производили до и после гидролиза кислотой [575]. Данные, полученные при использовании меченого ß-аланина, подтвердили образование карнозина из ß-аланина и гистидина [576].
Много внимания было уделено изучению синтеза пантотеновой кислоты из ß-аланина и пантоиновой кислоты. Реакция, по-видимому, не требует наличия кофермента А; для нее необходимо присутствие аденозинтрифосфата, ионов магния (или марганца) и калия (или аммония). Обсуждение реакции см. на стр. 311.
1 Существование такой реакции переамидирования не нашло подтверждения [Сюй Тии - сень, Биохимия, 24, 528 (1959)]. — Прим. ред.
Синтез пенициллина штаммами Penicillium изучали при помощи меченых аминокислот. При добавлении меченого DL-валина к ферментационной смеси Стивенс и сотрудники [577] нашли, что карбоксильная группа пенициллина могла иметь источником валин; эта аминокислота, меченая в метальных группах, включается в пеницилламиновую часть молекулы антибиотика [578]. L-Валин включается, по-видимому, быстрее, чем D-валин [709]. Предшественниками ацильной группы могут служить самые различные кислоты [579], а источником β-лактамного кольца является, по-видимому, L-цистин [578—581, 709, 710]. L-Цистин более эффективен как предшественник пенициллина, чем D-цистин [578].
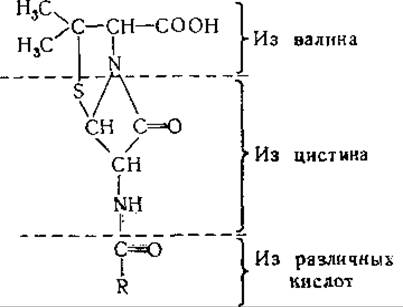
Выяснение механизма образования пенициллина из указанных предшественников остается задачей будущих исследований (см. [710]).