Биохимия аминокислот - А. Майстер 1961
Общая биохимия и физиология аминокислотного обмена
Биосинтез пуринов
Возможную роль аминокислот в качестве предшественников, в биосинтезе пуринового ядра изучали уже давно. В опытах с применением меченых соединений было найдено, что гистидин и аргинин, несмотря на их структурное сходство с пуринами, не являются непосредственными источниками азота для синтеза пуринов [669, 670]. Вместе с тем было показано, что срезы печени голубя синтезируют гипоксантин и что добавление глутамина или щавелевоуксусной кислоты к таким тканевым препаратам повышает количество синтезируемого гипоксантина [671—673].
Успешному изучению биосинтеза пуринов в значительной мере способствовали изотопные исследования, пролившие свет на происхождение атомов азота и углерода в пуриновом ядре. Было установлено, что глицин является предшественником атомов С-4, С-5 и N-7 [674, 675], СО2 — предшественником атома С-6 [674—676], муравьиная кислота — предшественником атомов С-2 и С-8 [676], глутамин — предшественником атомов N-3 и N-9 [677] и аспарагиновая кислота — предшественником атома N-1 [677, 723]. Эти данные иллюстрирует следующая схема:
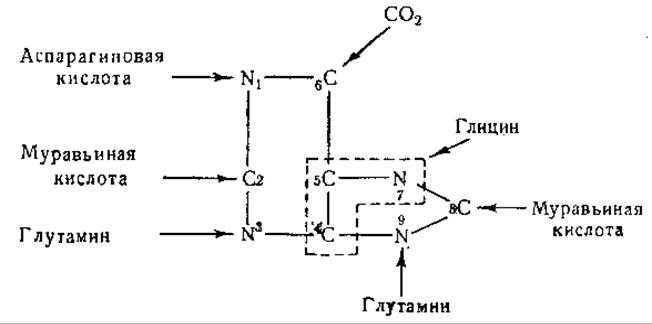
В опытах с экстрактами из печени голубя было найдено, что для образования одного моля гипоксантина используются 2 моля муравьиной кислоты, 1 моль СО2 и 1 моль глицина [678]; позднее установили, что на каждый моль включенного в гипоксантин глицина приходится два атома азота, имеющих источником амидную группу глутамина. Половина включенного в пурин амидного азота была найдена в атоме N-9, а другая половина — в смешанном азоте атомов N-1 и N-3. При использовании N15-аспарагиновой или N15-глутаминовой кислоты изотопом метилась только суммарная фракция N-1 + N-3 [677]. Эти данные свидетельствовали о возможной роли амидной группы глутамина как источника атома N-1 (или N-3) и о происхождении второго из этих атомов из а-аминогруппы. Дальнейшие работы показали, что источником атома N-1 является аспарагиновая кислота [723].
При исследовании синтеза инозиновой кислоты в препаратах печени голубя (в присутствии глицина, формиата, бикарбоната, рибозо-5-фосфата, 3-фосфоглицериновой кислоты и цитроворумфактора) было найдено, что добавление L-аспарагина или L-глутамина стимулирует синтез этой кислоты [678]. Меньшее влияние оказывают глутаминовая и аспарагиновая кислоты, а ряд других аминокислот вообще не дает никакого эффекта. Добавление глутаминовой кислоты к глутамину или аспарагиновой кислоты к аспарагину не приводило к существенному усилению синтеза инозиновой кислоты по сравнению с синтезом ее в присутствии одних амидов. Вместе с тем добавление аспарагиновой кислоты к глутамину и в несколько меньшей степени добавление глутаминовой кислоты к аспарагину значительно повышало количество образующейся инозиновой кислоты. Эти данные указывают на то, что требуется одновременное наличие производных С4- и С5-аминодикарбоновых кислот, из которых одно должно иметь амидную группу в ω-положении. Такие результаты можно объяснить образованием глутамина из глутаминовой кислоты и аммиака, отщепляющегося от аспарагина при его ферментативном гидролизе.
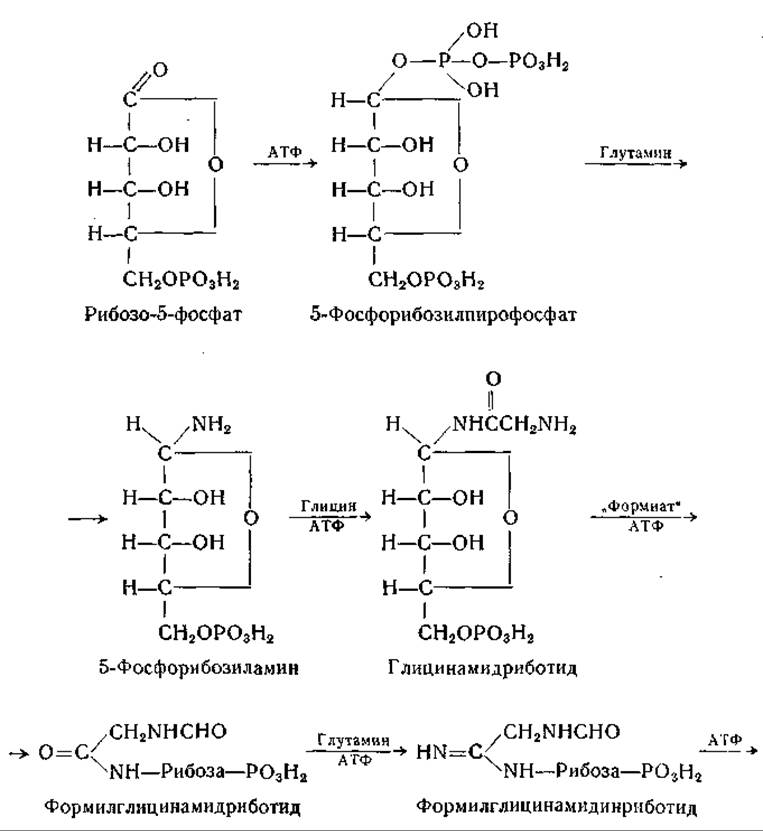
То обстоятельство, что в ферментных препаратах из печени голубя инозиновая кислота служит предшественником гипоксантина, давало основание предполагать образование рибонуклеотидов на ранних этапах процесса биосинтеза пуринового ядра [679]. Дальнейшие исследования, выполненные в лабораториях Гринберга [679—683, 718—720] и Бьюкенена [684—690, 721—723], способствовали расшифровке механизма синтеза пуринов. Было найдено, что в присутствии глутамина, аденозинтрифосфата, глицина и 5-фосфорибозилпирофосфата одна из белковых фракций печени голубя синтезирует глицинамидриботид. Первой ступенью в цепи реакций является, по-видимому, образование 5-фосфорибозиламина из глутамина и 5-фосфорибозилпирофосфата [683, 718]. Глицинамидриботид, присоединяя формильную группу, превращается в формилглицинамидриботид. Последний реагирует с глутамином, образуя формилглицинамидинриботид, который, вероятно, превращается путем замыкания кольца в аминоимидазолриботид. Из этого соединения в присутствии СО2 и аспарагиновой кислоты образуется 5-амино-4-имидазолкарбоксамидриботид, который затем акцептирует формильную группу и циклизуется с образованием инозиновой кислоты. Эти реакции можно представить следующим образом:
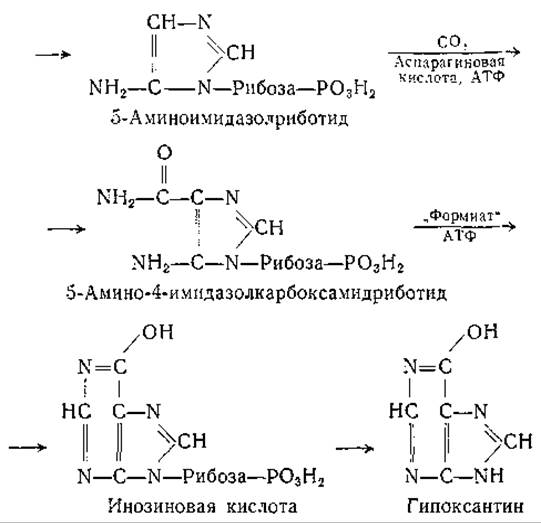
Большое значение имели данные о накоплении 4-амино-5-имидазолкарбоксамидрибозида и соответствующего рибонуклеотида в культурах Escherichia coli при торможении их роста сульфамидными препаратами [691—694]. Эти наблюдения послужили поводом к изложенным выше исследованиям об образовании ациклических рибонуклеотидов. Ранее из культур Е. coli, выращенных в присутствии сульфамидов, был выделен свободный 4-амино-5-имидазолкарбоксамид [691—692]. Вероятно, торможение роста бактерий и синтеза пуринов под действием сульфамидов связано с нарушением синтеза кофакторов, образующихся из n-аминобензойной кислоты. Описано также конкурентное торможение превращения формилглицинамидриботида в формилглицинамидинриботид под влиянием азасерина. В присутствии этого антибиотика, который, по-видимому, способен тормозить рост опухолей (стр. 46), накапливается глицин-амидриботид [687]. Азасерин вызывает также конкурентное торможение реакции между глутамином и 5-фосфорибозилпирофосфатом, приводящей к образованию 5-фосфорибозиламина [721].
Найдено, что цитроворум-фактор (стр. 327) или родственное ему производное фолевой кислоты участвует во включении формиата в пуриновое ядро в положениях 2 и 8, а также в реакции обмена между формиатом и атомом С-2 инозиновой кислоты [695].
Ряд деталей реакций, с которыми связан биосинтез пуринов, еще не выяснен. Однако, судя по тому, как успешно продвигается изучение этого процесса в настоящее время, можно ожидать, что многие относящиеся к нему вопросы будут решены в ближайшем будущем1.
1 Сводка более новых данных о механизме биосинтеза пуринов дана в обзорной статье J. М. Buchanan and S. С. Hartman, Advances Enzymol. 21, 199 (1959); о пути биосинтеза пиримидинов см. обзор Р. Reichard, Advances Enzymol., 21, 263 (1959). — Прим. ред.