Биохимия - Химические реакции в живой клетке Том 1 - Д. Мецлер 1980
Как молекулы соединяются друг с другом
Кооперативные изменения конформации
Гемоглобин
Рассмотрим теперь вопрос о природе кооперативного связывания кислорода с тетрамерной (a2ß2) молекулой гемоглобина (разд. Г.8) и физиологическое значение этого процесса [65]. Полипептидная цепь каждой из субъединиц гемоглобина специфическим образом уложена вокруг большого плоского железосодержащего кольца гема (рис. 4-17). Характер укладки полипептидной цепи в а- и ß-субъединицах всех гемоглобинов, как и в мономерном связывающем кислород мышечном белке миоглобине, по существу, одинаков. Имидазольная группа гистидина F-8 связана координационной связью с атомом железа, расположенным в центре гема. С другой стороны к атому железа присоединяется молекула O2.
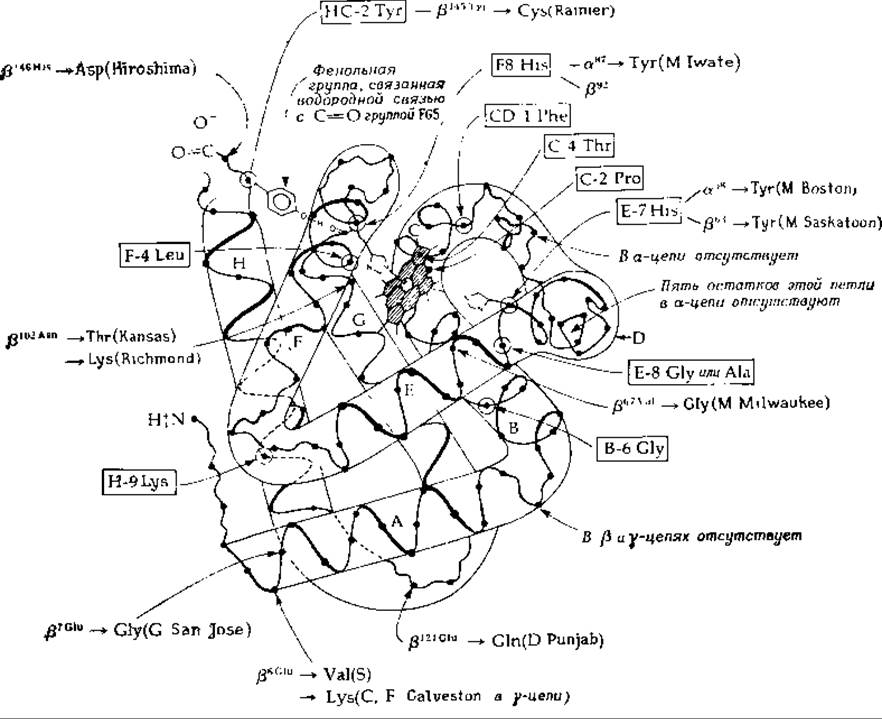
РИС 4-17. Схематическое изображение структуры мономера гемоглобина. На этом рисунке изображена ß-цепь гемоглобина человека Указаны некоторые различия между данной цепью, а цепью и многлобином. Инвариантные аминокислотные остатки заключены в прямоугольные рамки. Отмечены также остатки, которые заменены в некоторых аномальных гемоглобинах человека Инвариантные остатки пронумерованы в соответствии с их местоположением в одной из спирален (от А до Н), для остатков, обнаруженных в мутантных гемоглобинах, указаны положения, по которым происходят замещения в а- или ß-цепях
Кооперативный характер связывания O2 гемоглобином иллюстрируется кривыми, приведенными на рис. 4-18. Значение nХилл [уравнение (4-35)] зависит от условий и может достигать трех. Физиологическое значение кооперативного связывания ясно. В капиллярах легких при парциальном давлении кислорода, равном — 100 мм рт. ст., гемоглобин почти полностью насыщен кислородом, однако когда эритроциты проходят через капилляры тканей, потребляющих кислород, его парциальное давление падает примерно до 5 мм рт. ст. Кооперативноеть приводит к тому, что гемоглобин «разгружается» более полно, чем в том случае, если бы четыре гемогруппы действовали независимо.
Дезоксигемоглобин обладает слабым сродством к О2, однако после оксигенации одной или большего числа субъединиц сродство остальных субъединиц к кислороду возрастает приблизительно в 500 раз1. Мономерный миоглобин, как и аномальный гемоглобин Н, молекулы которого состоят из четырех ß-субъединиц, обладает высоким сродством к кислороду, причем связывание для последнего не носит кооперативного характера [66]. Эти результаты можно объяснить, исходя из того, что дезоксигемоглобин находится в А(Т)-конформации, а оксигемоглобин — в В (R)-конформации. Разделенные же субъединицы и миоглобин в обоих состояниях оксигенации находятся в В-конформации. Субъединицы гемоглобина Н также, по-видимому, «заморожены» в В-конформации, хотя его четвертичная структура аналогична четвертичной структуре дезоксигемоглобина [66]. Исходя из данных по оксигенации гемоглобина при pH 7, были рассчитаны параметры, характеризующие этот процесс [67], в рамках модели Моно—Уаймена—Шанжё: L = 9∙103, с = КfA/KfB = 0,014 [см. уравнение (6-52)].
Если в случае дезоксигемоглобина никакой заметной диссоциации тетрамера на субъединицы не наблюдается, то оксигемоглобин слабо диссоциирует на aß-димеры (K=2∙10-6). Вопросу связывания гемоглобинов с кислородом посвящено огромное количество pабот. Последние данные рассмотрены в обзорах [67, 68, 68а].
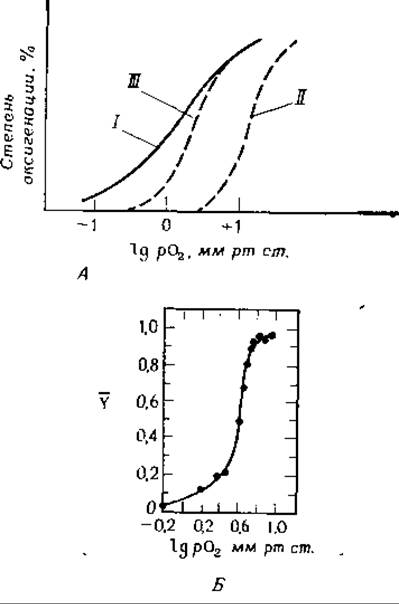
РИС. 4-18. Кооперативное связывание кислорода гемоглобинами. А. Кривые связывания для миоглобина (отсутствие кооперативности) (I), для гемоглобина в цельной крови (II) и в отсутствие 2,3-дифосфоглицерата (III) [75]. Обратите внимание на уменьшение сродства гемоглобина к кислороду, обусловленное дифосфоглицератом Б. Кривая насыщения для эритрокруорина Arenicola — кольчатого червя. Молекула содержит 192 субъединицы и 96 гемов Форма кривой свидетельствует об очень высокой степени кооперативности (nХилл ≈ 6) (Waxman L., JBC, 246, 7318—7327, 1971).
1 Имеется в виду присутствие эффектора 2,3-дифосфоглицерата в физиологичееких концентрациях.
а. Структурные изменения, сопровождающие связывание кислорода
С помощью рентгеноструктурного анализа Перутц с сотрудниками обнаружили, что конформации субъединиц дезокси- и оксигемоглобина, хотя и слабо, но вполне достоверно различаются [69, 70]. Более удивительным оказался тот факт, что в процессе оксигенации как а-, так и ß-субъединицы поворачиваются друг относительно друга, в результате чего гемы обеих ß-субъединиц оказываются в оксиформе примерно на 0,07 нм ближе друг к другу, чем в дезоксиформе. Изменения в области a1ß1-контакта (рис. 4-19) невелики, зато изменения в области а1β2-контакта очень значительны. По выражению Перутца, здесь имеет место «плотное схлопывание» CD-участка a-субъединицы с FG-участком ß-субъединицы, сопровождающееся перестройкой всей системы водородных связей.
Другое очевидное различие между окси- и дезоксигемоглобином состоит в наличии на концах молекул последнего ионных связей.
Группа —NH3 Lys Н-10 каждой из a-субъединиц связана при помощи водородной связи с карбоксильной группой С-концевого аргинина противоположной a-цепи, гуанидиниевая же группа каждого С-концевого аргинина связана с карбоксильной группой аспарагиновой кислоты Н-9 в противоположной a-цепи. Кроме того, она связана водородной связью с неорганическим анионом (фосфатом или ионом Сl-), который в свою очередь связан (также при помощи водородной связи) с a-аминогруппой валина-1 противоположной a-цепи (пара изологических взаимодействий). На другом конце молекулы С-концевая группа гистидина-146 каждой ß-цепи связана с аминогруппой лизина С-6 а-цепи, а имидазольная боковая цепь — с аспарагиновой кислотой FG-1 той же самой ß-цепи. По-видимому, именно эти ионные связи обусловливают повышенную устойчивость дезоксигемоглобина и ответственны за высокое значение константы L.
Остаток тирозина НС-2, расположенный на втором месте со стороны С-конца, является одним из немногочисленных инвариантных остатков в молекуле гемоглобина. Положение его сохранилось в процессе эволюции в гемоглобинах и миоглобинах всех изученных видов. В дезоксигемоглобине тирозин НС-2 лежит как бы в «кармане», образуемом Н- и F-спиралями, и связан водородной связью с карбонильной группой полипептидной цепи у остатка FG-5 (рис. 4-17 и 4-19). Перутц и его сотрудники обнаружили, что при оксигенации этот тирозин выходит из кармана, солевые мостики на концах молекул разрываются и субъединицы смещаются, образуя новую систему связей, характерную для оксигемоглобина. Оксигенация двух гемов (Перутц считает, что ими являются гемы a-цепей) приводит к кооперативному конформационному изменению всех четырех субъединиц [71, 72].
Каким образом присоединение O2 к гемовому железу вызывает конформационное изменение гемоглобина? Как указано в гл. 10 (разд. Б.4), при связывании с кислородом атом железа в геме, по-видимому, смещается в плоскости гемогруппы приблизительно на 0,06 нм [73]. Это смещение передается через гистидин F-8, и спираль F смещается в сторону гема; в результате происходит изменение третичной структуры, приводящее к ослаблению водородных связей в области а1β2-контактов и солевых мостиков между субъединицами. Несмотря на тщательные рентгеноструктурные исследования, детали механизма, инициирующего конформационные изменения при присоединении О2, остаются неясными. Необходимо иметь в виду, что разрешение, которое удается получить при рентгеноструктурном исследовании кристаллов белков, позволяет установить локализацию легких атомов с достаточной точностью, в результате чего механизм передачи кооперативных эффектов не поддается непосредственному изучению и его приходится выяснять, исходя из изменений третичной структуры субъединиц при отщеплении лиганда от Р(т. е. окси-)- или при присоединении его к Т (т. е. дезокси-)-структуре. Ясно, что выяснение столь тонкой вещи, как молекулярный механизм кооперативного связывания кислорода гемоглобином, представляет собой весьма сложную задачу.
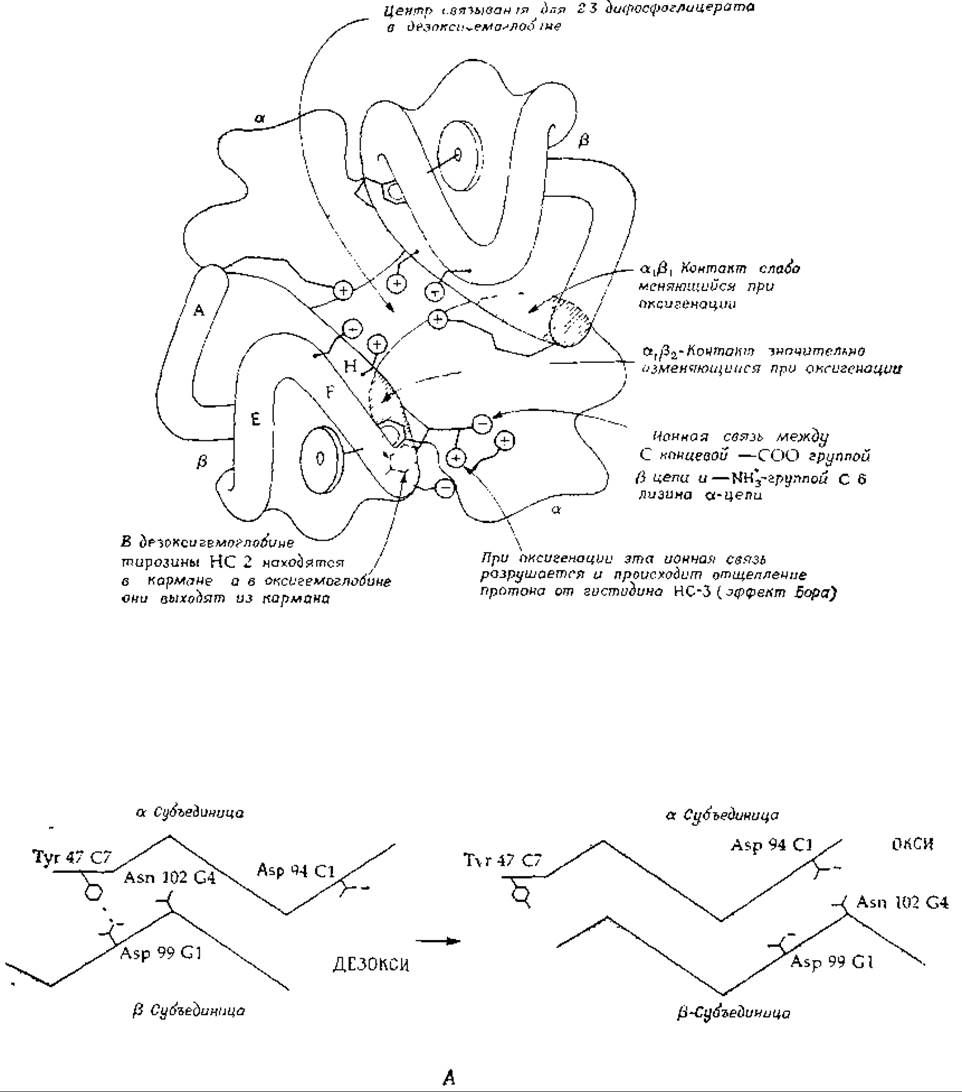
РИС 4 19 А Структурные изменения происходящие в гемоглобине при оксигенации [71, 72] «Поворот в области контакта а1ß2приводит к более плотной «подгонке» CD области (а1 субъединицы и FG области ß2субъединицы и быстрой перестройке всей системы водородных связей» (Перутц)
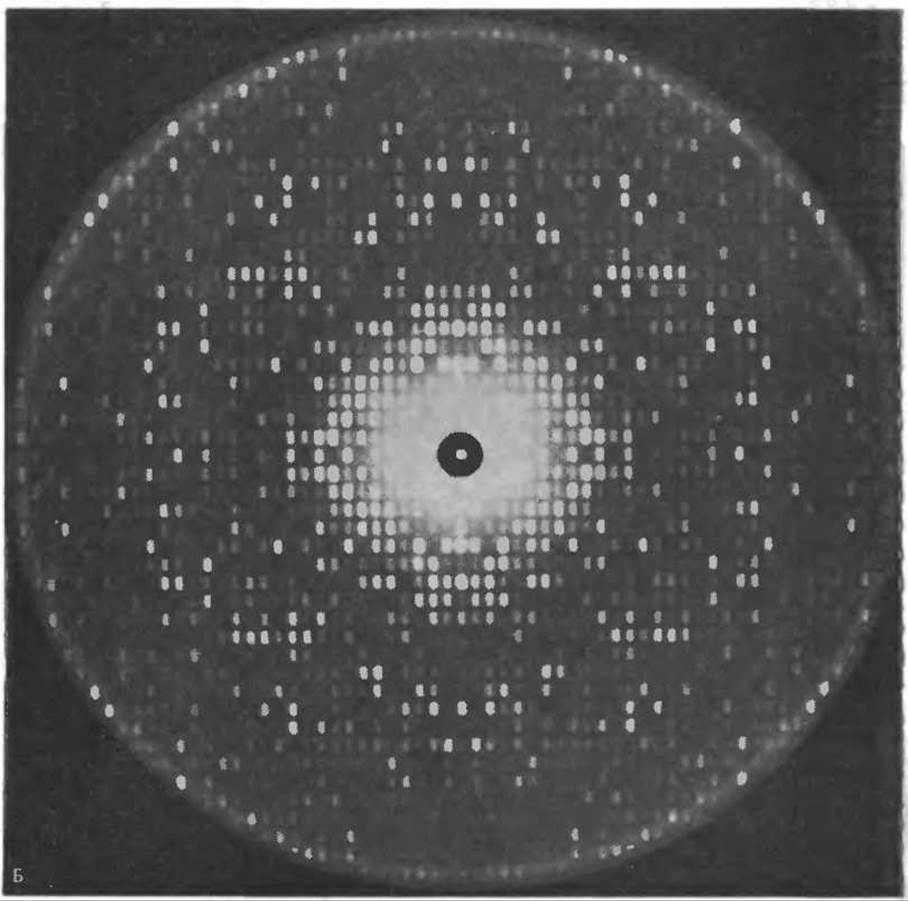
РИС. 4-19. Б. Рентгенограмма, используемая при определении структуры гемоглобина. Дифракционная картина получена от кристалла дезоксигемоглобина человека; кристалл вращали определенным образом вокруг двух разных осей, пропуская через него пучок рентгеновских лучей. При этом синхронно перемещалась и рентгеновская пленка. Наблюдаемая на рентгенограмме периодичность является следствием дифракции рентгеновских лучей на периодически расположенных атомах в кристалле. Расстояния рефлексов от начала координат (центра) обратно пропорциональны расстояниям между плоскостями атомов в кристалле. На этой фотографии (которая показывает только два измерения трехмерной дифракционной картины) рефлексы, расположенные на периферии, соответствуют расстоянию 0,28 нм. Измерив интенсивности рефлексов и определив фазы гармонических функций, необходимых для проведения обратного Фурье преобразования, из полного набора аналогичных дифракционных картин можно установить структуру с разрешением 0,28 нм. Для дезоксигемоглобина человека полный набор должен включать примерно 27 000 рефлексов. (С любезного разрешения А. Аrnоnе.)
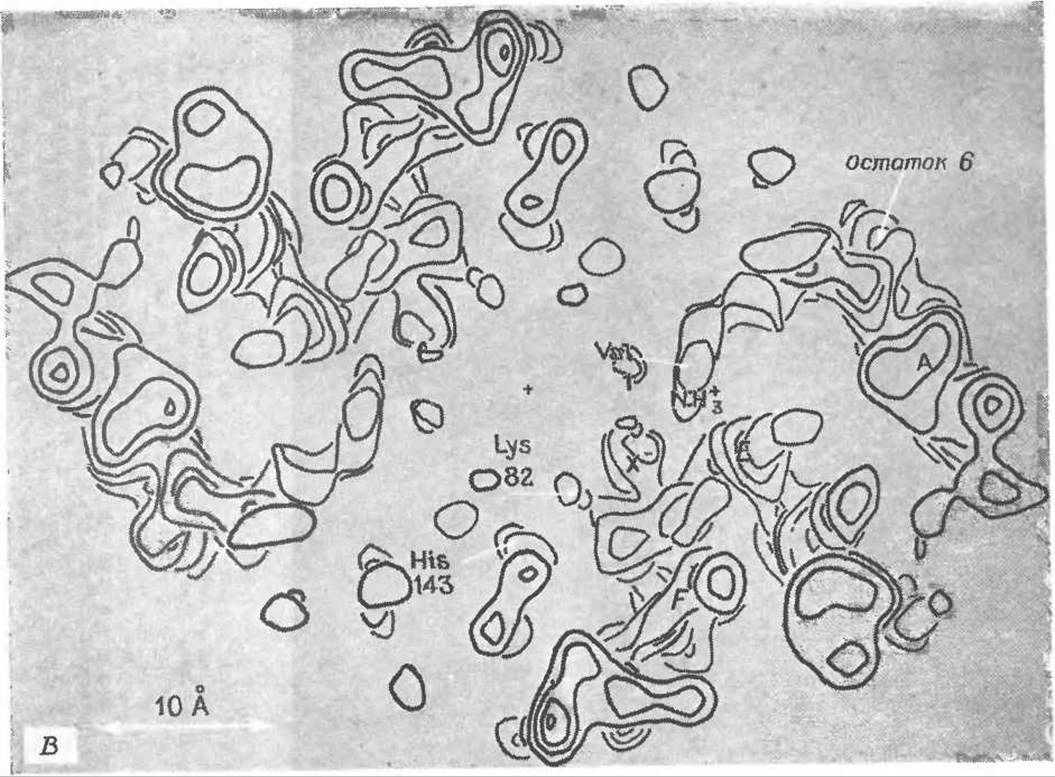
РИС. 4-19 В. Карта электронной плотности дезоксигемоглобина человека, построенная по рентгеноструктурным данным; разрешение 0,35 нм. Контурные линии указывают области высокой электронной плотности в отдельных участках молекулы гемоглобина. На этой карте показано сечение, сделанное в основном по ß-субъединицам перпендикулярно оси симметрии 2-го порядка на уровне остатка глутаминовой кислоты в 6-м положении, т. е. в месте, по которому происходит замещение в молекуле гемоглобина при серповидноклеточной анемии. Видны части спиралей А, Е и F, а также остатки Val-1, Glu-6, Lys-82 и His-143. Максимум, обозначенный через X-, соответствует неорганическому аниону, вероятно сульфату или фосфату.
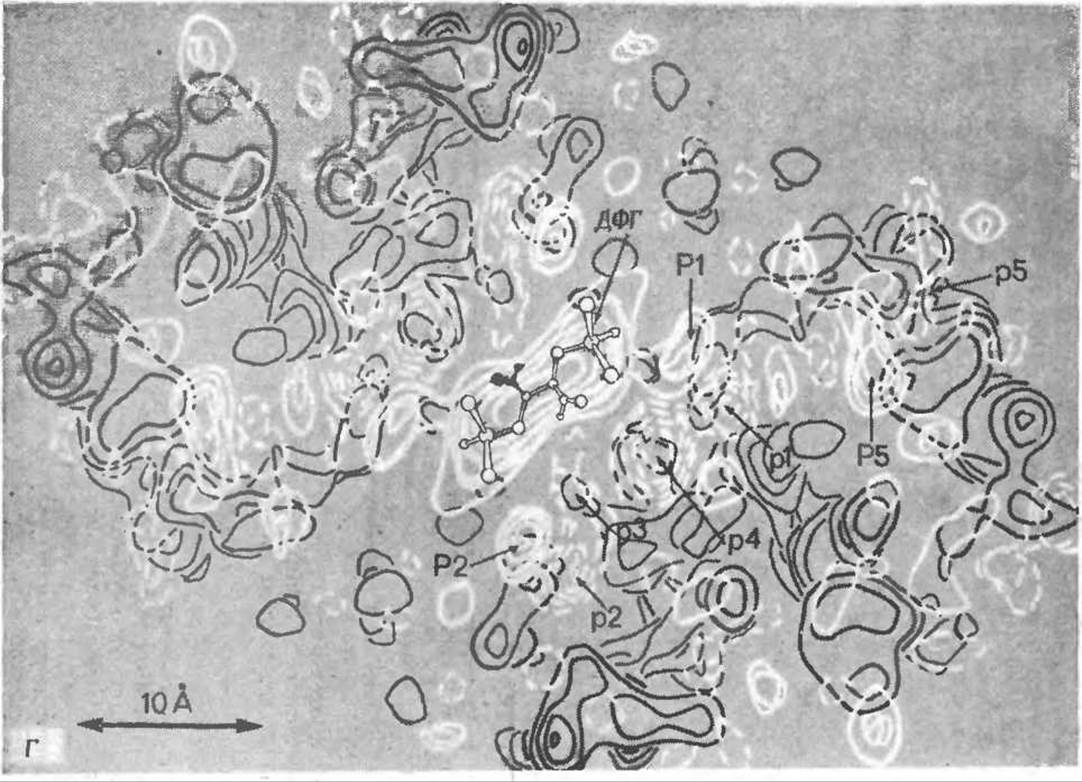
РИС. 4-19. Г. Дифференциальная карта, показывающая изменение электронной плотности при связывании гемоглобина с 2,3-дифосфоглицератом (ДФГ) (светлые контуры), наложена на карту, изображенную на рис. 4-19, В. Области, где электронная плотность увеличивается, обведены сплошными светлыми линиями и обозначены заглавными буквами, области, где электронная плотность уменьшается, обведены светлыми пунктирными линиями и обозначены прописными буквами. Молекула ДФГ с «усредненной симметрией» наложена на карту таким образом, чтобы она совпала с областью максимального увеличения электронной плотности на оси 2 го порядка Наличие двух пар областей с увеличенной и уменьшенной электронной плотностью, обозначенных через P1, p1 и Р2, р2, показывает, что при связывании гемоглобина с ДФГ N-концевые а-аминогруппы и гистидины Н-21 перемещаются внутрь структуры. Сильное уменьшение электронной плотности в области р4 указывает на то, что при связывании с ДФГ анион смещается в соседнее положение.
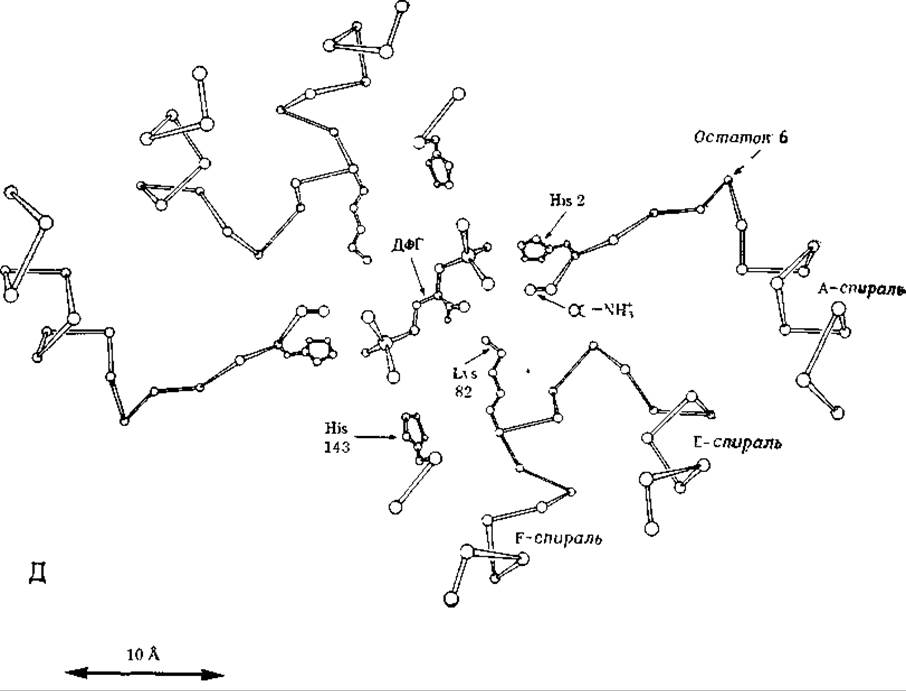
РИС. 4-19 Д. Интерпретация карт электронной плотности, представленных на рис. 4-19, В и 4-19, Г. Фосфатные группы 2,3-дифосфоглицерата образуют ионные связи с остатками валинов-1 и гистидинов-2 и 143 обеих ß-цепей и с остатком лизина-82 одной из цепей. Это связывание смещает А-спираль и остаток 6 в направлений Е-спирали, что приводит к появлению пар областей с увеличенной и уменьшенной электронной плотностью, обозначенных на рис. 4-19, Г P1, p1 и Р2, р2 [74].
б. Эффект Бора
Разрушение солевых мостиков на концах молекулы гемоглобина при оксигенации приводит к другому интересному эффекту. Значения рКа N-концевых валинов а-субъединиц и гистидинов НС-3 ß-субъединиц в дезокси-форме гемоглобина аномально высоки, поскольку остатки этих аминокислот участвуют в образовании солевых мостиков. В окси-форме эти группы не принимают участия в образовании мостиков и их рКа ниже. Если гемоглобин находится в среде с постоянным значением pH, равным 7, то при оксигенации происходит высвобождение протонов. Это явление, получившее название эффект Бора, имеет важное значение, поскольку подкисление раствора гемоглобина способствует стабилизации дезокси-формы. В капиллярах, где парциальное давление кислорода невелико и может накапливаться двуокись углерода и молочная кислота, понижение pH приводит к тому, что оксигемоглобин отдает свой кислород более эффективно.