Биохимия - Химические реакции в живой клетке Том 1 - Д. Мецлер 1980
Мембраны и клеточные оболочки
Антигены и рецепторы на поверхности клетки
Внимание многих биохимиков в настоящее время сосредоточено на вопросе о том, каким образом поверхности клеток взаимодействуют с другими биологическими объектами. На поверхности мембран, например, содержатся группировки, играющие роль антигенов. Антигены — это специфические химические структуры, которые вызывают образование антител, способных специфически связываться с ними. На поверхности эритроцита уже обнаружено около 250 различных антигенных группировок (детерминант). Эти детерминанты определяют группу крови, а аналогичные детерминанты, содержащиеся на поверхностях других клеток, определяют, будет ли отторгнута трансплантированная ткань. Различные белки из растений и из других источников действуют как агглютинины, связываясь, подобно антителам, с поверхностными группировками. Вирусы, атакующие клетки, адсорбируются на специфических поверхностных рецепторах, которые могут быть идентичны определенным антигенным детерминантам. Особенно интересно выяснить, каким образом одни клетки «решают», что другие клетки являются «чужеродными». Повышенный интерес к этой проблеме обусловлен тем, что ее решение может открыть путь к предотвращению реакций отторжения тканей и к лечению серьезных аутоиммунных заболеваний (гл. 16, разд. В.7).
Дополнение 5-Д
Кальций
Необходимость ионов кальция для живых существ впервые выявил в прошлом столетии Рингер, который установил, что для поддержания сокращений перфузируемого сердца
лягушки необходимы ионы Са2+ в концентрации ~ 1 мкМ. Позже была показана важная роль кальция при восстановлении повреждений клеточной мембраны простейших Stentor и при движении амеб. В отсутствие кальция животные быстро погибают. Исследования на сердце лягушки позволили установить, что ионы Са2+ участвуют в передаче нервного импульса с нерва на сердечную мышцу.
Подобно ионам Na+, ионы Са2+ активно выводятся из клетока,б. Основная масса кальция в организме человека содержится в костяхв-д. В сыворотке крови человека концентрация ионов Са2+ составляет 2,5 мкМ, из которых приблизительно 1,5 мкМ находится в свободной форме, а остальная часть связана с белками, углеводами и другими соединениями. Внутри клеток концентрация свободного кальция ниже. Так, например, общая концентрация ионов Са2+ в цитоплазме эритроцитов составляет около 3 мкМ, однако на свободные ионы приходится менее 1 мкМ. Градиент концентрации ионов Са2+ по разные стороны от мембраны (от 102 до 105) поддерживается при помощи кальциевого насоса. Работе насоса противодействует очень медленная обратная диффузия ионов внутрь клетки.
Характерная функция ионов Са2+ у живых существ состоит в способности активировать различные метаболические процессы. Это происходит при резких изменениях проницаемости плазматических мембран или мембран эндоплазматического ретикулума, в результате которых становится возможной диффузия ионов Са2+ в цитоплазму. Так, например, при сокращении мышцы в результате освобождения ионов Са2+ из эндоплазматического ретикулума его концентрация увеличивается приблизительно от 0,1 до 10 мкМе. Связывание ионов Са2+ с тропонином С инициирует сокращение (гл. 4, разд. Е.1)ж. Мембраны эндоплазматического ретикулума мышечного волокна содержат большое количество белка кальциевого насоса, а также ряд белков, связывающих кальций (гл. 4, разд. В.8.в)3. Один из Са2+-связывающих белков мышцы кролика, кальсеквестрин (мол. вес 46 500), способен связывать до 43 молей Са2+ на моль белкаи,к.
Другая триггерная функция кальция заключается в освобождении медиаторов из нервных окончаний (в синапсах). В большинстве случаев инициации импульса в постсинаптическом нейроне предшествует повышение концентрации ионов Са2+ в синапсе (гл. 16, разд. Б.4). Было высказано предположение, что освобождение ионов Са2+ является одним из двух основных элементов общего механизма, при помощи которого клеши реагируют на внешние раздражители. Другим элементом является освобождение циклического АМР (гл. 6, разд. Е.5)е,л,м.
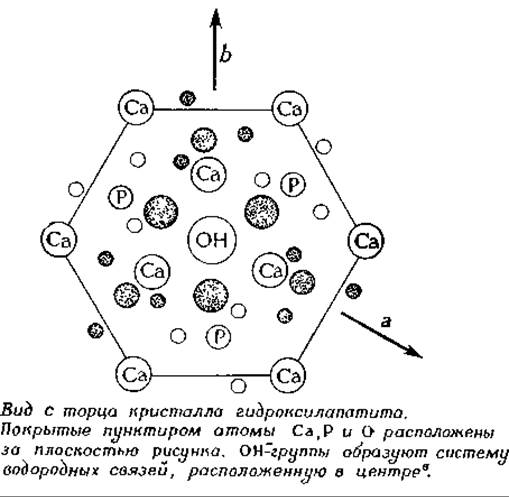
Главная роль в метаболизме кальция в организме человека принадлежит костной ткани. В состав плотного матрикса кости наряду с белком коллагеном входит фосфат кальция — кристаллическое минеральное соединение, близкое к гидроксилапатиту Са10(РО4)6(ОН)2. Часть ионов Са2+ замещена ионами Mg2+, а очень незначительная часть ионов ОН- замещена ионами фтора, которые повышают прочность кости. Внутри основного материала кости находятся остеоциты, к которым относятся, в частности, остеобласты, секретирующие вещество, из которого затем строятся волокнистые структуры, и способствующие отложению фосфата кальция. Минеральные компоненты костной ткани находятся практически в состоянии химического равновесия с ионами кальция и фосфата сыворотки крови. Клетки костной ткани могут легко ускорять либо отложение, либо растворение минеральных компонентов при локальных изменениях pH, концентрации ионов Са2+ или НРО2-4 и хелатообразующих соединений. Крупные многоядерные клетки — остеокласты — реабсорбируют кальций.
Гомеостаз ионов кальция регулируется сложным путем. Ключевые роли в этом процессе играют паратиреоидный гормон (ПТГ) и тиреоидный гормон кальцитонин. При уменьшении концентрации ионов Са2+ возрастает секреция ПТГ — пептидного гормона, содержащего 83 аминокислотных остатка. Непосредственно под влиянием этого гормона остеокласты увеличивают растворение содержащихся в костях минеральных соединений. ПТГ увеличивает также реабсорбцию ионов Са2+ в почечных канальцах. Суммарный эффект проявляется в повышении уровня кальция в сыворотке крови. В свою очередь при увеличении содержания ионов Са2+ секретируется гормон кальцитоцин, действие которого состоит в снижении концентрации ионов Са2+ засчет ускорения отложения кальция в результате деятельности остеобластов. Таким образом, эти два гормона действуют по системе «пушпул (push-pull) с обратной связью» (гл. 6, разд. Е.4). В процессе регуляции концентрации ионов кальция принимает участие также витамин D (дополнение 12-Г), который, судя по всему, требуется для синтеза Са2+-связывающих белков, необходимых для всасывания ионов Са2+ в кишечнике, реабсорбции его в почках и растворения костной ткани. Своевременное поступление нужных количеств витамина D является необходимым условием для нормального течения процессов кальцификации.
Кроме специфических Са2+-связывающих белков, ион Са2+ связывают также и другие белки. К их числу относятся ct-амилазы (гл. 7, разд. В.6), термолизин (гл. 7, разд. Г.4), стафилококковая нуклеаза (гл. 7, разд. Д.5), конканавалин А (рис. 5-7) и некоторые белки системы свертывания крови (рис. 6-16). Последние представляют особый интерес, поскольку они содержат специфические Са2+-связывающие участки, образование которых зависит от витамина К (дополнение 10-Г). Ионы кальция связываются также с различными углеводами, например с карагениновыми гелями (гл. 2, разд. В.5).
Концентрация свободных ионов кальция в тканях чрезвычайно низка, и до последнего времени не существовало надежного метода для ее количественной оценки. Сейчас в этих целях используют метод, основанный на измерении интенсивности кальций-зависимой флуоресценции белка экворина (гл. 13, разд. 3).
а Bianchi С. Р., Cell Са2+, Appleton, New York, 1968.
б Cuthbert A. W., Calcium and Cellular Function, St. Martins, New York, 1970.
в Zipkin І., ed, Biological Mineralization, Wiley, New York, 1973.
г Bourne G. H. ed., The Biochemistry and Physiology of Bone, 2nd ed., Vol. 1, Academic Press, New York, 1972
д Teo T. S., Wang J. H., JBC, 248, 5950—5955 (1973).
e Mani R. S., McCubbin W. D., Кау С. M, Biochemistry, 13, 5003—5007 (1974).
ж Rubin R. P., Calcium and the Secretory Process, Plenum, New York, 1974.
з Siegel F. L., Struct. Bonding (Berlin), 17, 221—268 (1973).
и Ostwald T. J., MacLennan D. H., JBC, 249, 974—979 (1974).
к Ostwald T. J., MacLennan D. H., Dorrington K. J., JBC, 249. 5867—5871 (1974).
л Rasmussen H., Science, 170, 404—412 (1970).
м McMahon D., Science, 185, 1012—1021 (1974).
н Dorrington K. J., Hui A., Hofmann T., Hitchman A. J. W., Harrison I. E., JBC, 249, 199—204 (1974).