Биохимия - Химические реакции в живой клетке Том 3 - Д. Мецлер 1980
Свет в биологии
Фотосинтез
Пигменты и их окружение
Хлорофиллы (рис. 13-19) по строению сходны с гемами (рис. 10-1), но кольцо IV в отличие от соответствующего ему кольца D в порфиринах неполностью дегидрировано. Кроме того, хлориновая кольцевая структура в хлорофилле модифицирована путем образования пятого кольца (V), содержащего кетонную группу и метиловый эфир. Как можно заметить, кольцо V формируется в результате образования поперечной связи между боковой цепью пропионовой кислоты кольца III и углеродом метенового мостика. Данная кольцевая система известна под названием феопорфирин. Характер заместителей по периферии кольца указывает на родство хлорофиллов и порфиринов. Однако у большинства хлорофиллов одна из карбоксиэтильных групп этерифицирована длинной фитольной цепью. Главным пигментом в хлоропластах и самым важным для фотосинтеза хромофором зеленых растений является хлорофилл а. Другие формы хлорофилла наряду с каротиноидами и некоторыми другими пигментами относятся к числу вспомогательных пигментов и рассматриваются как своего рода «светонакопители». Их относительное содержание в фотосинтезирующей единице хлоропластов шпината (разд. 4) указано в табл. 13-2.
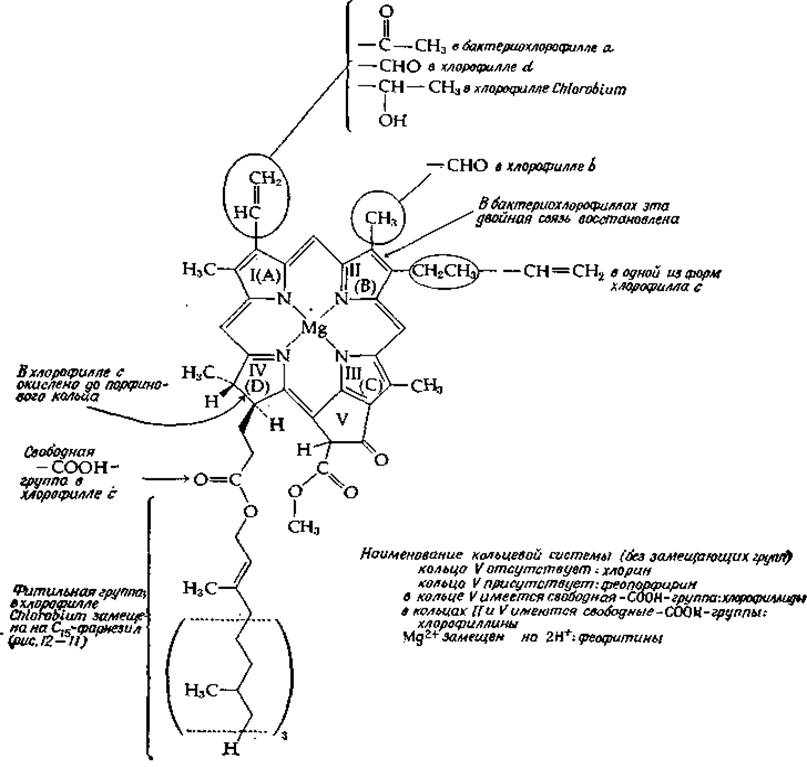
РИС. 13-19. Структурные формулы хлорофиллов.
В 80%-ном ацетоне хлорофилл а имеет интенсивную и узкую полосу поглощения с Vmах = 663 нм (15 100 см-1); у хлорофилла а в составе хлоропластов этот максимум сдвинут в красную область — основная часть хлорофилла поглощает при 678 нм. В зеленых листьях почти неизменно присутствует хлорофилл b (рис. 13-19). Максимум поглощения этого соединения в ацетоне равен 635 нм (15 800 см-1). Хлорофилл с обнаруживается у диатомей, бурых водорослей (Phaeophyta) и панцирных жгутиковых (рис. 1-7); он не содержит фитольной группы и, как полагают, является смесью двух соединений. Хлорофилл d, который наряду с хлорофиллом а присутствует в некоторых видах Rhodophyta (гл. 1, разд. Г,3), охарактеризован лишь частично [77].
Таблица 13-2 Приблизительный состав «усредненной» фотосинтезирующей единицы хлоропластов шпинатаа,б
|
Компонент |
Число молекул |
|
Хлорофилл а |
160 |
|
Хлорофилл b |
70 |
|
Каротиноиды |
48 |
|
Пластохинон А |
16 |
|
Пластохиион В |
8 |
|
Пластохинон С |
4 |
|
а-Токоферол |
10 |
|
а-Токоферилхинон |
4 |
|
Витамин К |
4 |
|
Фосфолипиды |
116 |
|
Сульфолипиды |
48 |
|
Галактозилглицериды |
490 |
|
Железо |
12 атомов |
|
Ферредоксин |
5 |
|
Цитохром b563 |
1 |
|
Цитохром b559 |
|
|
Цитохром f |
1 |
|
Медь |
6 атомов |
|
Пластоцианин |
1 |
|
Марганец |
2 атома |
|
Белок |
928 000 дальтон |
а Из монографии Грегори [77] [по данным статьи Luchtenthaler Н. К., Park R. В., Nature (London), 198, 1070 (1963)] и книги White A., Handler Р., Smith Е. L., Principles of Biochemistry, 5th ed., p. 528, McGraw-Hill, New York, 1973.
б Число молекул рассчитано исходя из допущения, что каждая единица содержит два нона Мn2+.
Фотосинтезирующие бактерии содержат бактериохлорофиллы, у которых восстановлено кольцо II (рис. 13-19). Полоса поглощения этих соединений сдвинута относительно полосы поглощения хлорофилла а в красную сторону до ∼770 нм. Основной хлорофилл зеленых серных бактерий Chlorobium — хлоробиум-хлорофилл — имеет оксиэтильную и фарнезильную боковые цепи. К числу производных хлорофилла относятся феофитины, образующиеся в результате удаления Mg2+ при обработке хлорофилла слабой кислотой. В результате гидролиза сложноэфирной метильной группы образуются хлорофиллы, а при одновременном удалении метильной и фитильной групп — хлорофиллины.
Поскольку хлорофиллы легко и полностью экстрагируются мягкими растворителями [81], можно подумать, что они попросту растворены в липидном компоненте мембран. Однако в спектре поглощения хлорофилла в листьях присутствуют полосы, сдвинутые в красную сторону относительно их положения в спектре хлорофилла а в ацетоне, причем величина сдвига достигает 900 см-1. В большинстве зеленых растений хлорофилл имеет по меньшей мере четыре основные полосы с λmах = 662 нм (15 120 см-1), 670 нм (14940 см-1), 677 нм (14770 см-1) и 83 нм (14 630 см-1) [82]. Иногда наблюдаются также минорные полосы с vmax = 14 420 и 14 230 см-1 (рис. 13-20). Отсюда можно сделать вывод, что молекулы хлорофилла внутри мембран находятся в разном окружении. В результате спектр поглощения становится шире, способствуя более эффективному улавливанию света. Считается, что в реакционных центрах тоже имеется хлорофилл; в фотосинтезирующей системе I он поглощает при ~700 нм (14 290 см-1), а в фотосистеме II — при ~682 нм (14 660 см-1).
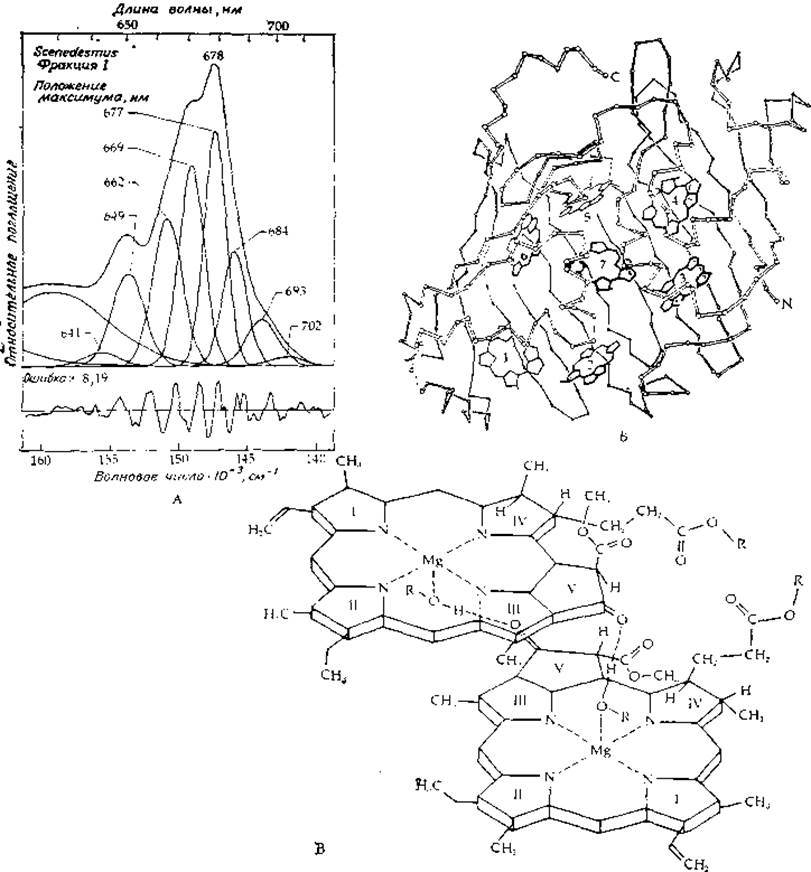
РИС. 13-20. А. Анализ спектра поглощения хлорофилла в суспензии хлоропластных фрагментов из Scenedesmus [82]. Б. Схематическое представление пространственной конфигурации полипептидного остова и расположения молекул хлорофилла в одной субъединице бактериохлорофиллсодержащего белка [Ferma R. Е., Matthews В. W., Nature (London), 258, 573—577 (1975)]. Кружочками указаны предполагаемые положения атомов а-углерода. Ход полипептидиой цепи в нескольких местах остается неопределенным (пунктирная линия). Чтобы не загромождать рисунок, атомы магния, заместители в кольце хлорофилла и фитольные цепи (за исключением первой) не указаны. В. Предполагаемое расположение пары молекул хлорофилла а в реакционных центрах [93а]. R — фитол; R'— атом Н молекулы воды или аминокислотного остатка белка.
Бактериохлорофилл, содержащийся в клетках Chromatium, тоже имеет три полосы поглощения с λmах = 800, 850 и 890 нм. Последняя полоса соответствует бактериохлорофиллу реакционного центра — единственной из форм, которая флуоресцирует. Водорастворимый бактериохлорофиллсодержащий белок, выделенный из зеленых фотосинтезирующих бактерий Chlorobium, удалось получить в кристаллическом виде. Расшифровка трехмерной структуры этого белка с помощью рентгеновской кристаллографии [83] показала, что каждая из субъединиц (с мол. весом 50 000) тримерной молекулы содержит семь встроенных молекул бактериохлорофилла, как это показано на рис. 13-20,5. В зеленых растениях хлорофилл может присутствовать также в комплексе с более гидрофобными белками. Было выделено два таких комплекса [84], один из которых предположительно принадлежит фотосистеме I, а другой — фотосистеме II.
Облучение хлоропластов вызывает легко измеряемую флуоресценцию хлорофилла а, в то время как хлорофилл b и другие формы хлорофилла, а также каротиноиды и прочие пигменты совершенно не флуоресцируют. Отсюда следует, что все они служат вспомогательными пигментами, эффективно передающими энергию хлорофиллу а, который находится в реакционном центре. Как видно из рис. 13-21, полосы поглощения вспомогательных пигментов лежат обычно в области более высоких энергий, чем полосы поглощения реакционных центров. Таким образом, фотосинтезирующий организм поглощает свет в широком диапазоне длин волн, и вся поглощенная энергия поступает далее в реакционные центры.
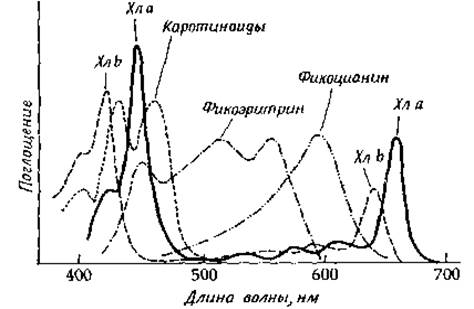
РИС. 13-21. Спектры поглощения хлорофиллов и вспомогательных пигментов [Govindjee G. and R., Sci. Am., 231, 68—82 (Dec. 1974)].
К наиболее важным вспомогательным пигментам относятся каротины (рис. 12-14), из которых главным в большинстве зеленых растений является ß-каротин. Зеленые серные бактерии содержат у-каротин; один из концов молекулы этого соединения не подвергается циклизации и напоминает ликопен. Хлоропласт содержат разнообразные оксигенированные каротиноиды (ксантофиллы). Из них в высших растениях и зеленых водорослях преобладают неоксантин, виолаксантин [уравнение (12-30)] и лютеин. Лютеин напоминает зеаксантин, но на одном из концов цепи кольцо изомеризуется путем перемещения двойной связи в положение, показанное ниже:
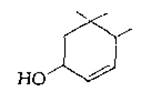
Эвглена и родственные ей микроорганизмы содержат в больших количествах антераксантин (разд. Д, 7), тогда как в бурых водорослях и диатомеях преобладают фукоксантин и зеаксантин (рис. 12-14). Пурпурные серные бактерии Rhodospirillum rubrum синтезируют особый спириллоксантин; на обоих концах молекулы этого соединения имеется представленная ниже структура:
Еще один класс вспомогательных пигментов, распространенных менее широко, составляют тетрапирролы с открытой цепью [85]; из-за структурного родства с пигментами желчи (рис. 14-14) их часто называют «растительными желчными пигментами». Фикоцианины придают характерный цвет сине-зеленым водорослям. Они образуют группу конъюгированных белков (билипротеидов), содержащих в качестве связанного с ними пигмента фикоцианобилин (рис. 13-22). Подобным же образом красные фикоэритрины из Rhodophyta содержат связанный фикоэритробилин (рис. 13-22). Хотя эти пигменты иногда называют линейными тетрапирролами, не исключено, что на самом деле их молекулы уложены в виде спирали (рис. 13-22). Билипротеиды водорослей (фикоцианины и фикоэритрины), по-видимому, агрегируют и образуют особые гранулы, находящиеся с наружной стороны фотосинтезирующих мембран. В сине-зеленых водорослях эти гранулы называют фикобилисомами.
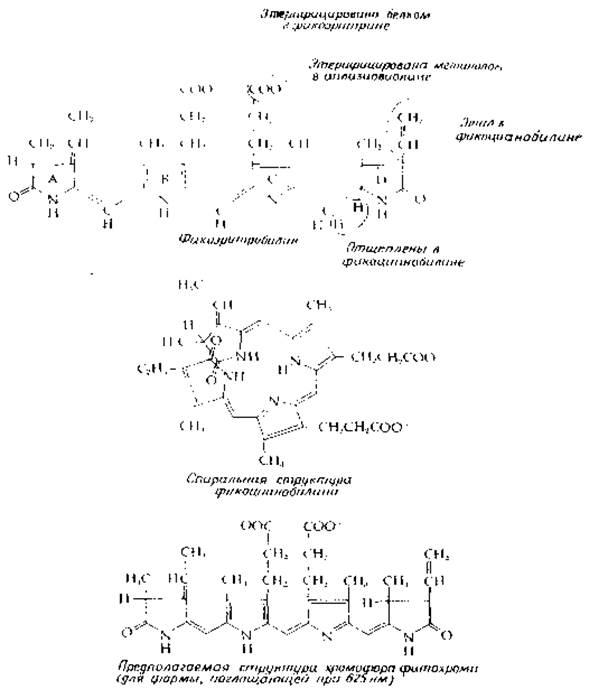
РИС. 13-22. Структура тетрапирролов с открытой цепью, присутствующих в растениях (см. также рис. 14-14).