Биохимия - Химические реакции в живой клетке Том 3 - Д. Мецлер 1980
Метаболизм азотсодержащих соединений
Фиксация N2 и другие превращения неорганических соединений азота
Механизм восстановления
Хотя N2 очень инертен, он тем не менее образует нитриды с металлами и комплексы с некоторыми хелатами металлов. Эти комплексы обычно носят «торцевой» характер, например N ≡ N—Fe. Штифель [12] предположил, что N2 сначала образует комплекс такого типа с атомом железа в молекуле молибдоферредоксина. Затем атом Mo(IV) может отдать два электрона на N2 [уравнение (14-9), стадия а]:
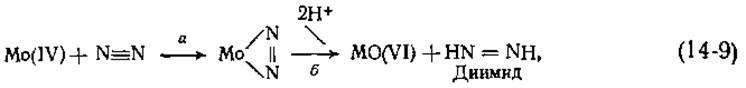
что приведет к образованию комплекса N2 с Mo(VI). Присоединение двух протонов [уравнение (14-9), стадия б] дает молекулу динмида, которая остается связанной с железом, пока молибден не пройдет второй тур восстановления. Далее динмид восстанавливается в гидразин я в конечном итоге в аммиак:
![]()
Как указал Штифель, Mo(VI) притягивает электроны настолько сильно, что протоны, связанные с окружающими молибден лигандами, например с Н2О, полностью диссоциируются. Так образуется непротонированный молибдат-ион МоО2-4. То же будет справедливо и в отношении азотистых лигандов, таких, как аминогруппы белка, которые могут быть координационно связаны с находящимся на белке молибденом. Напротив, восстановленный Mo(IV) стремится окружить себя протонированными лигандами. В первоначальном комплексе с N2 Mo(IV) может быть связан с протонированными азотистыми лигандами. Перенос этих протонов на молекулу N2 может сопутствовать переносу на N2 электронов от молибдена.
В полном соответствии с этим предположением в присутствии 2Н2О из ацетилена образуется исключительно цис-дидейтероэтилен.
![]()
Лихтенштейн и сотр. [13] предположили, что молекула N2 связывается между двумя молибденовыми центрами и получает электроны от обеих половин димерной структуры (рис. 14-1).
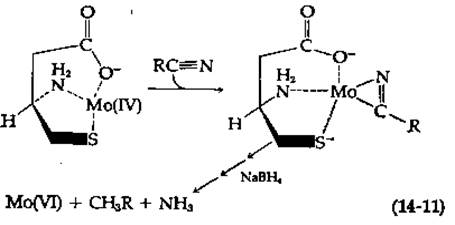
Ввиду огромного практического значения для сельского хозяйства очень большой интерес представляла бы разработка более эффективных неферментативных процессов фиксации азота. Предпринимались многочисленные попытки создать модель нитрогеназы, имитирующую природный биологический фермент. Например, смесь цистеина и молибдата натрия в отношении 1 : 1 обрабатывали таким восстанавливающим агентом, как NaBH4, считая, что в результате должен образоваться комплекс, содержащий Mo(IV). Этот комплекс должен был координационно связывать алкилнитрилы, способные восстанавливаться под действием NaBH4 на всех стадиях вплоть до алкена и аммиака [уравнение (14-11)].
Само собой разумеется, что эта реакция должна проходить в несколько стадий. Интересно, что ее скорость значительно увеличивается в присутствии АТР и соединений, содержащих железо-серный кластер; присутствие СО или N2 ингибирует реакцию [14, 15]. Таким образом, использованная модельная система по целому ряду признаков обнаруживает замечательное сходство с нитрогеназами. Сообщалось еще об одной модельной системе, в которой для восстановления N2 использовали несколько иной молибденовый комплекс н другой железо-серный кластер [16]. Однако для всех этих модельных систем скорости реакций оказываются значительно ниже тех скоростей, которые наблюдаются при использовании самой нитрогеназы.
Большой интерес представляют также попытки повысить эффективность биологической фиксации азота. Например, с помощью различных генетических манипуляций можно вызвать дерепрессию генов нитрогеназы. В результате выражение этих генов становится «конститутивным» (гл. 15, разд. Б, 1), а это дает возможность получать бактерии, способные фиксировать азот в почве или в клубеньках значительно быстрее, чем это делают природные штаммы. Обычно гены нитрогеназы репрессируются при накоплении в клетках глутамина, о чем подробнее говорится в разд. Б, 2. Гены азотфиксации обнаружены только в прокариотах. Важным достижением в области сельского хозяйства явилось бы осуществление переноса этих генов (с сохранением их функциональной активности) в зеленые растения (гл. 15, разд. 3, 4).