Биохимия - Химические реакции в живой клетке Том 3 - Д. Мецлер 1980
Метаболизм азотсодержащих соединений
Фолиевая кислота, флавины и диметилбензимидазол
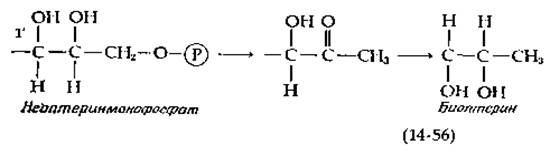
Опыты с использованием изотопных меток показали, что и рибофлавин и фолиевая кислота происходят от одного из производных гуанозина. В продукте сохраняются все атомы пуринового кольца, за исключением атома С-8 пятичленного кольца. На рис. 14-34 показаны гипотетические пути, начинающиеся от гуанозинтрифосфата, который служит исходным соединением по крайней мере у некоторых организмов. Первая стадия, воспроизведенная в опытах с бесклеточными ферментными системами, способными синтезировать птерины, сводится к гидролитическому отщеплению формиата. Далее следует перегруппировка Амадори, продукт которой подвергается простому замыканию цикла между карбонилом и соседней аминогруппой [158—162]. В результате образуется дигидронеоптеринтрифосфат (гл. 8, разд. Л), обозначенный на рис. 14-34 буквой X. В его молекуле имеется боковая цепь, показанная в уравнении (14-56). Вслед за альдольным расщеплением протекает серия реакций (рис. 14-34), ведущих прямо к образованию фолатных коферментов. Образование других птеринов может происходить путем простых модификаций. Например, биоптерин может быть образован из неоптеринфосфата в результате элиминирования фосфата, кетонизации и восстановления [уравнение (14-56)]. Как инверсия при атоме С-1', указанная в этом уравнении, так и промежуточное образование сепиаптерина (гл. 8, разд. Л), содержащего 3'-карбонильную группу, свидетельствуют о промежуточной реакции дегидрирования с образованием С-1'-карбонила, предшествующей элиминированию фосфата.
Пути синтеза рибофлавина схематически показаны на рис. 14-34; они установлены в результате исследований, выполненных на грибе Еrеmothecium (дополнение 8-3) и на мутантах Saccharomyces [163—165]. Восстановление продукта перегруппировки Амадори (на рис. 14-34 этот продукт показан в виде трифосфата, однако не известно, так ли это на самом деле)1), дезаминирование и дефосфорилирование приводят к образованию предшественника флавина, 4-рибитиламин-5-амин-2,6-диоксипиримидина. Дополнительные атомы углерода, необходимые для построения бензольного ядра рибофлавина, поступают в две стадии. Хотя это точно не установлено, но есть основания считать, что эти атомы поставляет пируват после его превращения в ацетоин [уравнение (9-28)] или диацетил.
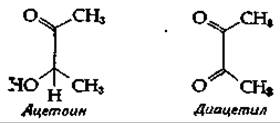
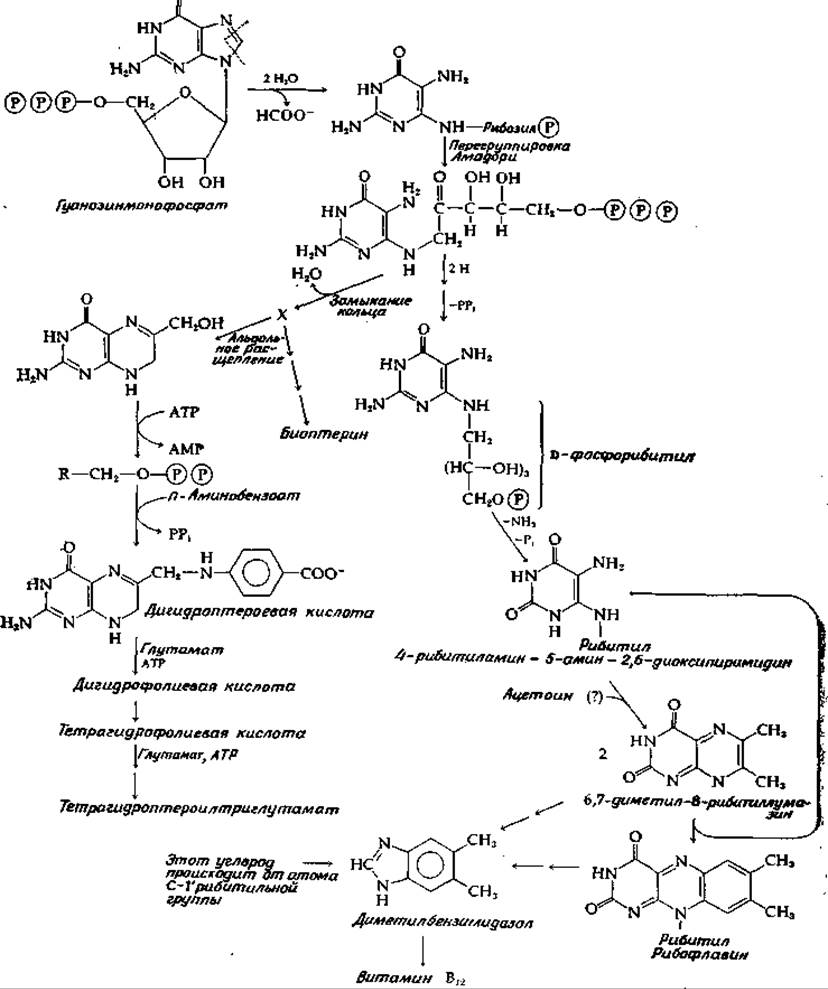
РИС. 14-34. Биосинтез фолиевой кислоты, рибофлавина и диметилбензимидазольной группы витамина В12.
1) По данным, полученным недавно в работе с мутантом Salmonella, прямым предшественнком рибофлавина служит не трифосфат, показанный на рис. 14-34, а гуанозия [165а].
В результате спонтанного соединения диацетила с диаминовым предшественником образуются 6,7-диметил-8-рибитиллумазин. Для завершения построения флавинового кольца требуются еще четыре атома углерода, которые доставляются второй молекулой диацетила. Это происходит не прямо, а путем переноса диацетильного остатка от второй молекулы 6,7-диметил-8-рибнтиллумазина, как показано на рис. 14-34. Реакция на первый взгляд кажется весьма примечательной, но впечатление оказывается менее разительным, если принять во внимание, что эта бимолекулярная реакция протекает спонтанно в мягких условиях. Однако ферментативный процесс, изученный Плаутом, может идти несколько иначе, чем неферментативная реакция. Были предложены детальные механизмы этого процесса, который сопровождается регенерацией предшественника (4-рибитиламин-5-амин-2,6-диоксиметилпиримидина), содержащего две аминогруппы.
Из 6,7-диметил-8-рибитиллумазина может также быть получен диметилбензимидазол в результате процесса, сходного с процессом синтеза рибофлавина, но при этом образовавшийся рибофлавин распадается, гидролитически с удалением пиримидинового цикла и образованием имидазольного ядра [166]. Не исключено также, что таким путем реагирует свободный рибофлавин, составляющий отдельный фонд.
Вопросы и задачи
1. Можете ли вы прокомментировать (с указанием механизма) следующее наблюдение: нитрогеназа восстанавливает ацетилен в этилен, но не восстанавливает этилен в этан, однако циклопропен восстанавливается в смесь циклопропана и пропена? [см. McKenna С. Е., McKenna М, Higa М. Т., JACS, 98, 4657—4659 (1976)].
2. В настоящее время возник интерес к выведению азотфиксирующих бактерий с повышенной активностью гидрогеназы. Последняя может окислять Н2 в Н+. Объясните, почему это могло бы привести к более высокой эффективности фиксации азота в корневых клубеньках бобовых [см. Dixon R. О. D., Nature (London), 262, 173 (1976)].
3. Проследите пути, благодаря которым некоторые бактерии могут превращать: a) N2 в атом азота глутаминовой кислоты и глутамина; б) NO3 в атом азота аланина; в) N глутаминовой кислоты в N порфобилиногена; г) N глутамина в N адениловой кислоты; д) N аспарагиновой кислоты в N лизина.
4. Какие 10 аминокислот должны обязательно входить в рацион крыс? Какие аминокислоты являются незаменимыми для человека?
5. Что подразумевается под термином «баланс азота»? В какой мере это понятие может быть использовано при изучении вопросов питания?
6. Предложите путь биосинтеза тропина, компонента алкалоидов вонючего дурмана Datura. Исходным соединением служат глутаминовая кислота (превращающаяся сначала в орнитин) и ацетоацетат.
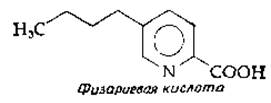
7. Предложите подробную схему биосинтеза фузариевой кислоты, продукта одного из видов грибов ряда Fusarium, начиная с аспартата и ацетил-СоА.
8. Предложите путь метаболического превращения треонина в глицин и ацетил-СоА. Этот путь, по-видимому, используется многими бактериями для разрушения треонина [см. Bell S. С., Turner J. М., Bioсhern. Soc. Trans., 4, 497—500 (1976)].
9. Хотя HCN высоко токсичен для большинства организмов, многие высшие растения могут использовать HCN в процессах биосинтеза. Предложите пути превращения серина и HCN в аспарагин и а,у-диаминомасляную кислоту. Предложите путь синтеза в грибах аланина из ацетальдегида, HCN и аммиака. (Примечание: соответствующей неферментативной реакцией является хорошо известный синтез аминокислот путем реакции Штрекера.)
10. Кетопантоат-оксиметилаза E.coli представляет собой фермент, катализирующий первый «сопричастный» этап биосинтеза пантотеновой кислоты (см. рис. 14-10); фермент не инактивируется боргидридом в присутствии избытка субстрата и активируется ионами Mg2+. Как бы вы классифицировали этот фермент в соответствии со схемой, предложенной в гл. 7? [см. Powers S. G., Snell Е. Е., JBC, 251, 3786—3793 (1976)].
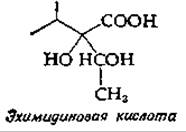
11. Предложите путь биосинтеза эхимидиновой кислоты, продукта некоторых растений из семейства Borraginaceae.
12. Напишите структурную формулу протопорфирина IX. а) Отметьте звездочками все атомы углерода и кружками все атомы азота, непосредственными источниками которых служат углеродный атом карбоксилатной группы и азот аминогруппы глицина, б) От каких предшественников произошли остальные атомы? в) Какой дополнительный предшественник передает атомы непосредственно в состав молекулы хлорофилла? г) Дайте ответ на такой же вопрос в отношении витамина В12.
13. Некоторые растения («цианогенные растения»), такие, как Prunus amygdalis и Sorghum, используют цианид, превращая его в цианогенные гликозиды, такие, как амигдалин (рис. 14-23). Считается, что помимо путей биосинтеза, показанных на рисунке, эти гликозиды могут образовываться из соответствующих аминокислот следующим образом: аминогруппа гидроксилируется с образованием N-оксиаминокислоты, которая может быть дегидрирована в оксим. Последний может быть превращен в нитрат и (после еще одной стадии гидро- ксилирования) в гликозид.
Недавно предложен новый цикл углерод — азот [Thatcher R. Т., Weaver Т. L., Science, 192, 1234—1235 (1976)]. Этот цикл функционирует у всех цианогенных растений, гриба, превращающего цианид в формамид, псевдомонад и нитрифицирующих организмов Niirosomonas и Nitrobacter. Предложите схему предлагаемого цикла и рассмотрите химию отдельных реакций.
14. Опишите два главных пути биосинтеза ароматических соединений. Каким путем, по вашему мнению, могло бы синтезироваться следующее соединение?
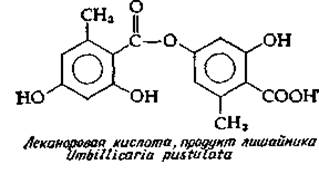
15. Галловая кислота может образовываться в растениях в реакциях пути шикимовой кислоты (разд. 3,6), но, кроме того, она может быть синтезирована в грибах через поликетидный путь. Предложите подробную схему этого метаболического пути.
16. Предложите трехстадийный путь образования салициловой кислоты (о-оксибензойной кислоты) из хоризмовой кислоты.
17. Предложите детальный механизм, используемый на стадии г (рис. 14-31), который заключается в глутамин- и АТР-зависимом аминировании формилглицинамидриботида. Есть основания думать, что эта реакция катализируется единственным ферментом.