Химия белка. Структура, свойства, методы исследования - Шендрик А.Н. 2022
Аминокислоты
Аминокислоты
Стереоизомерия аминокислот
Все, за исключением глицина, а-аминокислоты имеют хиральный атом углерода (атом с четырьмя различными заместителями). Эта структурная особенность аминокислот обуславливает реальное существование их в двух различных стереоизомерных формах. Они (формы) отличаются друг от друга различной пространственной ориентацией заместителей при а-углеродном атоме. В ряду наиболее распространенных 20 белковых аминокислот треонин и изолейцин имеют по два асимметричных атома углерода.
Соединения с хиральным атомом углерода подразделяются на два энантиомера, которые обозначаются как L- и D-стереоизомеры. Эти изомеры можно рассматривать как две несовместимые в пространстве конформации, которые в паре составляют зеркальное отражение одна - другой. В качестве стандарта для отнесения энантиомеров оптически активных соединений к L- или D-ряду выбраны стереоизомеры глицеральдегида.
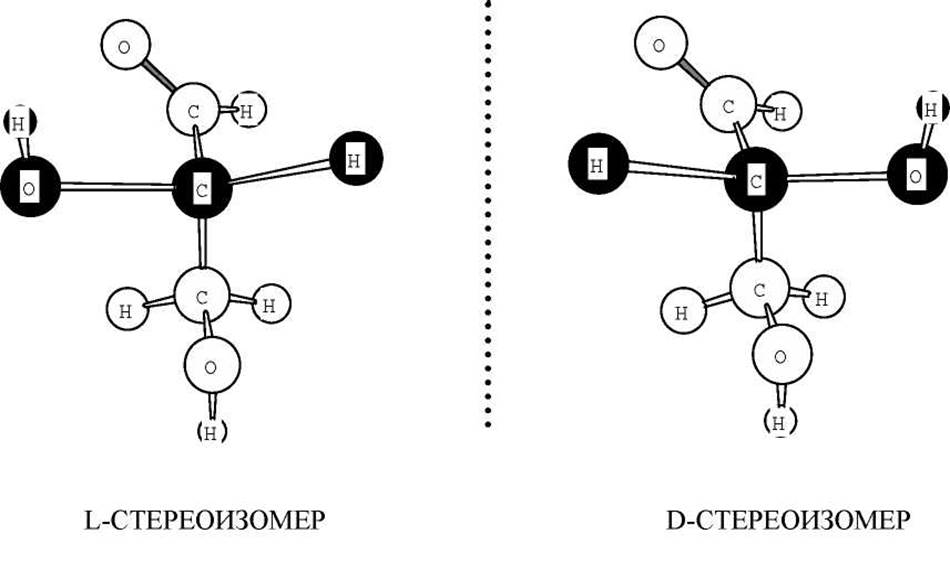
Энантиомеры глицеральдегида разделены на L- и D-стереоизомеры по следующему формальному признаку. Если молекула альдегида занимает в пространстве такое положение, что группы -СНО и -СН2ОН расположены за плоскостью рисунка и направлены вверх и вниз соответственно, а заместители -Н и -ОН расположены над плоскостью рисунка, то группа -ОН в L- изомере направлена влево, а D - вправо.
L- и D-энантиомеры не следует путать с оптическими антиподами, которые различаются между собой направлением (левовращающие, правовращающие) и величиной угла вращения плоскости поляризации света. L- и D- Энантиомеры могут быть как лево- так и правовращающими. Величины удельного вращения некоторых L- и D-аминокислот в воде при рН=7 (облучающий свет: D-линия натрия при λ = 5461 Å) приведены ниже:
L-аланин |
+1.8 |
L-серин |
-7.5 |
L-лейцин |
-11.0 |
L-пролин |
-86.2 |
L-изолейцин |
+12.4 |
L-триптофан |
-33.7 |
L-фенилалинин |
-34.5 |
D-аланин |
-1.8 |
L-глутаминовая кислота |
+12.0 |
D-глутаминовая кислота |
-12.0 |
L-аспаригиновая кислота |
+5.0 |
D-лизин |
-13.5 |
Величина удельного вращения аминокислоты зависит от рН-среды и максимальна в изоэлектрической точке.
Таким образом, L- и D-стереоизомеры характеризуют абсолютную конформацию молекулы в пространстве, а оптическая активность является лишь признаком наличия хирального атома углерода в молекуле, и направление вращения плоскости поляризации света не несет информации о принадлежности стереоизомера к L- или D-ряду. Поэтому, направление вращения плоскости поляризации обозначают малыми латинскими буквами l и d, т. е. вращающие влево и вправо соответственно.
В состав белков входят только L-аминокислоты:
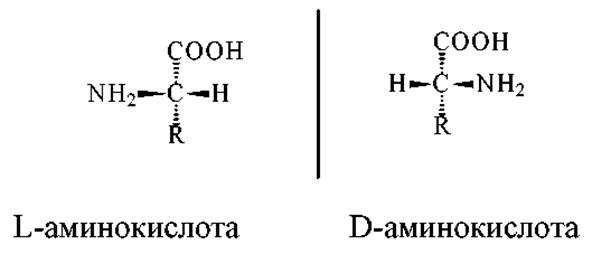
При изображении структурной формулы стереоизомеров принято общее правило: направление связи в пространстве обозначается сектором (треугольником)-
![]()
Относительно плоскости рисунка:
![]()
До настоящего времени неизвестно ни одного случая вхождения в белковые молекулы D-аминокислот. В свободном состоянии и в качестве компонентов небелковых структур D-аминокислоты встречаются в клетках живых организмов и выделены из различных источников, в том числе и из организма человека. В качестве примера можно привести вещество клеточной стенки бактерий - это тетрапептид: L-ala - D-glu - L-lys - D-ala, и пептидные антибиотики: бацитрацин А, который синтезируется штаммами бактерии “Bacilus licheniformis” и грамицидин S, выделяемых Bacilus brevis (где orn = (NH2)CООHCH(CH2)3NH2) - -орнитин:
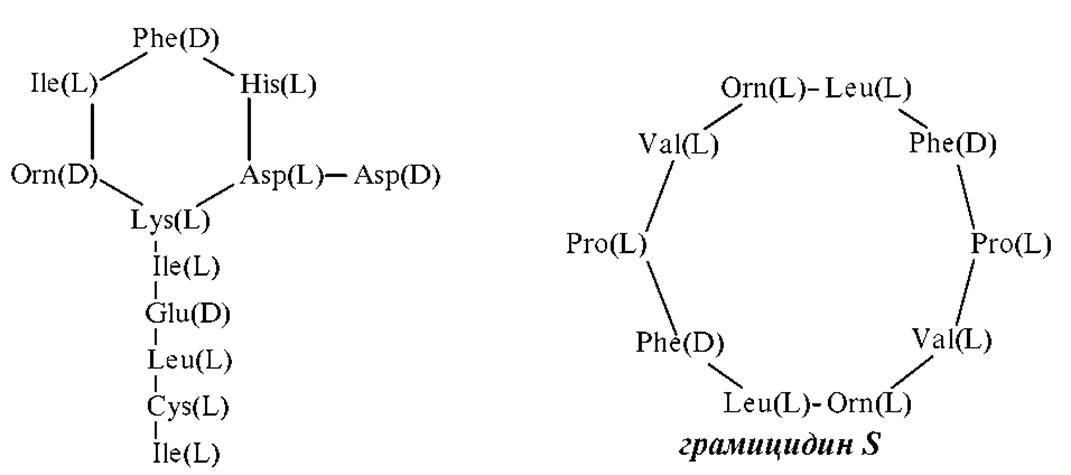
Процесс перехода аминокислот из L- в D-форму и наоборот называется рацемизацией. При этом, равновесие L ↔ D in vivo смещено в сторону L-формы. После гибели организма процесс рацемизации протекает самопроизвольно и завершается установлением неметаболического (термодинамического) состояния равновесия. Время достижения такого равновесия может быть большим и составляет иногда десятки тысяч лет, что находит практическое применение. Например, измерение соотношения D/L-энантиомеров аспарагиновой кислоты в образцах окаменелых костей положены в основу нового метода датирования. Он хорошо дополняет другие методы, например радиоуглеродный.
Установлено также, что повышение D/L-отношения для аспарагиновой кислоты в зубах животных хорошо коррелирует с их биологическим возрастом. Измерения выполнены на зубах потому, что белки зубных тканей (эмаль, дентин) не регенерируются в течении жизни.
Аминокислоты с двумя хиральными атомами углерода могут существовать в четырех стереоизомерных формах. Для треонина все они обнаружены. Ту форму треонина, которую выделяют из гидролизатов белков условно называют L-формой, а ее зеркальное отражение - D-формой.
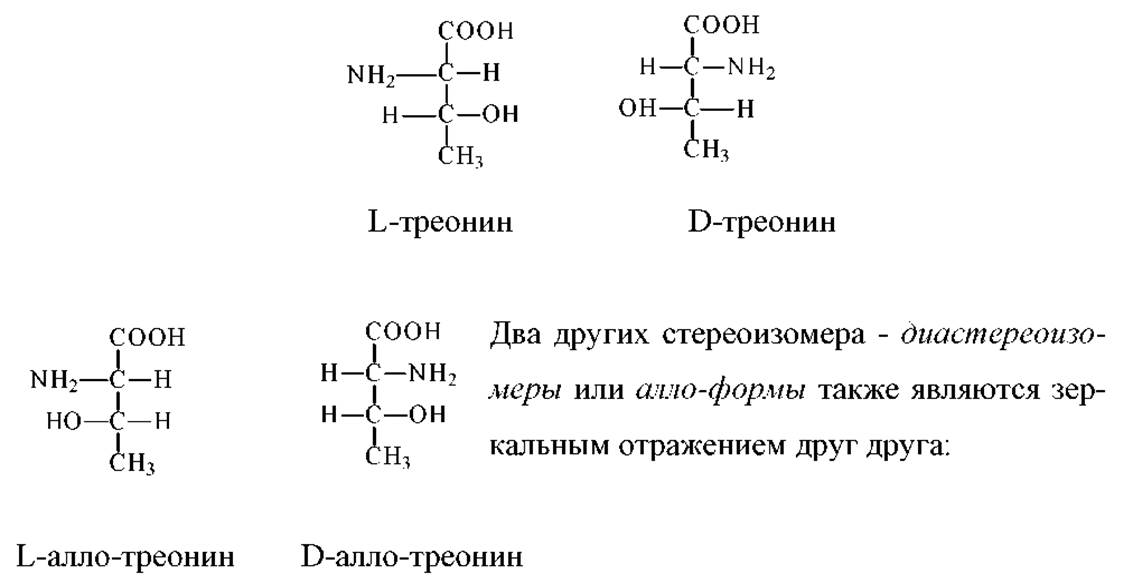
В аминокислотах с двумя хиральными атомами отнесение к L- или D- ряду проводят по положению заместителей при а-углеродном атоме.