БИОХИМИЯ - Л. Страйер - 1984
ТОМ 1
ЧАСТЬ I. КОНФОРМАЦИЯ И ДИНАМИКА
ГЛАВА 6. ВВЕДЕНИЕ В ЭНЗИМОЛОГИЮ
6.8. Некоторые свойства активных центров
Активный центр фермента - это участок, который связывает субстраты (и простетическую группу, если она есть) и в котором содержатся аминокислотные остатки, непосредственно участвующие в образовании или разрыве химических связей. Такие остатки называют каталитическими группами. Несмотря на огромное разнообразие структуры ферментов, их специфичности и механизма каталитического действия, все же можно сделать ряд обобщений в отношении свойств активных центров.
1. На активный центр приходится относительно малая часть общего объема фермента. Большая часть аминокислотных остатков в молекуле фермента не контактирует с субстратом. Остается загадкой, почему размер ферментов так велик. Почти все ферменты содержат более 100 аминокислотных остатков и имеют массу свыше 10 к Да, а диаметр-свыше 25 А.
2. Активный центр - трехмерное образование. Другими словами, это не точка, не линия и даже не плоскость, а сложная трехмерная структура, в формировании которой участвуют группы, принадлежащие разным частям линейной последовательности аминокислот. Действительно, как мы уже видели на примере гемоглобина и миоглобина, взаимодействие между аминокислотными остатками, расположенными далеко друг от друга в линейной последовательности, нередко сильнее, чем взаимодействие между соседними (в последовательности) остатками аминокислот. В лизоциме - ферменте, который мы рассмотрим подробно в следующей главе, основные группы активного центра представлены аминокислотными остатками, занимающими 35, 52, 62, 63 и 101-е положения в линейной последовательности из 129 аминокислот.
3. Субстраты относительно слабо связываются с ферментами. Константы равновесия Е8-комплексов обычно лежат в пределах от 10-2 до 10-8 М, что соответствует свободным энергиям взаимодействия от — 3 до — 12 ккал/моль. Сравним эти величины с силой ковалентных связей, составляющей от — 50 до — 110 ккал/моль.
4. Активный центр имеет форму узкого углубления или щели. Во всех ферментах с изученной структурой связывание субстратов происходит в таком углублении или щели, куда нет доступа воде, за исключением тех случаев, когда вода является одним из реагирующих веществ. В этом углублении присутствует несколько полярных аминокислотных остатков, необходимых для связывания и катализа. Неполярный характер всей области в целом способствует связыванию субстрата. Кроме того, щелевидная форма активного центра создает микроокружение, в котором отдельные полярные остатки приобретают особые свойства, существенно важные для катализа.
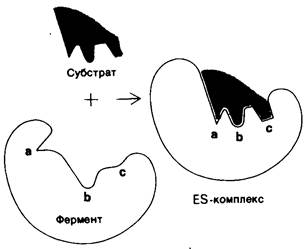
5. Специфичность связывания зависит от строго определенного расположения атомов в активном центре. Субстрат входит в активный центр, только если он соответствует ему по форме. В 1890 г. Эмиль Фишер (Е. Fischer) использовал сравнение с ключом и замком (рис. 6.10), которое оказалось по существу правильным и исключительно плодотворным представлением о стереоспецифичности катализа. Однако, как показывают работы последних лет, активные центры некоторых ферментов не являются жесткой структурой, их форма модифицируется при связывании субстратов. В этих ферментах форма активного центра становится комплементарной форме субстрата с ферментами, согласно модели, индуцированного соответсвия. При связывании субстрата происходит изменение формы фермента. Активный центр фермента только после присоединения субстрата становится комплементарным ему по форме только после связывания субстрата. Такой процесс динамического узнавания называют индукцией соответствия (рис. 6.11). Кроме того, некоторые ферменты предпочтительно связывают субстрат в напряженной («искаженной») форме, соответствующей переходному состоянию.
Рис. 6.10. Взаимодействие субстратов с ферментами согласно модели ключ-замок. Активный центр фермента сам по себе комплементарен по форме субстрату
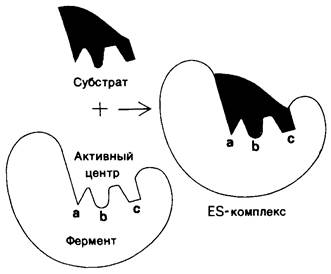
Рис. 6.11. Взаимодействие субстратов