БИОХИМИЯ - Л. Страйер - 1984
ТОМ 2
ЧАСТЬ III. БИОСИНТЕЗ ПРЕДШЕСТВЕННИКОВ МАКРОМОЛЕКУЛ
ГЛАВА 22. БИОСИНТЕЗ НУКЛЕОТИДОВ
22.3. Фосфорибозилпирофосфат- донор рибозофосфатного остатка нуклеотидов
Путь биосинтеза пуринов был расшифрован в 50-х годах в работах Джона Бьюкенена, Дж. Роберта Гринберга и др. (John Buchanan, G. Robert Greenberg). Рибозофосфатный остаток пуриновых и пиримидиновых нуклеотидов происходит из 5-фосфорибозил-1 - пирофосфата (ФРПФ), ключевого промежуточного продукта биосинтеза гистидина и триптофана. ФРПФ синтезируется из АТР и рибозо-5'-фосфата, который в свою очередь образуется в реакциях пентозофосфатного пути (разд. 15.1). Пирофосфатная группа переносится с АТР на С-1 рибозо-5-фосфата. ФРПФ находится в α-конфигурации.
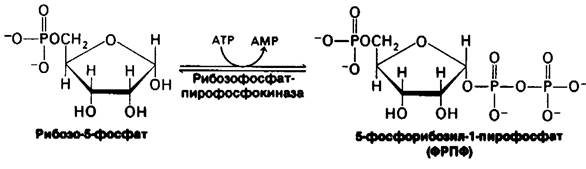
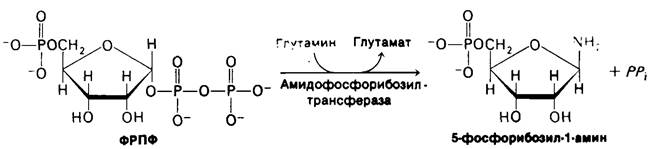
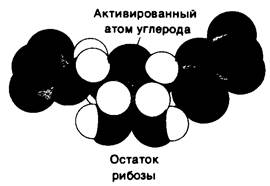
Рис. 22.5. Пространственная модель 5-фосфорибозил-1 -пирофосфата (ФРПФ), активированного донора остатка сахара при биосинтезе нуклеотидов
22.4. Пуриновое кольцо присоединяется к рибозофосфату во время его сборки
Первый решающий этап синтеза пуриновых нуклеотидов de novo-образование 5-фосфо- рибозиламина из ФРПФ и глутамина. Аминогруппа боковой цепи глутамина замещает пирофосфатную группу, присоединенную к С-1 ФРПФ. В ходе этой реакции α-конфигурация атома С-1 переходит в β-конфигурацию. Образующаяся гликозидная связь С—N имеет p-конфигурацию, характерную для природных нуклеотидов. Движущая сила этой реакции - гидролиз пирофосфата.
Продукт присоединения глицина к фосфорибозиламину - рибонуклеотид глицинамида (рис. 22.6). На образование амидной связи между карбоксильной группой глицина и аминогруппой фосфорибозиламина затрачивается одна молекула АТР. Затем α- аминогруппа остатка глицина форматируется метенилтетрагидрофолятом, образуя рибонуклеотид α-Nформилглицинамида.
Рис. 22.6. Первый этап биосинтеза пуринов: образование 5-аминои- мидазолрибонуклеотида из ФРПФ. Смысл этих реакций заключается в замещении пирофосфатной группы аминогруппой боковой цепи глутамина (1), присоединении глицина (2), формилировании с участием метенилтетраги- дрофолята (3), переносе атома азота глутамина (4), дегидратировании и замыкании кольца (5)
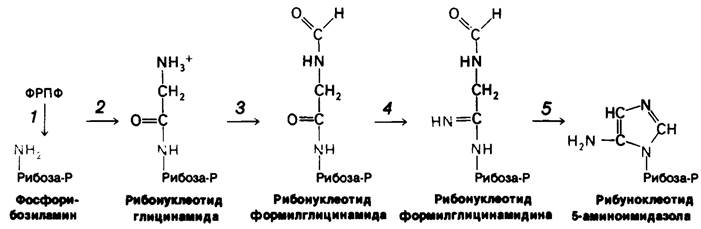
Амидная группа этого соединения превращается в амидиновую группу. Атом азота происходит из боковой цепи глутамина; в этой реакции затрачивается одна молекула АТР. Рибонуклеотид формилглицинамидина вступает затем в реакцию замыкания кольца с образованием рибонуклеотида 5-аминоимидазола. Этот промежуточный продукт содержит полное пятичленное кольцо пуринового остова.
Теперь начинается следующий этап синтеза скелета пурина-образование шестичленного кольца (рис. 22.7). Три из шести атомов этого кольца уже присутствуют в рибонуклеотиде аминоимидазола. Три другие атома происходят из СO2, аспартата и формил- тетрагидрофолята. Следующий атом углерода шестичленного кольца вводится путем карбоксилирования рибонуклеотида аминоимидазола, приводящим к образованию рибонуклеотида 5-аминоимидазол-4-карбоновой кислоты.
Рис. 22.7. Второй этап биосинтеза пуринов: образование инозината из 5-аминоимидазолрибону- клеотида. Суть этих реакций - карбоксил ирование (6), присоединение аспартата (7), отщепление фумарата (в результате которого остается аминогруппа аспартата) (5), форматирование с использованием N10-формилтетра- гидрофолята (9), дегидратация и замыкание кольца (10)
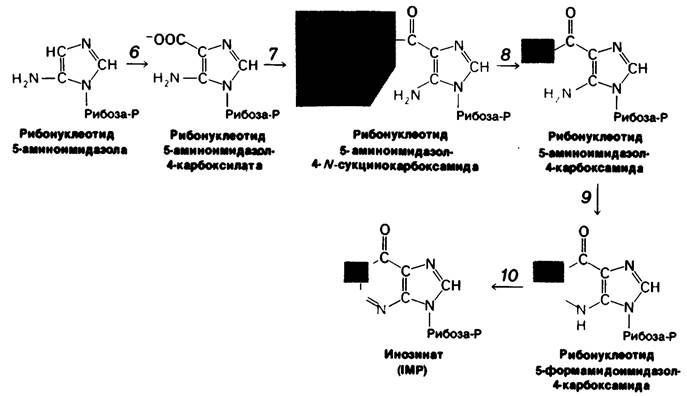
Затем аминогруппа аспартата реагирует с карбоксильной группой этого промежуточного продукта с образованием рибонуклеотида 5-аминоимидазол-4-N-сукцинокарбок- самида. На образование этой амидной связи затрачивается молекула АТР. В следующей реакции углеродный скелет остатка аспартата отщепляется в виде фумарата, и образуется рибонуклеотид 5-аминоимидазол-4-карбоксамида. Следует отметить, что в результате этих двух реакций карбоксилат превращается в амид. Таким образом, из аспартата в пуриновое кольцо включается только атом азота. Последний атом пуринового кольца происходит из N10-формилтетрагидрофолята. В результате образуется рибонуклеотид 5-формамидоимидазол-4-карбоксамида.; он претерпевает дегидратацию и замыкание кольца, давая инозинат (IMP), содержащий полный пуриновый скелет. Пуриновое основание, входящее в состав инозината, называется гипоксантин.
22.5. АМР и GMP образуются из IMP
Инозинат (инозинмонофосфат, IMP)-предшественник АМР и GMP (рис. 22.8). Аденилат синтезируется из инозината путем введения аминогруппы по С - 6 положению вместо карбонильного кислорода. Аминогруппу поставляет аспартат путем присоединения этой аминокислоты к рибонуклео- тиду и последующего удаления фумарата. GTP-донор высокоэнергетической фосфатной связи при синтезе аденилосукцина- та из инозита и аспартата. Отщепление фумарата от аденилосукцината и от рибонуклеотида 5-аминоимидазол-4-N-сукцино- карбоксамида катализируется одним и тем же ферментом.
Рис. 22.8. АМР и GMP синтезируются из IMP
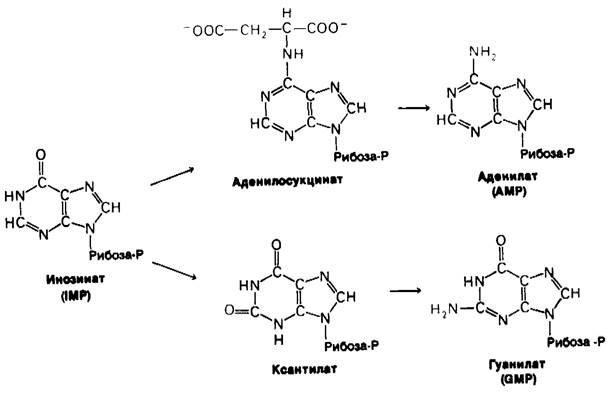
Гуанилат (инозинмонофосфат, GMP) синтезируется путем окисления инозината и последующего введения аминогруппы в положение С-2. NAD + - акцептор водорода при окислении инозината до ксанти- лата (ксантинмонофосфата, ХМР). Затем аминогруппа боковой цепи глутамина переносится на ксантилат. В этой реакции тратятся две высокоэнергетические связи, так как АТР расщепляется на АМР и PPi который затем гидролизуется.
При превращении инозината в аденилат и гуанилат карбонильный атом кислорода замещается аминогруппой. Сходное замещение происходит при синтезе рибонуклеотида формилглицинамида из соответствующего амидного предшественника (реакция 4 на рис. 22.6) при образовании СТР из UTP (разд. 22.13) и при превращении цитруллина в аргинин в цикле мочевины (разд. 18.5). Общий принцип этих реакций заключается в том, что карбонильный кислород превращается в какое-то производное, которое легко может вступить в реакцию замещения аминогруппой. Таутомерная форма карбонильной группы реагирует с АТР (или с GTP) и образует фосфорный эфир, который атакуется нуклеофильным амином (рис. 22.9). Затем неорганический фосфат отщепляется от тетраэдрического переходного комплекса, и реакция завершается. В качестве атакующего амина может выступать NH3, амидная группа боковой цепи глутамина или α-аминогруппа аспартата. На промежуточной стадии реакций этого типа отщепляется фосфат, пирофосфат или остаток АМР. Например, при синтезе 5-фосфорибозил-1-амина из ФРПФ аминогруппа глутамина замещает пирофосфат (разд. 22.4).
Рис. 22.9. Механизм реакции замещения карбонильного кислорода аминогруппой