БИОХИМИЯ - Л. Страйер - 1984
ТОМ 3
ЧАСТЬ V. МОЛЕКУЛЯРНАЯ ФИЗИОЛОГИЯ
ГЛАВА 37. ВОЗБУДИМЫЕ МЕМБРАНЫ И СЕНСОРНЫЕ СИСТЕМЫ
37.17. Свет снижает содержание циклического GMP путем активации фосфодиэстеразы
Как показывают приведенные экспериментальные данные, возбудимость палочек зависит и от Са2+, и от cGMP. Взаимодействие этих агентов может играть решающую роль в зрительном возбуждении. Что касается молекулярного механизма, индуцированного светом высвобождения Са2+ в цитозоль, то в этом вопросе еще много неясного. Что же касается регуляции светом содержания cGMP в наружных сегментах палочек, то в изучении этого вопроса в последние годы был достигнут значительный прогресс. На гуанилат-циклазу - фермент, катализирующий синтез cGMP, свет, по- видимому, не оказывает существенного влияния:
![]()
Зато на фосфодиэстеразу, гидролизующую cGMP, свет оказывает поразительное по силе действие:
![]()
В результате освещения активность фосфо- диэстеразы возрастает в несколько сотен раз. Стимуляция этого фермента фотолизированным родопсином опосредована регуляторным белком, называемым трансдуцином. В темноте трансдуцин содержит прочно связанную молекулу GDP. При освещении фотолизированный родопсин образует комплекс с GDP-трансдуцином и катализирует обмен GDP на GTP (рис. 37.34). Возникающий комплекс GTP-трансдуцин активирует фосфодиэстеразу. Крайне важное значение имеет то обстоятельство, что всего лишь одна фотолизированная молекула родопсина катализирует обмен GDP на GTP на нескольких сотнях молекул трансдуцина, что в свою очередь активирует сотни молекул фосфодиэстеразы. Следовательно, если число оборотов фосфодиэстеразы составляет примерно 103 с-1, то на свету в течение секунды гидролизуется уже более 105 молекул cGMP в расчете на одну молекулу фотолизированного родопсина. Система возвращается в исходное темновое состояние благодаря встроенной в нее GTP-азной активности. Присоединенный к трансдуцину GTP подвергается медленному гидролизу с образованием GDP-трансдуцина, неспособного активировать фосфодиэстеразу. Таким образом, весь этот цикл протекает за счет свободной энергии гидролиза GTP. Здесь мы видим пример того, как для усиления сигнала используется ~Р. Описанный каскад реакций, регулирующих содержание cGMP (рис. 37.35), очень напоминает каскад реакций, опосредующих действие β-адренергических гормонов, в частности адреналина (разд. 35.4).
Рис. 37.33. Молекулярная модель циклического GMP
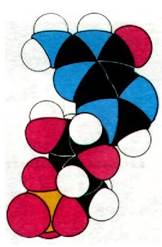
Рис. 37.34. Фотолизированный родопсин (Рд*) катализирует образование комплекса GTP с трансдуцином; этот комплекс в свою очередь активирует фосфодиэстеразу циклического GMP
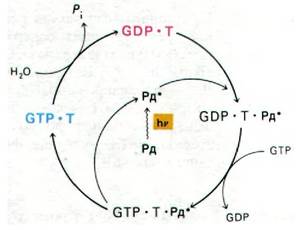
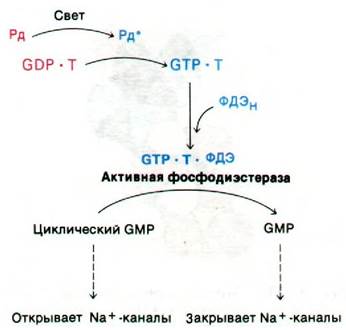
Рис. 37.35. Предполагаемый каскад реакций, регулирующих содержание cGMP в сетчатке глаза. Сокращения: Рд - родопсин, Рд* - фотолизированный родопсин, Т трансдуцин, ФДЭн - неактивная фосфодиэстераза, ФДЭ - активная фос- фодиэстераза
37.18. Цветовое зрение опосредуется фоторецепторами трех типов
В 1802 г. Томас Юнг (Thomas Young) высказал предположение, что цветовое восприятие опосредовано тремя основными рецепторами. Как показали спектрофотометрические исследования интактной сетчатки, проведенные более 150 лет назад, в глазу существует три типа клеток-колбочек, а именно клетки, поглощающие синий, зеленый и красный свет. Для получения спектра поглощения этих трех фоторецепторных пигментов колбочки освещали лучом света
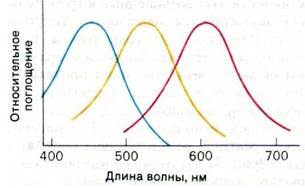
диаметром I мкм (рис. 37.36). Кроме того, во многие колбочки вводили микроэлектроды. Спектры действия, основанные на гиперполяризации плазматических мембран, разделяются на три группы с максимумами соответственно в синей, зеленой и красной областях видимого света. У золотой рыбки максимумы поглощения трех цветовых рецепторов приходятся на 455, 530 и 625 нм, тогда как родопсин характеризуется максимумом 500 нм.
Рис. 37.36. Спектры поглощения трех цветовых рецепторов
Хромофором в колбочках всех трех типов служит 11-цис-ретиналь. В отсутствие белка протонированное шиффово основание имеет максимум поглощения при 380 нм. Следовательно, различные группировки на опсине оказывают значительное действие на хромофорные свойства связанного 11-цис- ретиналя. Зависимость спектральных свойств этого хромофора от белкового окружения - частное проявление общего принципа, а именно взаимодействие с белком оказывает модулирующее влияние на свойства простетической группы. Другой пример тому - функционирование гема в качестве переносчика кислорода в гемоглобине, переносчика электронов в цитохроме с и катализатора в пероксидазе.
Большинство форм дальтонизма (цветовой слепоты) обусловлено сцепленной с полом рецессивной мутацией. Около 1% мужчин не видят красного цвета, около 2% - зеленого. Как показали спектральные исследования, проведенные на интактном глазе, у этих людей либо совсем отсутствуют фоторецепторные молекулы, воспринимающие красный или зеленый цвет, либо имеется измененный пигмент со сдвинутым спектром поглощения. Таким образом, дальтонизм обусловлен отсутствием или дефектом одного из типов опсина в колбочках.
37.19. 11-цис-ретиналь - хромофор всех известных органов зрения
Только у трех типов животных - моллюсков, членистоногих и позвоночных - глаза способны отображать образ предмета. Анатомически глаза этих трех типов устроены совершенно по-разному и, по-видимому, в ходе эволюции возникли независимо. Однако во всех трех случаях хромофором в фоторецепторных молекулах служит 11-цис- ретиналь. Это поразительный пример конвергентной эволюции. Что же такого особенного в 11-цис-ретинале? Во-первых, это соединение обладает интенсивной полосой поглощения, которая легко сдвигается в видимую область спектра. Во-вторых, под действием света 11-цис-ретиналь легко изомеризуется. Более того, в темноте скорость изомеризации очень низка. В-третьих, изомеризация вызывает большие изменения в структуре. В итоге поглощенный свет преобразуется в движение атомов такого масштаба, которое способно инициировать генерирование нервного импульса. Наконец, исходными предшественниками11-цис-ретиналя являются каротины (разд. 20.27), очень широко распространенные в живой природе.
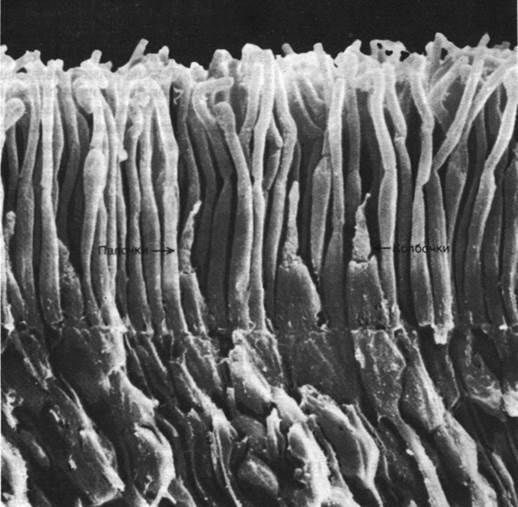
Рис. 37.37. Вид клеток - палочек и колбочек - фоторецепторного слоя сетчатки в сканирующем электронном микроскопе