Биохимия в таблицах схемах и графиках - С.Д. Жамсаранова 2009
Ферменты
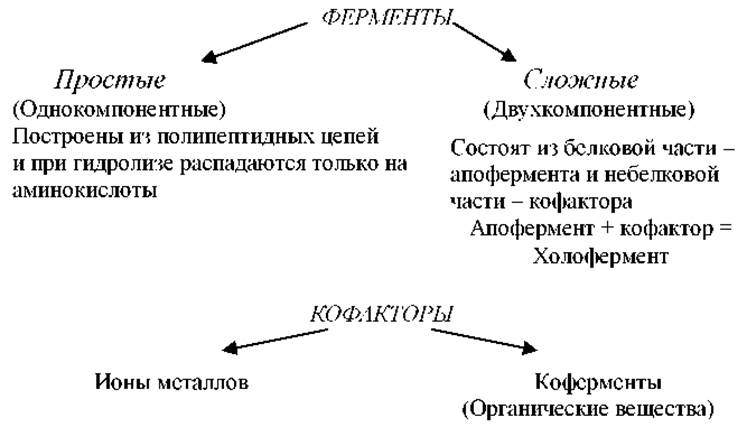
Классификация ферментов
Ферменты (Е) - это белковые катализаторы, ускоряющие реакции в клетке.
Сходство ферментов с химическими катализаторами:
- увеличивают скорость реакции, но не расходуются в ходе процесса и не претерпевают необратимых изменений;
- не изменяют состояние равновесия химической реакции, ускоряя как прямую так и обратную реакцию в равной степени;
- повышают скорость реакции, понижая энергию активации, тот энергетический барьер, который отделяет одно состояние системы от другого.
Отличия ферментов от небиологических катализаторов:
- высокая эффективность действия;
- высокая специфичность действия - способность выбирать определенный субстрат и катализировать специфическую реакцию;
- мягкие условия протекания ферментативных реакций: температура 370С, нормальное атмосферное давление, рН, близкое к нейтральному;
- способность к регуляции.
Класс |
Тип катализируемой реакции |
Оксидоредуктазы |
Окислительно-восстановительные реакции |
Трансферазы |
Перенос отдельных групп атомов от донорной молекулы к акцепторной молекуле |
Гидролазы |
Гидролитическое (с участием воды) расщепление связей |
Лиазы |
Расщепление связей способом, отличным от гидролиза или окисления |
Изомеразы |
Взаимопревращение различных изомеров |
Лигазы (синтетазы) |
Образование связей в реакции конденсации двух различных соединений (используется энергия АТР) |
НЕКОТОРЫЕ МЕТАЛЛОЗАВИСИМЫЕ ФЕРМЕНТЫ
Фермент |
Ион металла |
Функция иона металла |
Гексокиназа |
Mg2+ |
Связывание субстрата |
Пируваткиназа |
Mg2+, К+ |
Связывание субстрата и катализ |
Пируваткарбоксилаза |
4Mn2+ |
Катализ |
а-Амилаза |
Са2+ (Cl-) |
Стабилизация третичной структуры |
Транскетолаза |
Са2+ |
Стабилизация четвертичной |
структуры |
||
Супероксиддисмутаза |
2Zn2+,2Cu2+ |
Катализ |
Карбоксипептидаза А |
Zn2+ |
Катализ |
Аргиназа |
4Mn2+ |
Связывание субстрата и катализ |