БІОТЕХНОЛОГІЯ - В. Г. Герасименко - 2006
Частина ІІ. Спеціальні біотехнології
Розділ 17.БІОТЕХНОЛОГІЯ ОДЕРЖАННЯ ВІТАМІНІВ
Забезпечення потреб людини і сільськогосподарських тварин достатньою кількістю вітамінів є важливою проблемою, яку в сучасних умовах неможливо вирішити лише за рахунок використання традиційних природних вітамінних ресурсів. Крім того, вітаміни, їх коферментні форми і похідні дедалі ширше застосовуються як препарати для лікування різних форм гіповітамінозів і авітамінозів, а також інших захворювань.
Термін «вітаміни» був запропонований Функом ще на початку минулого сторіччя. Сьогодні до вітамінів належить велика група низькомолекулярних органічних сполук різної хімічної природи, які присутні в організмі у незначних концентраціях, і як компоненти ферментних систем, що каталізують відповідні реакції. Вищі тварини і людина в основному потребують одержання готових вітамінів, а серед мікроорганізмів широко розповсюджена здатність до їх синтезу.
До вітамінів включають за прийнятою літерною класифікацією: в групу В (В1 - тіамін, В2 - рибофлавін, В3 - пантотенова кислота, В5 - нікотинова кислота, В6 - піридоксин, Вс чи В9- фолієва кислота, В12 - ціанкобаламін, Н - біотин); вітамін С (аскорбінова кислота); групи А - ретиноли і провітамін А - β-каротин; D (кальцифероли і провітаміни - ергостерин, холестерин); Е (токофероли); К (нафтохінони); їх коферментні форми та різні інші похідні.
Вітаміни групи В ще називають кофакторними вітамінами, тому що вони входять у структуру коферментів. Ці вітаміни беруть участь в метаболізмі як вищих організмів, так і мікробних клітин. Механізм дії інших вітамінів вивчений недостатньо. Деякі з них, наприклад С, А, D, не функціонують в мікробних клітинах, хоча провітаміни останніх двох - β-каротин і ергостерин - беруть участь у життєдіяльності певних типів мікроорганізмів і ними синтезуються.
Вітаміни одержують як хімічним, так і мікробіологічним синтезом.
Практичне використання здатності мікроорганізмів до біосинтезу вітамінів розпочалося в 30-40-і роки минулого століття. В першу чергу звернули увагу на пивні і пекарські дріжджі як джерело вітамінів — ВрD2, С тощо.
Однак широкі перспективи щодо використання мікроорганізмів для одержання вітамінів з’явилися пізніше завдяки виявленню у них здатності до так званого надсинтезу вітамінів, тобто до утворення і накопичення в культурах деяких видів набагато більшої їх кількості, ніж потрібно для виконання каталітичних функцій. На це явище вперше звернув увагу в 30-х роках XX ст. Гільєрмон, який виявив накопичення рибофлавіну в культурі гриба Eremothecium ashbyii. Його роботи показали, що мікроорганізми можуть бути такою собі фабрикою вітамінів, і викликали в усьому світі посилений інтерес до питань їх мікробіологічного синтезу.
Незабаром надсинтетики рибофлавіну були знайдені і серед інших груп мікроорганізмів — дріжджів, бактерій, міцеліальних грибів. Потім була виявлена здатність до підвищеного синтезу інших вітамінів — В12 (у актиноміцетів, пропіоновокислих, метанових і деяких інших груп бактерій), каротиноїдів (у гетероталічних мукорових грибів), ергостерину (у деяких сахароміцетів).
У Радянському Союзі були створені виробництва кормового препарату вітаміну В2 з використанням активного продуцента гриба E. аshbyii, медичного і кормового препаратів вітаміну В12 за участю пропіоновокислих і метанових бактерій, β-каротину з грибом Blakeslea trispora і каротиногенними дріжджами, а також одержання дріжджів з підвищеним вмістом ергостерину.
Прогрес у вивченні хімізму біосинтезу вітамінів дав можливість використовувати для їх одержання не тільки активні продуценти, але й мікроорганізми, здатні здійснювати окремі етапи синтезу. Наприклад, при виробництві вітаміну С оцтовокислі бактерії використовуються для трансформації сорбіту в сорбозу.
Завдяки встановленню механізмів вітаміногенезу одержані мутанти продуцентів спроможні до надсинтезу вітамінів, що сприяло створенню більш економічних способів виробництва продуктів порівняно з існуючими. Є дані про одержання мутантів, які накопичують у середовищі вітаміни В1, В6, біотин (Діканська Е.М., 1984).
Крім вітамінів, мікробіологічним шляхом одержують інші речовини вітамінної природи, передусім коферменти. Дедалі ширше їх застосовують у медичній практиці, а мікробіологічний синтез в багатьох випадках єдиний або найбільш прийнятний спосіб їх одержання.
Нові перспективи практичного використання мікроорганізмів як синтетиків вітамінів відкриває використання в мікробіологічній промисловості нетрадиційних видів вуглецевих субстратів (вуглеводні, нижчі спирти і кислоти) - нехарчових субстратів.
Встановлено, що вуглець належить до факторів, задіяних у регуляції процесів вітаміногенезу, і використання вуглецевих субстратів забезпечує підвищення рівня синтезу цілої низки сполук вітамінної природи (рибофлавіну, ергостерину, пантотенової кислоти, ФАД, НАД, вітаміну В6, коензиму Q, вітаміну В12).
На сьогодні існують такі напрями вирішення проблеми одержання вітамінів мікробіологічним синтезом:
1. Одержання вітамінів і коферментів з використанням мікро- організмів-продуцентів, в основному надсинтетиків, і спеціальних режимів їх культивування. До цієї категорії належать уже існуючі біотехнології одержання вітамінів В2, В12, каротиноїдів.
2. Одержання індивідуальних вітамінів і коферментів з біомаси мікроорганізмів, яку вирощують у промислових масштабах на різних вуглецевих субстратах, або використання її як комплексних вітамінних препаратів. Сьогодні, коли в усьому світі існує крупнотоннажне виробництво білка одноклітинних, цей напрям набуває великого значення, тому що мікробна білкова біомаса може слугувати комплексним джерелом вітамінів у тваринництві, а також використовуватися для виділення деяких синтезованих продуцентами білка сполук вітамінної природи.
3. Використання мікроорганізмів для здійснення окремих стадій процесу синтезу вітамінів. Можливості використання для вирощування таких мікроорганізмів нових видів нехарчової сировини розширюють межіі цього напряму.
Варто наголосити, що багато вітамінів успішно одержують хімічним синтезом. Однак для деяких вітамінів і багатьох ко- ферментів мікробіологічний спосіб їх одержання поки що залишається єдиним або найбільш ефективним. В деяких випадках мікробіологічний синтез може успішно конкурувати з хімічним, особливо коли немає необхідності виділяти окремі вітаміни, наприклад при використанні їх у тваринництві.
Каротиноїди - це ізопреноїдні сполуки, які синтезуються багатьма пігментними мікроорганізмами із родів Aleuria, Blakeslea, Corynebacterium, Flexibacter, Fusarium, Halobacterium, Phycomyces, Pseudomonas, Rhodotorula, Sarcina та ін. Всього описано майже 500 каротиноїдів.
З однієї молекули β-каротину при гідролізі утворюються дві молекули вітаміну Аг Це відбувається, наприклад, у кишечнику людини.
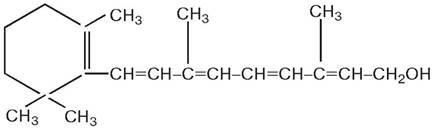
ВІТАМІН A1
Каротиноїди локалізуються у вигляді складних ефірів і глікозидів у клітинній мембрані мікроорганізмів або у вільному стані - в ліпідних гранулах у цитоплазмі. Каротиноїд «ретиналь», наприклад, у галофільного виду Halobacterium halobium сполучений з білком через залишок лізину. Він бере участь в синтезі АТФ завдяки генерації трансмембранного потенціалу. В цілому основна функція каротиноїдів - захисна. їхньому біосинтезу в клітинах сприяє світло.
Як продуценти каротиноїдів можна використовувати бактерії, дріжджі, міцеліальні гриби. Найчастіше використовують зигоміцети Blakeslea trispora i Choanephora conjucta. При спільному культивуванні вони можуть утворювати 3-4 г каротину на 1 л середовища.
Поживні середовища для них досить складні і включають джерела вуглецю, азоту, вітамінів, мікроелементів і спеціальних стимуляторів. Останні доцільно вносити в культуральне середовище в кінці трофази.
Спочатку штами вирощують порізно, а потім - спільно при температурі 26 оС і посиленій аерації з подальшим перенесенням в основний ферментер. Умови культивування зберігаються. Тривалість ферментації - 6-7 днів. Каротиноїди вилучають ацетоном (можна будь-яким іншим полярним розчинником) і переводять у неполярний розчинник. У випадках вилучення білково-каротиноїдних комплексів використовують поверхнево-активні речовини в концентрації 1-2 %. З метою очищення і більш тонкого розділення гомологів використовуються методи хроматографії або зміни розчинників. Вітамін А1 порівняно легко можна одержати з β-каротину при гідролізі.
У разі виготовлення каротиновмісної біомаси для згодовування тваринам і птиці можливе поєднання використання її з вітаміном А чи без нього. Для застосування вітаміну А з лікувальною метою його виготовляють в капсулах для перорального вживання.
ВІТАМІН D — це група споріднених сполук, в основі яких знаходиться ергостерин, що виявлений в клітинних мембранах еукаріот. Тому, наприклад, пекарські чи пивні дріжджі використовують для одержання ергостерину як провітаміну з антирахітичною дією. Вміст ергостерину в дріжджових клітинах коливається у межах 0,2-11 %.
За нестачі в організмі гормона 1,25 — дігідроксіхолекальциферолу, попередником якого є вітамін D3, у дітей розвивається рахіт (аналогом рахіту в дорослих є остеомаляція).
Трансформація ергостерину у вітамін D2 (кальциферол) відбувається під впливом ультрафіолетового опромінення. При цьому розривається зв’язок в кільці (позиції 9, 10) і утворюється подвійний зв’язок у бічному ланцюзі (позиції 22, 23). Останній гідрований у вітаміні D3 (холекальциферол). Фізіологічна активність обох вітамінів (D2 і D3) однакова.
Крім дріжджів продуцентами ергостерину можуть бути міцеліальні гриби — аспергіли і пеніцили, в яких міститься 1,2—2,2% ергостерину. Виявлено, що поліенові антибіотики, які діють на клітинну мембрану дріжджів, помітно стимулюють вміст ергостерину в біомасі.
При одержанні ергостерину у виробничих умовах можна виділити такі етапи: розмноження вихідної культури і накопичення інокулята; ферментація; сепарування клітин; опромінення клітин ультрафіолетовими променями; висушування і упакування цільового продукту.
Так, стосовно дріжджів інокулят одержують на середовищах, які забезпечують повноцінний розвиток клітин. Після цього основне середовище з ацетатом (активатором біосинтезу стеринів), яке містить знижену кількість азоту, але збагачене джерелом вуглецю (високе значення C:N), засівають порівняно великим об’ємом інокулята. Культивування дріжджів (ферментацію) проводять при температурі, наближеній до максимальної для конкретного штаму, і належній аерації (2 % О2 в газовій фазі). Через 3-4 доби, залежно від ростових характеристик і біосинтетичної активності культури, клітини сепарують і піддають вакуум-висушуванню. Потім сухі дріжджі опромінюють ультрафіолетовими променями - УФП (довжина хвилі 280-300 нм) протягом оптимального часу за необхідної температури і з урахуванням домішок.
Опромінення дріжджів можна проводити до сепарації клітин у тонкому шарі 5 % суспензії, враховуючи невелику проникну здатність УФП.
Опромінені сухі дріжджі використовують у тваринництві. У промисловості їх випускають під назвою «кормові гідролізні дріжджі, збагачені вітаміном D2». У такому препараті міститься не менше 46 % сирого білка, незамінні амінокислоти (лізин, метіонін, триптофан) і 5000 МО вітаміну D2/г
У випадку одержання кристалічного вітаміну D2 клітини продуцента гідролізують соляною кислотою при температурі 110 оС. Потім температуру знижують до 75-78 оС і додають етанол. Суміш фільтрують при 10-15 оС і масу, яка залишилася після фільтрації, промивають водою, висушують, подрібнюють, нагрівають до 78 оС і двічі обробляють потрійним об’ємом етанолу. Спиртові екстракти об’єднують і упарюють до 70 %-го вмісту сухих речовин. Одержаний «ліпідний концентрат» обробляють розчином їдкого натрію. Ергостерин кристалізується з неомиленої фракції концентрату при 0 оС. Його можна очистити повторними перекристалізаціями. Кристали висушують, розчиняють у сірчаному ефірі, опромінюють УФП, ефір відганяють, а розчин вітаміну D2 концентрують і кристалізують.
«Кислотний фільтрат» зазвичай упарюють до 50 %-го вмісту сухих речовин і використовують як концентрат D-вітамінів. Виробляють також масляний концентрат вітаміну D2.
Рибофлавін або ВІТАМІН В2. Міститься в клітинах різних мікроорганізмів, будучи коферментом у складі флавопроте- їнів (перш за все відповідних ферментів класу оксидоредуктаз - ФМН, ФАД). Продуцентами рибофлавіну (флавопротеїнів) можуть бути бактерії, дріжджі і нитчасті гриби. Однак найбільш перспективними є штами, які утворюють на рідких середовищах 0,5 г і більше рибофлавіну в 1 л середовища. До таких організмів належать Ashbyii gossypii, Eremothecium ashbyii i Candida guilliermondii. Враховуючи мінливість активних продуцентів названих видів за здатністю синтезувати вітамін В2, необхідний систематичний підтримувальний відбір культур у процесі їх експлуатації на виробництві. Зазвичай активні продуценти перших двох видів формують яскраво-оранжеві колонії на агаризованих середовищах.
Методами генетичної інженерії вдалось одержати штам сінної палички, яка утворює приблизно 6 г рибофлавіну в 1 л культурального середовища, що містить патоку, білково-вітамінний концентрат і його гідролізат.
Високий вихід рибофлавіну у E. ashbyii корелює з азотом пуринів та іншими азотистими джерелами, вміст яких у середовищі має бути достатнім. Як джерело вуглецю використовують глюкозу або цукрозу, дріжджовий або кукурудзяний екстракт, соєву муку, масла (жири).
Рідкі поживні середовища для одержання інокуляту і для основної ферментації можуть дещо відрізнятися між собою. Наприклад, для одержання посівного матеріалу відоме середовище, яке містить цукрозу, пептон, кукурудзяний екстракт, калію дигідрофосфат, магнію сульфат, рослинну олію. Час вирощування продуцента на цьому середовищі — 2 доби при температурі 27-30 оС (залежно від штаму). Ферментаційне середовище
зазвичай включає кукурудзяну і соєву муку, цукрозу, кукурудзяний екстракт, калію дегідрофосфат, кальцію карбонат, натрію хлорид і ненасичений жир.
Зазвичай тривалість ферментації становить 5 діб при рН 5,5-7,7. Після використання цукрози (приблизно через 30 годин) починає помітно накопичуватися вітамін В2, спочатку — в міцелії, а потім — у культуральній рідині.
Для використання в годівлі тварин всю біомасу висушують і в одержаному сухому продукті вологістю 8 % міститься 1,5—2,5 % рибофлавіну, 20 % білка, тіамін, нікотинова кислота, піридоксин, ціанкобаламін, мікроелементи та інші речовини.
У випадку високих вихідних показників за рибофлавіном вітамін можна виділяти індивідуально і разом із синтетичним рибофлавіном використовувати в медицині.
Для Candidia guilliermondii дуже важливо регулювати вміст заліза в поживному середовищі, оптимальна концентрація якого коливається в середньому від 0,005 до 0,05 мкг/мл. При цьому певні штами дріжджів можуть утворювати за 5-7 днів понад 0,5 г/л вітаміну. Однак для промислового виробництва рибофлавіну перевагу надають більш продуктивним видам і штамам грибів - E.ashbyii i Ashbyn gossypii.
Аскорбінова кислота, або ВІТАМІН С. Це протицинготний вітамін, який міститься у всіх вищих рослинах і тваринах. Тільки людина і мікроби не синтезують її, але людям вона вкрай необхідна, а мікроби не потребують цього вітаміну. Однак певні види оцтовокислих бактерій синтезують напівпродукт аскорбінової кислоти — L-сорбозу. Таким чином, весь процес одержання аскорбінової кислоти є змішаним, тобто хіміко-ферментативним.
Біологічна стадія процесу каталізується мембранозв’язаною поліолдегідрогеназою, а остання (хімічна) включає послідовно такі етапи: конденсація сорбози з діацетоном і одержання діацетон-Lсорбози; окислення останньої до діацетон-2-кето-L-гулонової кислоти, яку в подальшому піддають гідролізу з одержанням 2-кето-L-гулонової кислоти; останню піддають енолізації з наступною трансформацією в L-аскорбінову кислоту (рис. 17.1).
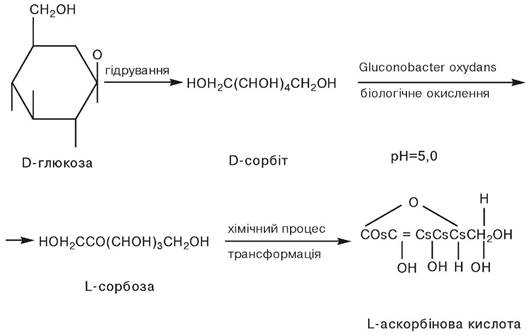
Рис. 17.1. Схема хіміко-ферментативного методу одержання аскорбінової кислоти
(за Єліновим Н.П., 1995)
Ферментацію G.oxydans проводять на середовищах, які містять сорбіт (20 %), кукурудзяний або дріжджовий екстракт, при інтенсивній аерації (8-10 г О2/л/год). Вихід L-сорбози може сягнути 98 % за одну-дві доби. При досягненні культурою log-фази можна додатково вводити в середовище сорбіт, доводячи його концентрацію до 25 %. Також установлено, що G.oxydans може окислювати і вищі концентрації поліспирту (30-50 %), який утворюється на останніх стадіях процесу. Ферментацію бактерій проводять в періодичному або безперервному режимі. Доведена можливість одержання L-сорбози із сорбіту за допомогою іммобілізованих у поліакриламідному гелі бактеріальних клітин.
Аскорбінову кислоту використовують як антиоксидант у медицині, а також у харчовій промисловості.
Ціанкобаламін, або ВІТАМІН В12. Одержують тільки мікробіологічним синтезом. Його продуцентами є прокаріоти і перш за все пропіоновокислі бактерії, які в природних умовах утворюють цей вітамін. Мутанти Propionibacterium shermanii M-82 і Pseudomonas denitrificans M-2436 продукують на рідкому середовищі до 58-59 мг/л ціанкобаламіну.
Враховуючи важливу функцію вітаміну в організмі людини (він є протианемічним фактором), його світове виробництво досягло 10 т на рік, з яких 6,5 т витрачають на медичні потреби, а 3,5 т — у тваринництві (Єлінов Н.П., 1995).
Вітчизняне виробництво ціанкобаламіну базується на використанні Р. freudenreichii Var. shermanii, яка культивується у періодичному режимі без доступу кисню. Ферментативне середовище зазвичай містить глюкозу, кукурудзяний екстракт, солі амонію і кобальту. pН близько 7,0 підтримують додаванням NH4OH. Тривалість ферментації 6 діб. Через 3 доби у середовище додають 5,6-диметилбензімідазол — попередник вітаміну В12 і продовжують ферментацію ще 3 доби.
Ціанкобаламін накопичується в клітинах бактерій, тому операції з виділення вітаміну полягають у наступному: сепарування клітин, ектрагування водою при рН 4,5-5,0 і температурі 85-90 оС за присутності стабілізатора (0,25 %-й розчин натрію нітриту). Екстракція відбувається протягом години, після чого водний розчин охолоджують, нейтралізують розчином NaOH, додають коагулянти білка (хлорид заліза тривалентного і алюмінію сульфату) з подальшою фільтрацією. Фільтрат упарюють і додатково очищують, використовуючи методи іонного обміну і хроматографії, потім проводять кристалізацію вітаміну при температурі 3-4 оС з водно-ацетонового розчину.
Кристалічний ціанкобаламін можна одержати за допомогою резорцину або фенолу, що утворюють з ним аддукти, які порівняно легко розкладаються на складові компоненти.
При реалізації даного біотехнологічного процесу потрібно зважати на високу чутливість до світла вітаміну В12. Через це усі операції необхідно проводити в умовах затемнення (або при червоному світлі).
На ацетонобутиловій або спиртових бардах з додаванням солей кобальту і метанолу одержують кормовий препарат КМБ12 - концентрат, який містить вітамін В12 та інші ростові біологічно активні речовини. Біооб’єктом є змішана культура метаногенних бактерій.