БІОТЕХНОЛОГІЯ - В. Г. Герасименко - 2006
Частина І. Загальна біотехнологія
РОЗДІЛ 4. КЛІТИННА ІНЖЕНЕРІЯ
4.2.БІОТЕХНОЛОГІЇ ГІБРИДИЗАЦІЇ СОМАТИЧНИХ КЛІТИН
Причиною встановленого ще в минулому столітті факту багатоядерності клітин як патологічних (пухлини, ділянки з запаленням, що утворюються при коров’ячій віспі та ін.), так і нормальних (м’язові волокна) тканин могло бути, з одного боку, поділ ядер без одночасного поділу клітин (наприклад, формування плазмодія слизуватого гриба Physarium), з іншого — злиття декількох клітин (міобластів) і утворення багатоядерної клітини — м’язового волокна. Злиття відбувається не тільки серед диференційованих клітин у багатоклітинних організмах, але й між клітинами в культурі. Зливатися можуть клітини різного типу, що належать до того самого виду (наприклад, мишачі фібробласти і мишачі лімфобласти), так і клітини тварин різних видів (наприклад, миша/людина; хом’як/курка; комар/людина). У першому випадку батьківські клітини, що зливаються, розрізняються між собою за морфологічними, біохімічними, імунологічними або функціональними властивостями, а продукти злиття є внутрішньовидовими гібридами. В другому випадку утворюються міжвидові гібриди, а вихідні батьківські клітини, від злиття яких ці гібриди з’являються, насамперед відрізняються генотипічно, а іноді й фенотипічно. Багатоядерні клітини (полікаріони), що утворяться в результаті злиття клітин двох різних типів (А і В), представлені трьома комбінаціями — АА, ВВ і АВ. Полікаріони, що містять ядра тільки одного клітинного типу (АА і ВВ), називаються гомокаріонами; полікаріони, у складі яких присутні ядра обох батьківських типів (АВ), належать до гетерокаріонів. Злиття в гетерокаріонах ядер після злиття клітин є результатом виникнення клітинного гібрида (рис. 4.1).
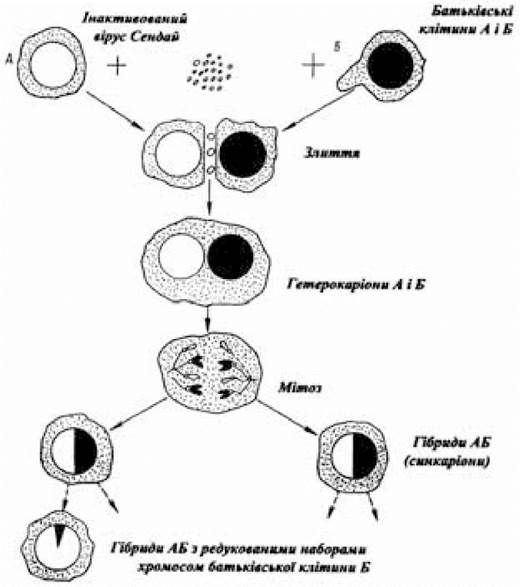
Рис. 4.1. Схема злиття двох одноядерних клітин А і Б, які належать тваринам двох різних видів
(за Рінгерцем Н. та Севіджом Р., 1979)
Овчинников Ю.А. (1982) знайшов вирішення проблеми за допомогою методу гібридизації соматичних клітин. Гібридизація широко використовується в генетиці, біології клітини, біології розвитку, вірусології, біології пухлин та інших галузях біологічної науки, а також на практиці.
Метод одержання і культивування гібридних клітин може бути використаний для вирішення практичних питань охорони здоров’я, тому що за продуктами експресії хромосоми, що залишилися в геномі синкаріона з батьківської клітини людини, визначаються ознаки генетичних спадкових захворювань. За допомогою методу гібридизації соматичних клітин вдається ре- активувати онкогенний вірус. При злитті клітин-вірусоносіїв з нормальними, але чутливими до пухлинного вірусу клітинами в синкаріонах, що утворилися, настає реактивація вірусу, який інтенсивно розмножується в кількостях, достатніх для його виявлення.
Цей методичний прийом використовують для виявлення в пухлинних клітинах онкогенного вірусу. Утворення синкаріонів, наступне вивчення клітинних гібридів у культурі, а також при введенні їхньої суспензії тваринам та поява пухлин, що спостерігається не у всіх випадках, подає необхідну інформацію для з’ясування механізмів виникнення раку. Наприклад, вирішувати питання про злоякісність або доброякісність одержаного з пухлинної і нормальної клітин синкаріона можливо, очевидно, залежно від наявності чи відсутності в гібридній клітині певних хромосом.
Антисироватки зі специфічними антитілами, отриманими звичайними методами, широко й успішно використовувалися для ідентифікації, очищення або для руйнування певних клітин, що знаходяться в оточенні клітинних популяцій, які розрізняються між собою. Специфічні антисироватки використовувалися при вивченні клітинних ліній і факторів, що беруть участь у процесах проліферації і диференціації, а також для ідентифікації компонентів синапсів, що являють собою місця міжклітинної взаємодії у нервовій системі.
За допомогою методик з використанням антисироватки була встановлена специфічна локалізація калмодуліну, клатрину і тубуліну в синаптичних ділянках, що дозволило сформулювати більш обґрунтовану думку про функції цих молекул, що беруть участь в забезпеченні життєдіяльності всіх клітин. Крім того, за допомогою антисироваток у місцях нервово-м’язового з’єднання були виявлені специфічні для цієї ділянки антигени, що відіграють важливу роль у функціонуванні цього синапсу. Стає очевидною потенційна можливість методу застосування анти- сироваток для розкриття механізмів диференціації нерва і м’яза в цій спеціалізованій ділянці.
Антисироватки виявилися найбільш ефективними реагентами, а їхнє застосування дало можливість виявляти локалізацію клітин, що синтезують і містять нейропептиди і непептидні медіатори, а також ферменти, що беруть участь у їхньому біосинтезі. Висока чутливість імуноцитохімічних методів дозволила ідентифікувати і визначити локалізацію більше двох десятків медіаторів.
Участь багатьох органічних молекул у регуляції специфічних клітинних функцій вдалося встановити також за допомогою імунологічних досліджень. Потенційні можливості методу неможливо реалізувати через недоліки, властиві антисироваткам, отриманим у результаті імунізації тварин гетерогенними імуногенами. Ефективність антисироваток зменшується через наявність не тільки молекул, які цікавлять у даний момент дослідника, але й інших антигенів. Так, є підстави вважати, що окрема клітина імунної системи, що синтезує імуноглобулін (Ig), і її нащадки відтворюють тільки один вид антитіл. Ця унікальна властивість імунної системи була покладена в основу при розробці методу щодо зниження гетерогенності стандартних антисироваток. Імунізацію тварин проводять гетерогенними чи поліспецифічними антигенами. Однак надалі в культурі вирощують клони окремих синтезуючих імуноглобулін клітин, що продукують окремі моноспецифічні чи моноклональні антитіла, вільні від домішок антитіл до сторонніх антигенів. Ідентифікація клітин, які утворюють антитіла, не має особливої складності; що стосується розмноження їх у культурі, то, як було сказано раніше, це вдається зробити протягом нетривалого часу. Гібридні клітини, отримані злиттям пухлинних і секретуючих імуноглобулін клітин імунної системи — гібридоми, поєднують у собі здатність до тривалого розмноження в культурі зі здатністю біосинтезу моноклональних антитіл. Уперше гібридоми були отримані шляхом злиття антитілоутворюючих клітин селезінки (спленоцитів) миші, імунізованої баранячими еритроцитами, з мієломними клітинами, у яких була відсутня гіпоксантинфосфорибозилтрансфераза (фермент, що бере участь у реакціях метаболізму пуринів). Щоб збільшити імовірність злиття батьківських клітин і підвищити вихід гібридом, як допоміжний засіб використовують віруси з аглютинуючими властивостями. Вірусні частки накопичуються на поверхні батьківських клітин, що вступають у контакт; на поверхні контактуючих клітин з’являється велика кількість мікроворсинок, що у місцях дотику зливаються, утворюючи цитоплазматичні містки. Зони злиття поступово розширюються, заповнюючи всю площу мембрани в ділянці клітинного контакту.
Kohler G., Milstein C. (1975), що першими запропонували спосіб одержання гібридом, для злиття батьківських клітин використовували вірус Сендай, що належить до групи вірусів парагрипу, інактивованого ультрафіолетовим випромінюванням. Замість вірусів використовуються ліпіди, іони кальцію в лужному розчині (рН 10,5), фосфоліпаза С. Останнім часом знайшов широке застосування поліетиленгліколь. Такі речовини, як цитохалазин В, інгібітори енергетичного обміну, а також засоби, що викликають місцеву анестезію, навпаки, блокують процес злиття клітин.
Клітини селезінки, що не взяли участі в утворенні гібридом, через певний час гинули, тому що не були здатні до проліферації і виживання в культурі. Мієломні клітини, що залишилися у культурі, під впливом доданого в середовище аміноптерину гинули, тому що процес синтезу пуринів de novo припинявся. Гібридомні клітинні лінії були життєздатними в культурі завдяки присутності гена, що кодує біосинтез ферменту гіпоксантин фосфорибозилтрансферази, за участю якого гіпоксантин перетворюється на пуринові нуклеотиди. Гени батьківської мієломи забезпечують гібридомній культурі постійний поділ.
Лінія гібридомних клітин, що синтезує антитіла проти баранячих еритроцитів, була ідентифікована методом їхнього гемолізу. Крім того, виявилося, що в популяції гібридомних клітин кількість клонів, продукуючих антитіла проти баранячих еритроцитів, у 100 разів перевищувало кількість клонів у вихідній батьківській популяції спленоцитів (10 % у гібридомній популяції проти 0,01 % у популяції спленоцитів). Цей приклад указує на здатність стимульованих антигеном клітин забезпечувати одержання функціонально активних гібридів.
При гібридомній технології придатною є така система добору, за якої життєдіяльними залишалися б тільки гетерокаріони. З цією метою підбираються вихідні батьківські клітинні лінії, що мають дефекти в генах, які перешкоджають їх поділу і росту. Одночасно внаслідок взаємної комплементації гетерокаріони зберігають здатність до поділу (Зенгбуш П.).
Найбільш розповсюдженою є система добору за допомогою селективного середовища, що містить гіпоксантин, аміноптерин і тимідин (середовище ГАТ). Вихідні батьківські клітинні лінії, використані для одержання клітинних гібридів, містять дефектні ферменти; гіпоксантингуанозинфосфорибозилтрансферазу (ГГФРТ), резистентну до 8-азагуаніну (АГ), чи тимідинкиназу (ТК), резистентну до 5-бромдезоксиуридину (БдУ). Вихідні батьківські клітини не можуть рости в середовищі, що містить гіпоксантин — перетворений пурин, тимідин — перетворений пірімідин і аміноптерин (середовище ГАТ). Аміноптерин блокує синтез гіпоксантину і тимідину, а під час відсутності ферменту ГГФРТ і (чи) ТК клітини не можуть використовувати ці речовини, що містяться у середовищі. З вихідних ліній батьківських клітин, що знаходяться в середовищі ГАТ, резистентних до АГ (ГГФРТ/ТК+) і резистентних до БдУ (ТК/ГГФРТ+), здатність до поділу будуть зберігати лише клітинні гібриди, утворені в результаті злиття вихідних клітинних ліній. Лінії ГГФРТ- і ТК- вже отримані для мишей, пацюків, золотавого і китайського хом’яків, а також для людини. За методикою, аналогічній описаній, з використанням поліетиленгліколю замість вірусу Сендай для індукування процесу злиття батьківських клітин отримані антитіла для великої кількості антигенів. На кількість у селезінці В-лімфоцитів, що взаємодіють з певним антигеном, впливає тривалість інтервалу між останньою імунізацією тварини і моментом узяття спленоцитів. Остання обставина впливає на чистоту утворення гібридом, що синтезують відповідні антитіла.
Крім описаних, є дані про можливість одержання гібридом шляхом злиття з мієломними клітинами селезінкових клітин, імунізованих антигенами in vitro. Кількість антигену для одержання імунної відповіді в цьому випадку значно зменшується. Для перетворення лінії клітин, що секретує антитіла, немає потреби проводити їхню гібридизацію з мієломними клітинами. За допомогою вірусу Епштейна-Барра можлива пряма трансформація клітин, які секретують антитіла, специфічні до дифтерійного і правцевого токсинів. Тривала підтримка у функціонально активному стані клітинної культури Т-лімфоцитів за допомогою додаткових ростових факторів свідчить про те, що в недалекому майбутньому можна буде одержувати безперервно клони В-лімфоцитів, які спроможні до безперервного поділу.
Як зазначає Овчинников Ю.А. (1982), гібриди є тільки одним з варіантів використання культури клітин у біотехнології. За допомогою гібридомної біотехнології можлива регуляція імунної відповіді за рахунок одержання моноклональних антитіл заданої специфічності.
Моноклональні антитіла є тим видом біотехнологічної продукції, яку з успіхом використовують як у науково-дослідній роботі, так і для задоволення потреб виробництва. Моноклональні антитіла застосовуються при проведенні ідентифікації молекул, що цікавлять дослідника, для очищення потрібних антигенів (для детального аналізу їхньої структури і функцій), для з’ясування механізмів диференціації клітин в онтогенезі і поділу різних типів клітин імунної системи. Моноклональні антитіла, що секретуються культурою гібридомних клітин, є високоефективним і високочутливим діагностичним препаратом. Вони можуть використовуватися як профілактичні та лікувальні засоби, а також для одержання імуносорбентів, ферментних препаратів, інтерферонів, гормонів та інших біологічно активних речовин (можна використовувати культури тваринних і рослинних клітин).