Введение в молекулярную биологию: От клеток к атомам - Энтони Рис, Майкл Стернберг 2002
Белки
Конформация пептидов
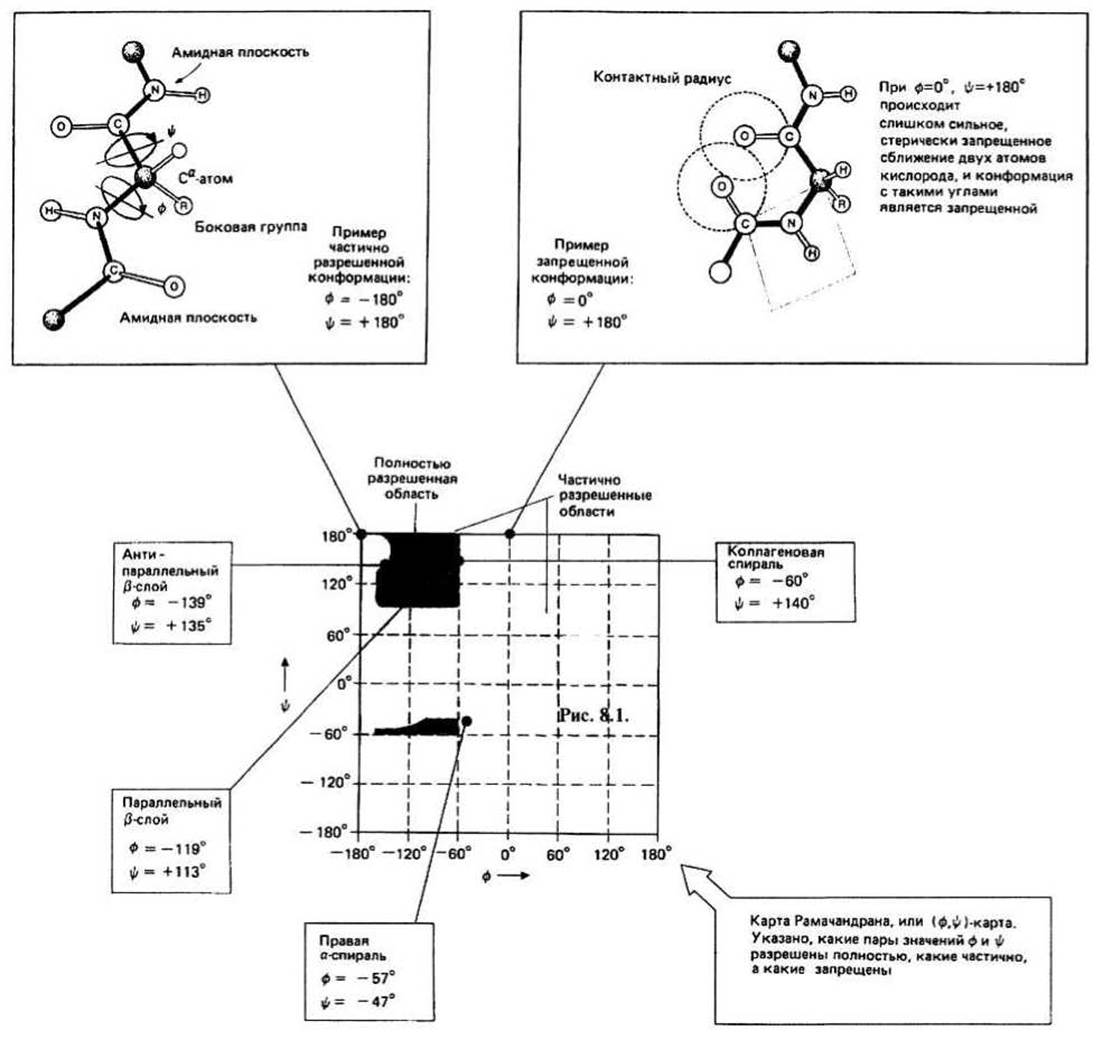
Рис. 8.1
Конформациями молекулы называются такие варианты расположения в пространстве составляющих молекулу атомов, которые могут быть получены один из другого вращением вокруг одинарных ковалентных связей. В противоположность этому конфигурации — это такие варианты взаимного расположения атомов молекулы, переходы между которыми требуют разрыва и образования ковалентных связей. Так, D- и L-изомеры аминокислотных остатков (гл. 6) представляют собой различные конфигурации, а а-спираль и коллагеновая спираль (см. ниже) — различные конформации полипептидной цепи.
Пептидной связью называется связь между >С=О-группой одного остатка и >N—Н-группой следующего. Эта С—N-связь вопреки ожиданиям не является одинарной, а в силу резонанса оказывается частично двойной (С—N). При этом соответственно уменьшается порядок двойной связи С=О. Такое изменение порядка связей вызвано тем, что одна пара электронов связи С=О распределяется между атомами О, С и N. Вследствие этого перераспределения атомы О, С, N, Н (пептидная группа) и связанные с ними ковалентно два Са-атома оказываются лежащими в одной плоскости, называемой амидной, а вращение вокруг связи O*N становится запрещенным. Предположение о планарности пептидной группы было высказано Полингом и Кори. Они заметили, что длина пептидной связи (0,132 нм) имеет промежуточное значение между длиной одинарной С—N-связи (0,149 нм) и двойной С=Ы-связи (0,127 нм).

Рис. 8.2.
Транс-конформации пептидной группы. Са-атомы, примыкающие с двух сторон к одной пептидной группе, обычно находятся в трансконформации по отношению друг к другу. Альтернативная Лис-конформация невыгодна из-за слишком сильного сближения объемных групп, присоединенных к Са-атомам.
Рис. 8.3.
Са-атом связан одинарными связями с - атомом одной пептидной группы и с С-атомом следующей. Вокруг этих одинарных связей возможно относительно свободное вращение.
Углы ф и Ψ. Для описания вращения вокруг связей N—Са и Са—С используются соответственно углы ф (фи) и Ψ(пси). Угол ф задает положение всех атомов, которые лежат в амидной плоскости, предшествующей Са-атому, а угол Ψ определяет положение всех атомов амидной плоскости, следующей за Са-атомом. Некоторые пары значений ф и Ψ запрещены, поскольку при этом имеют место стерические ограничения из-за сближения двух атомов на расстояние, меньшее чем сумма их контактных (т. е. вандерваальсовых) радиусов. Например, при ф = 0°, Ψ= 180° возникают стерические контакты между двумя атомами кислорода.
Конформационная карта Рамачандрана, или (ф, Ψ) - карта, показывает, какие пары значений ф и Ψ разрешены. Эта карта названа именем индийского ученого, рассчитавшего допустимые значения углов ф и Ψ. Каждая точка на карте соответствует определенной паре значений ф и Ψ и показывает, является ли данное взаимное расположение атомов двух амидных плоскостей и боковой группы, присоединенных к Са-атому, энергетически выгодным. Приведенная на рис. 8.1 (ф, Ψ) - карта характерна для большинства боковых цепей, за исключением глицина и пролина. В случае полностью разрешенных конформаций нежелательные контакты между атомами отсутствуют. Запрещенные углы (например, ф = 0°, Ψ = 180°) соответствуют конформациям, в которых отдельные атомы находятся друг от друга на расстоянии, меньшем суммы их контактных радиусов. Необходимо отметить что, поскольку атомы не являются жесткими сферами, возможно сближение их на расстояние, несколько меньшее суммы контактных радиусов. Хотя подобное сближение нежелательно, оно тем не менее может иметь место, а соответствующие конформаций называются частично разрешенными (например, ф = —180°, Ψ = 180°). Если каждую полностью разрешенную пару значений ф и Ψ представить на карте темно-коричневой точкой, то получающиеся в результате темно-коричневые участки будут отвечать полностью разрешенным областям значений углов ф и Ψ. Частично разрешенные области значений углов ф и Ψ отмечены на карте светло-коричневым цветом. Следует подчеркнуть, что (ф, Ψ) - карты указывают разрешенные пары значений ф и Ψ для данного конкретного остатка. Боковая цепь глицина, состоящая лишь из одного атома водорода, по размеру меньше, чем у любого ж другого остатка. Поэтому на (ф, Ψ) - карте для глицина больше разрешенных областей, чем на картах других остатков. Напротив, в случае пролина ограничения, налагаемые ковалентной связью между атомом углерода боковой цепи и атомом азота основной цепи, приводят к значительному уменьшению размеров разрешенных областей.
Регулярные или спиральные структуры нескольких соседних вдоль цепи остатков значения ф и Ψ окажутся одинаковыми, то в пределах этого участка у каждого Са-атома основная цепь будет поворачиваться на один и тот же угол. В результате получится регулярная вторичная структура. Подобные структуры часто обнаруживаются в глобулярных и фибриллярных белках. Особенно важное значение имеют параллельная и антипараллельная (ß-структуры (гл. 9), а-спираль (гл. 9) и коллагеновая спираль (гл. 11). Значения углов ф и Ψ, соответствующие эти типам вторичной структуры, приведены на рис. 8.1.