Основы биохимической инженерии Часть 1 - Бейли Дж., Оллис Д. 1989
Применение реакций, катализируемых ферментами
Технологические процессы с участием иммобилизованных ферментов
Промышленные процессы
Катализаторы на основе иммобилизованных ферментов уже используются в той или иной мере в ряде крупномасштабных промышленных производств. К числу наиболее важных областей применения иммобилизованных ферментов относятся производство сиропа с высоким содержанием фруктозы из кукурузного крахмала и производство L-аминокислот путем разделения рацемических смесей (состоящих из L- и D-изомеров). Кроме того, в производстве полусинтетических пенициллинов применяют иммобилизованную пенициллинацилазу. С экономической точки зрения наиболее важна первая из упомянутых областей.
Сахар (сахарозу) нельзя заменить d-глюкозой, поскольку глюкоза менее сладка. К тому же кристаллизация концентрированных растворов глюкозы может затруднить их последующую переработку и хранение. Эти осложнения в значительной мере могут быть устранены, если глюкозу частично изомеризовать во фруктозу с помощью фермента глюкозоизомеразы:
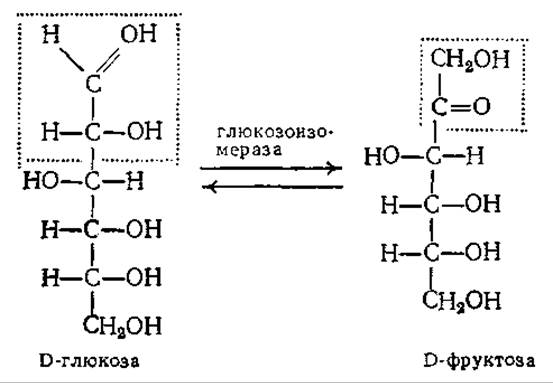
При 50 °С константа равновесия этой реакции близка к единице, и изменение температуры практически не влияет на нее, поскольку теплота реакции изомеризации составляет всего лишь, около 1 ккал/моль. Поэтому продуктом реакции является смесь глюкозы и фруктозы в отношении приблизительно 1:1. Такая смесь значительно более сладка, чем чистая глюкоза, и может с успехом заменять сахар в самых различных областях, в том числе в производстве безалкогольных напитков, приготовлении различных пищевых продуктов и в хлебопекарной промышленности. Еще более сладкие смеси можно получать путем хроматографического разделения (гл. 11) продуктов изомеризации, приводящего к обогащению смеси фруктозой.
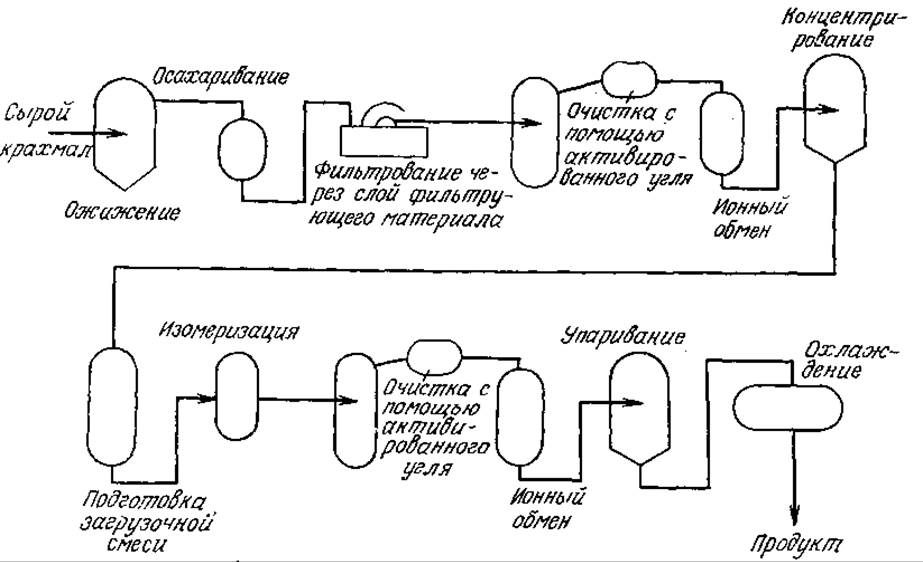
РИС. 4.10. Схема процесса производства кукурузного сиропа с высоким содержанием фруктозы с помощью глюкозоизомеразы. [Воспроизведено из статьи: Harden J. D. On-Line Control Optimizes Processing; Food Eng., 44, 59 (1972).]
Глюкозоизомераза представляет собой внутриклеточный фермент, продуцируемый рядом микроорганизмов, из которых используются главным образом некоторые штаммы Arłhrobacter и Streptomyces. Необходимость дезинтеграции клеток достаточно мягкими методами, не вызывающими необратимую инактивацию фермента, приводит к существенному повышению стоимости глюкозоизомеразы по сравнению, например, с внеклеточными гидролазами. К тому же глюкозоизомераза очень чувствительна к ряду ингибиторов. Оба этих фактора предполагают целесообразность иммобилизации глюкозоизомеразы и ведения процесса в строю контролируемых условиях. Изучены различные методы иммобилизации глюкозоизомеразы, в том числе и метод, основанный на применении содержащих фермент целых клеток, закрепленных в свою очередь в коллагене или с помощью какого-либо другого флокулирующего и связывающего агента. Такой прием может служить примером еще одного подхода к иммобилизации внутриклеточных ферментов, заключающегося в иммобилизации продуцирующих этот фермент клеток (обычно обработанных с целью снижения сопротивления клеточных мембран массообмену) или лизатов таких клеток. К проблеме иммобилизации клеток мы еще вернемся в гл. 9.
На рис. 4.10 приведена схема процесса производства кукурузного сиропа с высоким содержанием фруктозы, основанного на использовании иммобилизованной глюкозоизомеразы. Здесь необходимость множества операций разделения и обработки промежуточных продуктов между стадиями осахаривания и изомеризации диктуется свойствами ферментных систем. Так, для повышения термической устойчивости а-амилазы, применяемой для гидролиза крахмала (обычно этот процесс проводят при температуре около 105°С), добавляют ионы кальция. Последние, однако, ингибируют глюкозоизомеразу, и поэтому их связывают ионообменными смолами прежде, чем декстрозный раствор поступит в реактор изомеризации.
Пример 4.2. Параметры процесса изомеризации глюкозы в реакторе в присутствии иммобилизованной глюкозоизомеразы*. Для выбора типа катализатора, конструкции реактора и условий каталитического процесса в реакторе потребовалось тщательное изучение множества взаимосвязанных параметров. В табл. 4П2.1 перечислены некоторые из параметров и критериев, которые учитывались ранее при проектировании реакторов для получения кукурузного сиропа с высоким содержанием фруктозы с помощью иммобилизованной глюкозоизомеразы. В табл. 4П2.2 указаны основные свойства катализатора, выбранного в результате анализа перечисленных параметров в ходе разработки проекта компанией Н. J. Heinz Company. Выбранный размер частиц катализатора удовлетворяет двум взаимоисключающим требованиям: с одной стороны, частицы катализатора достаточно малы, чтобы скорость диффузии не лимитировала скорость всего процесса, а с другой — их размеры достаточно велики, чтобы удалось свести к минимуму перепад давлений на реакторе колонного типа со слоем иммобилизованного фермента.
Найденные оптимальные условия реакции суммированы в табл. 4П2.3. Обратите внимание на необходимость высокого содержания глюкозы в поступающей в реактор смеси; присутствие в последней более 10% олигосахаридов существенно снижает активность фермента. Большой диапазон времени контакта катализатора с субстратом объясняется постепенной инактивацией катализатора. С течением времени активность фермента падает и при постоянной скорости потока реагентов степень превращения субстрата постепенно снижается. Поэтому для обеспечения необходимого качества продукции по мере инактивации фермента время его контакта с субстратом увеличивают путем уменьшения скорости потока. Соответствующие математические выражения, позволяющие количественно оценить взаимосвязь между активностью, временем контакта и степенью превращения для различных типов ферментных катализаторов, мы рассмотрим в гл. 9.
* Venkatasubramanian К., Harrow Н. S., Design and Operation of a Commercial Immobilized Glucose Isomerase Reactor System, Ann. N.Y. Acad. Sсi., 326, 141 (1979).
Таблица 4П2.1. Параметры, изучавшиеся в ходе проектирования реактора с иммобилизованной глюкозоизомеразойа
Биохимические параметры |
1. Активность |
2. Стабильность фермента в процессе работы реактора (время жизни катализатора) и зависимость инактивации от времени |
3. Производительность в используемом диапазоне времени жизни |
4. Оптимальная концентрация субстрата |
5. Влияние концентрации олигосахаридов |
6. Влияние растворенного кислорода |
7. Минимальное и максимальное время контакта с субстратом |
8. Образование побочных продуктов реакции |
9. Чувствительность к изменению pH и температуры |
10. Устойчивость при хранении |
11. Вымывание фермента |
12. Рост микроорганизмов (если таковой вообще наблюдается) |
13. Характеристики потока на выходе из реактора (состав, цвет, запах, содержание белков, pH и т. п.). |
Механические параметры |
1. Размер, форма частиц и их распределение по размерам |
2. Насыпная масса в сухом и влажном виде |
3. Набухание |
4. Сжимаемость |
5. Когезия |
6. Истирание частиц |
Гидромеханические параметры |
1. Перепад давлений |
2. Тип потока (восходящий или нисходящий) |
3. Уплотнение слоя |
4. Осевая дисперсия и каналообразование |
5. Распределение времени пребывания |
6. Расслаивание |
7. Отношение длины к диаметру |
8. Минимальная скорость начала псевдоожижения |
а Воспроизведено с разрешения из статьи: Venkatasubramanian К., Harrow Н. S., Design and Operation of a Commercial Immobilized Glucose Isomerase Reactor System, Ann. N. Y. Acad. Sсi., 326, 141 (1979).
Размеры реактора колонного типа определяются гидромеханическими свойствами слоя катализатора. При нисходящем потоке реакционной смеси слой ферментного иммобилизованного катализатора способен сжиматься под давлением; в результате сопротивление потоку возрастает. На рис. 4П2.1 изображена зависимость перепада давлений на колонне от высоты слоя катализатора при максимальной скорости потока, допустимой в случае свежего катализатора. Если перепад давления на колонне превышает 0,2 кг/см2, то сопротивление колонны резко возрастает. Отсюда следует, что максимальная высота слоя катализатора должна составлять около 4,6 м. Учитывая известное время контакта катализатора с субстратом и заданную производительность всей установки, нетрудно определить размеры необходимых колонных реакторов и их число. В силу упоминавшихся выше процессов инактивации катализатора целесообразно устанавливать несколько колонн, так чтобы они инактивировались (и заменялись) последовательно; это позволит максимальным образом использовать катализатор и в то же время обеспечить постоянную высокую производительность установки в целом.
Таблица 4П2.2. Физические и каталитические свойства иммобилазы — катализатора с глюкозоизомеразной активностью (продукт фирмы ІСІ)а
Форма катализатора |
Сухие гранулы |
Внешний вид |
Окрашен в желто-коричневый цвет |
Размер частиц, меш |
Номинальный размер 12X20 (цилиндрические гранулы диаметром* около 1 мм, длиной около 2,5 мм) |
Объемная плотность в сухом состоянии, г/см3 |
0,64—0,72 |
Объемная плотность во влажном состоянии, г/см3 |
0,2 (±10%) |
Характерный размер пор, мкм |
0,2 |
Активностьб, ед./г |
Не менее 0,04 |
Производительность |
В среднем до 907 кг 42%-ного обогащенного фруктозой сиропа на 0,45 кг фермента в течение 1000 ч |
Объем пустот в слое, % |
Около 45% |
а Воспроизведено из статьи: Venkatasubramanian К., Harrow Н. S., Design and Operation of a Commercial Immobilized Glucose Isomerase Reactor System, Ann. N. Y. Acad. Sсi., 326, 141 (1979).
б Единица активности определяется как количество катализатора, способное превратить 10-9 молей субстрата в I мин при 60 °С и pH 8,0.
Таблица 4П2.3. Условия реакции изомеризации глюкозного сиропа в реакторе колонного типа в слое иммобилизованного фермента3
Содержание сухого вещества, % |
40—45 |
Содержание глюкозы в исходной смеси, % |
93—96 |
Требования к исходной смеси |
Смесь необходимо очистить фильтрованием, обработкой активированным углем и методом ионного обмена |
pH |
8,2—8,5 |
Падение pH |
На 0,2—0,4 |
Температура, °С |
60 |
Активатор |
0,0004 М Mg2+ |
Время контакта фермента с субстратом, ч |
0,5—4 |
а Воспроизведено с разрешения из статьи: Venkatasubramanian К., Harrow Н. S.,. Design and Operation of a Commersial Immobilized Glucose Isomerase Reactor Svstem, Ann. N. Y. Acad. Sсi., 326, 141 (1979).
Потребность в L-аминокислотах для производства пищевых, продуктов и в медицинских целях постоянно возрастает. В связи с этим большое внимание уделяется разработке как микробиологических, так и химических методов получения L-аминокислот. Недостатком химических методов является рацемическая природа синтетических аминокислот. В общем случае D-изомеры не имеют питательной ценности, поэтому желательно получать только физиологически активные L-аминокислоты.
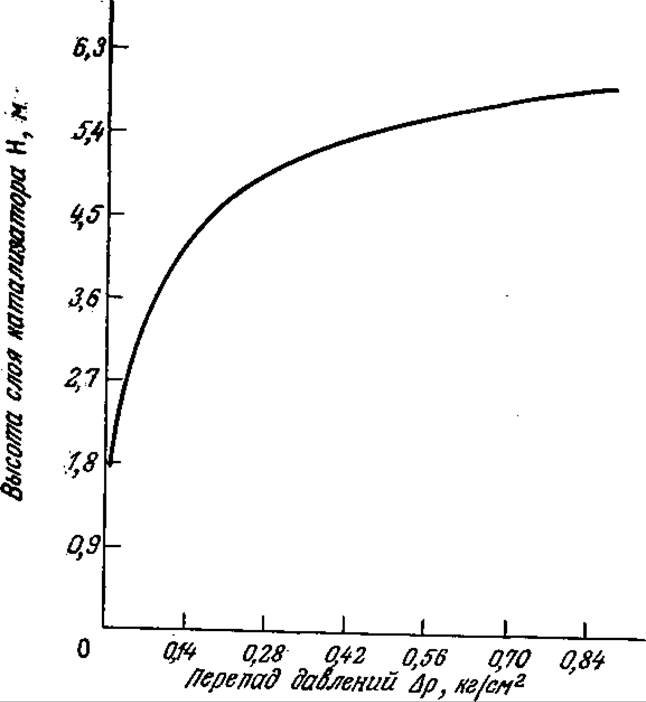
РИС. 4П2.1. Зависимость перепада давления в колонне от высоты слоя катализатора; колонна с нисходящим потоком раствора заполнена гранулами иммобилизованной глюкозоизомеразы. [Воспроизведено с разрешения из статьи: Venkatasubramanian К., Harrow Н. S., Design and Operation of a Commercial Immobilized Glucose Isomerase Reactor System; Ann. N.Y. Acad. Sci., 326, 1141 (1979).]
Указанная цель была достигнута в процессе, разработанном фирмой Tanabe Seiyaku Со., Ltd. (Осака, Япония), в котором впервые в промышленном масштабе применялись иммобилизованные ферменты и результаты которого были опубликованы в печати. Основой процесса является метод разделения оптических изомеров в соответствии со следующей реакцией, катализируемой ферментом аминоацилазой:
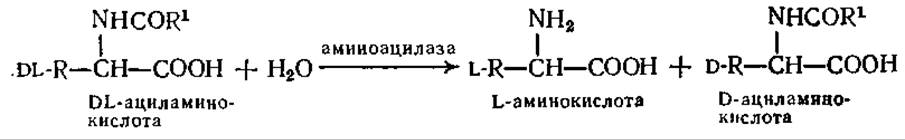

РИС. 4.11. Реакторы колонного типа с иммобилизованным ферментом, применяющиеся фирмой Tanabe Seiyaku Со., Ltd. в производстве L-аминокислот. (Фотография любезно предоставлена доктором И. Шибатой из фирмы Tanabe Seiyaku Со., Ltd.)
Эту реакцию осуществляют в реакторе колонного типа с иммобилизованной аминоацилазой (рис. 4.11), после чего основной продукт реакции, L-а минокислоту, отделяют от негидролизованной D-ациламинокислоты, используя их различные растворимости. Затем D-ациламинокислоту рацемизуют до DL-ациламино-кислоты, которая снова поступает в колонну с аминоацилазой. Общая схема процесса приведена на рис. 4.12.
Чтобы найти оптимальную форму иммобилизованного фермента для этого процесса, Шибата, Тоса и их сотрудники из фирмы Tanabe Seiyaku провели обширные исследования, результаты которых частично изложены в опубликованной ими статье [16]. В табл. 4.12 суммированы их выводы о свойствах различных форм иммобилизованных ферментов. Эти данные еще раз говорят о том, что при подборе катализатора для промышленного использования помимо начальной активности необходимо учитывать и многие другие факторы. В рассматриваемом случае в конечном итоге исследователи остановились на аминоацилазе, иммобилизованной ионными связями на DEAE-сефадексе, в силу высокой активности, простоты получения, возможности регенерации и устойчивости такого катализатора. В 1978 г. представители компании Tanabe Seiyaku сообщили, что этот катализатор используется уже более пяти лет без какого-либо механического разрушения и снижения (связывающей) активности.
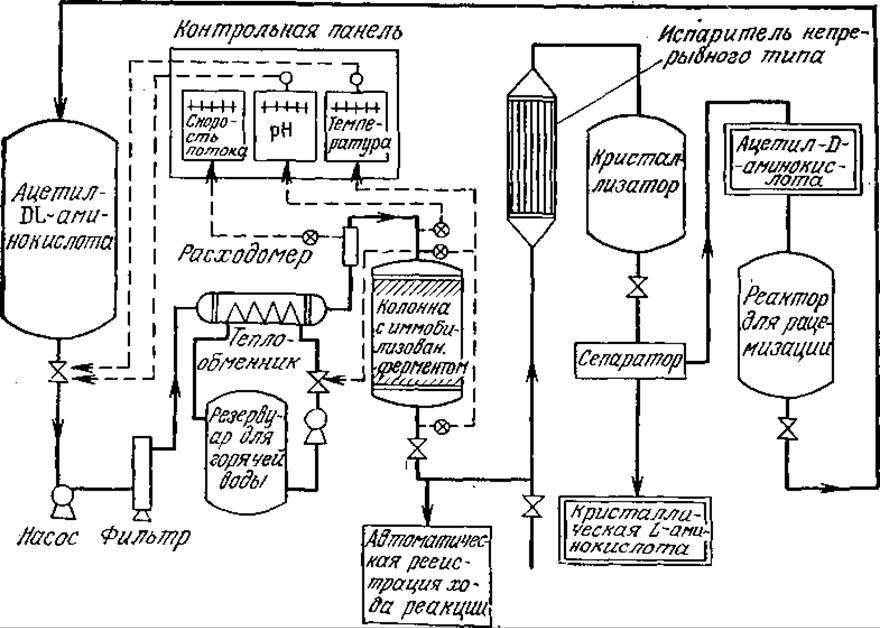
РИС. 4.12. Технологическая схема процесса с применением иммобилизованной аминоацилазы, реализованного фирмой Tanabe Seiyaku. [Воспроизведено с разрешения из работы: Chibata I. et al, Preparation and Industrial Application of Immobilized Aminoacylases, in Fermentation Technology Today, Terui G. (ed.), p. 387, Society of Fermentation Technology, Japan, Osaka, Japan, 1972.]
В 1983 г. было опубликовано сообщение о первом промышленном процессе с применением ферментов, иммобилизованных полупроницаемыми мембранами. В данном случае речь шла о процессе превращения N-ацетил-DL-метионина в L-метионин с помощью ацилазного фермента. Изучены возможности применения иммобилизованных ферментов во многих других химико-технологических процессах (табл. 4.13). Некоторые из этих возможностей уже реализованы в промышленности, другие находятся на стадиях разработки и внедрения.
Таблица 4.12. Свойства различных форм аминоацилазы (субстрат — ацетил- DL-метионин)а
|
Иммобилизованные аминоацилазы |
||||
Свойства |
Нативная аминоацилаза |
Ионное связывание (на DEAE-сефадексе) |
Ковалентное связывание (с иодацетил-целлюлозой) |
Фермент, включенный в полиакриламидный гель |
Оптимальный pH |
7,5—8,0 |
0,7 |
7,5—8,5 |
О |
Оптимальная температура, °С |
60 |
72 |
55 |
65 |
Энергия активации, ккал/моль |
6,9 |
7,0 |
3,9 |
5,3 |
Оптимальная концентрация Со2+, мМ. |
0,5 |
0,5 |
0,5 |
0,5 |
Кm, мМ |
5,7 |
8,7 |
6,7 |
5,0 |
vmах, мкмоль/ч |
1,52 |
3,33 |
4,65 |
2,33 |
Методика получения |
Простая |
Сложная |
Сложная |
|
Связывающие силы |
Слабые |
Сильные |
Сильные |
|
Возможность регенерации |
Возможна |
Невозможна |
Невозможна |
|
а Воспроизведено из статьи: Morl Т., Sato Т., Tosa Т., Chibata І., Studies on Immobilized Enzymes X: Preparation and Properties of Aminoacylase Entrapped into Acrylamide Gel-Lattice, Enzymologia, 43, 213 (1972).