Основы биохимической инженерии Часть 1 - Бейли Дж., Оллис Д. 1989
Стехиометрия и энергетика метаболических превращений
Биосинтез
Биосинтез низкомолекулярных соединений
Во вводных разделах мы отмечали, что большинство процессов в мире микроорганизмов характеризуются 1) утилизацией субстратов или питательных веществ, 2) ростом клеток и 3) выделением в среду продуктов их метаболизма. Биосинтез связан со всеми этими тремя сторонами жизнедеятельности клеток. Необходимость в питательных веществах определяется потребностями клетки в веществах-предшественниках, запасах химической энергии и восстанавливающих эквивалентах. Некоторые продукты биосинтеза клетка выделяет в среду. Наконец, скорость биосинтеза определяет скорость образования новых компонентов клетки и, таким образом, темпы клеточного роста. Скорости роста клеток изменяются в очень широких пределах; так, бактерии Е. coli могут делиться каждые 20 мин, жизненный цикл клеток печени крысы составляет от двух до трех месяцев, а нервные клетки взрослого человека вообще не самовоспроизводятся. Даже в последнем случае, однако, необходимость в биосинтезе не отпадает; здесь он нужен для поддержания жизнедеятельности клеток и восстановления повреждений.
Для биосинтетических целей клетка использует химические ресурсы, образующиеся в процессах катаболизма. Как правило, реакции синтеза термодинамически невыгодны и протекают только одновременно с гидролизом АТР до ADP или АМР. При гидролизе образующегося в последнем случае пирофосфата (Р~Р) выделяется дополнительная свободная энергия (∆G⁰' ≈ 7 ккал/моль), также использующаяся для «запуска» реакций синтеза. Поскольку питательные вещества обычно окислены в большей степени, чем необходимые клетке соединения, то для биосинтеза последних нужны и восстанавливающие эквиваленты.
Биологически важные низкомолекулярные соединения в основном являются мономерами и используются клеткой для построения биополимеров. Для этой цели необходимо в общей сложности примерно 70 различных соединений: 4 рибонуклеотида, 4 дезоксирибонуклеотида, 20 аминокислот, около 15 моносахаридов и около 20 жирных кислот и других предшественников липидов. Кроме того, в реакциях второго типа должны синтезироваться ATP, NAD, другие соединения-переносчики и коферменты. Все эти вещества называют центральными промежуточными метаболитами. В настоящем разделе мы рассмотрим некоторые основные пути биосинтеза промежуточных метаболитов и организацию этих путей.
Аминокислоты можно разделить на четыре группы, различающиеся химическим строением и природой биосинтетических предшественников. Как мы увидим позднее в ходе обсуждения регуляции метаболизма, синтез аминокислот каждой группы осуществляется с помощью разветвленной последовательности регулируемых реакций. Биосинтез всех аминокислот начинается с промежуточных соединений в метаболизме углерода (см. схему на рис. 5.11).
Живые клетки усваивают азот путем его включения в аминокислоты глутамин и глутаминовую кислоту. Сначала при взаимодействии аммиака с a-кетоглутаровой кислотой (одним из промежуточных веществ в цикле трикарбоновых кислот) образуeтcя глутаминовая кислота:
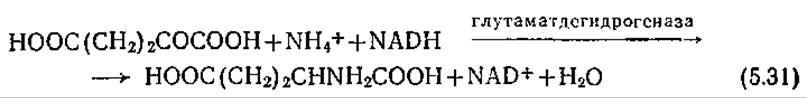
Глутаминовая кислота может связать еще один аммониевый ион и превратиться в глутамин:
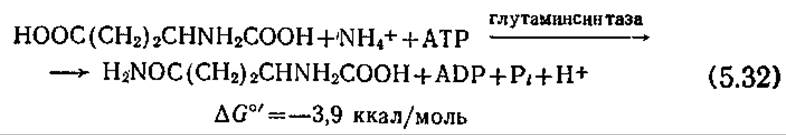
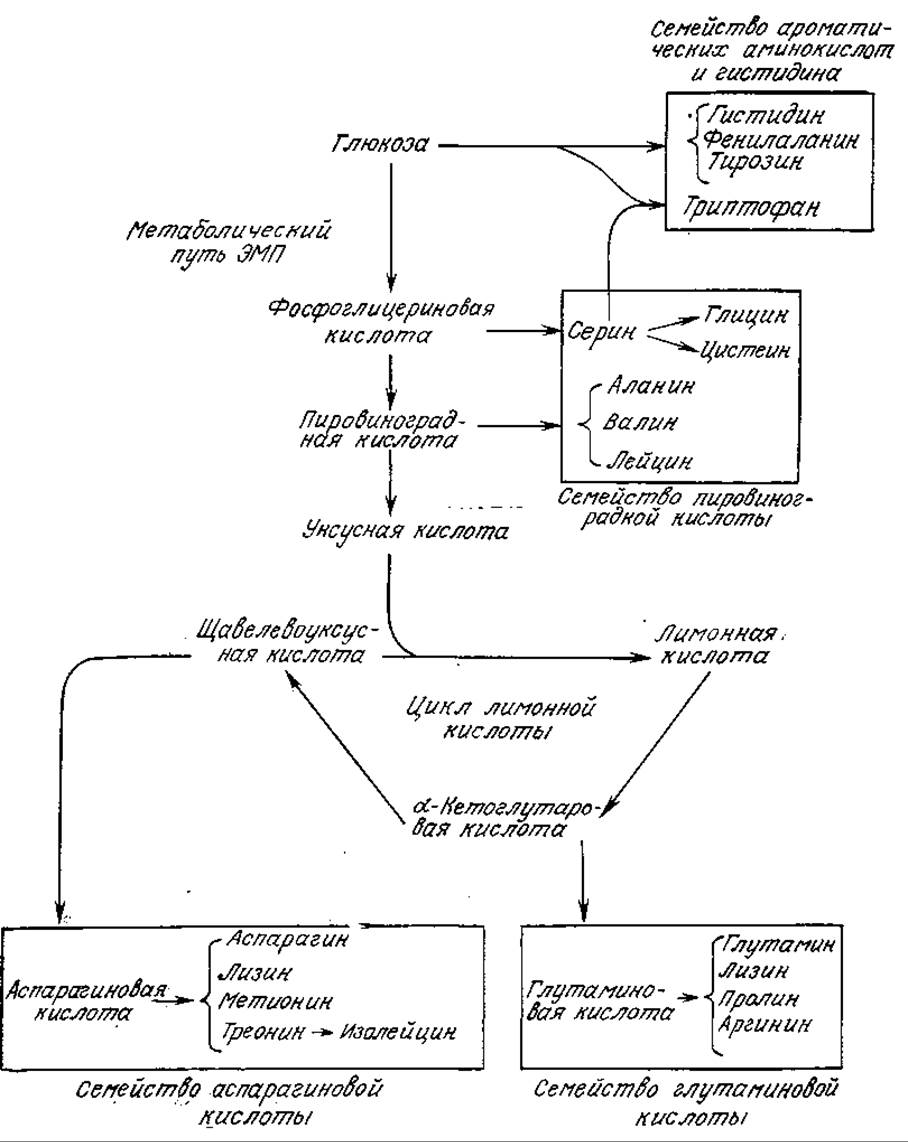
РИС. 5.11. Семейства аминокислот и их предшественники — углеводы. (Стент Г., Кэлиндар Р., Молекулярная генетика. — М.: Мир, 1981.)
Вторая реакция, происходящая с поглощением метаболической энергии, осуществляется при недостатке аммиака в среде. В некоторых бактериях с участием NADH происходит непосредственное аминирование пирувата до аланина, а другие бактерии способны превращать фумарат в аспартат. Ряд микроорганизмов усваивает азот в виде нитрата NО3- и свободного азота N2; сейчас известно, однако, что эти питательные вещества сначала трансформируются в аммиак, который; затем и ассимилируется клетками по описанным выше путям.
Все другие аминокислоты образуются из глутамата или на основе его углеродного скелета, или путем переноса аминогруппы к другим молекулам. Например, глутамат превращается в пролин в результате двух последовательных катализируемых ферментами реакций и одной неферментативной гидролитической реакции по общему уравнению:
C5NH8O4- + ATP + 2(NADPH + H+) →
→C5NH8O2- + ADP + Pi + 2NADP+ + H2O (5.33)
В большинстве организмов аланин и аспартат образуются путем переаминирования глутамата:
Глутамат+оксалоацетат → а-кетоглутарат + аспартат
Глутамат+пируват → а-кетоглутарат + аланин
Все реакции переаминирования происходят только в присутствии кофермента пиридоксальфосфата, производного витамина В6 (пиридоксаля).
В завершение этого краткого обзора биосинтеза аминокислот на рис. 5.12 приведены некоторые отдельные стадии и общая схема биосинтеза аминокислот семейства аспарагиновой кислоты; здесь обращает на себя внимание тот факт, что большинство стадий протекает с участием АТР или NADPH. На этом рисунке штриховыми линиями обозначены регуляторные механизмы, которые мы обсудим позднее.
Сколько-нибудь детальное изучение путей биосинтеза нуклеотидов выходит за рамки тематики этой книги. Источники предшественников этих соединений указаны на рис. 5.13. Более подробные сведения читатель может найти в литературе.
В биосинтезе жирных кислот и других предшественников липидов роль исходных веществ выполняют ацетил-СоА и глицерин. Чтобы еще раз подчеркнуть участие АТР и NADPH в в биосинтезе, мы несколько подробнее рассмотрим путь биосинтеза самой обычной из жирных кислот — пальмитиновой СН3(СН2)14СООН. Первая сталия этого пути заключается в карбоксилировании ацетил-СоА, в результате чего образуется малонил-СоА:
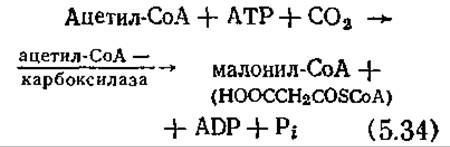
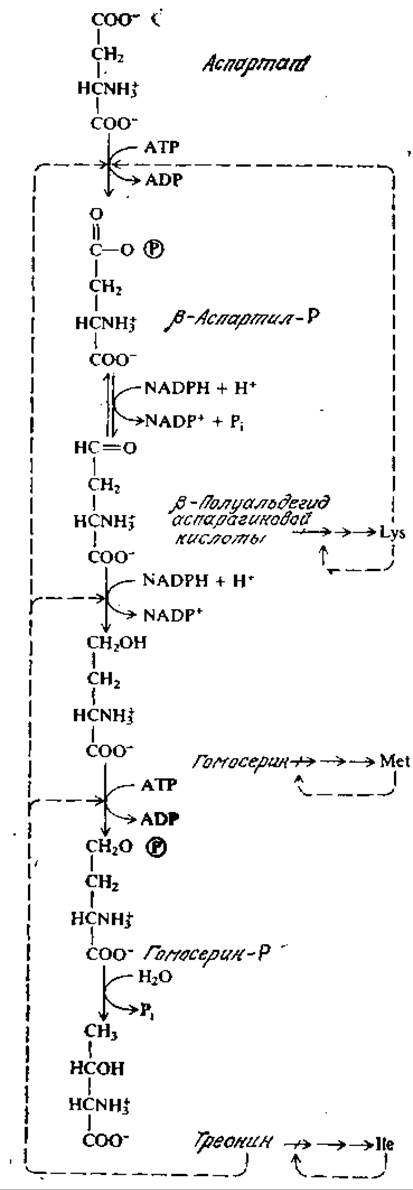
Рис. 5.12. Схема реакций, в ходе которых аспартат превращается в лизин, гомосерин, метионин, треонин и изолейцин. (Воспроизведено с разрешения из работы: Wood W. В., Willson J. H., Benbow В. M., Hood L. E., Biochemistry, A Problems Approach, 2d ed p. 294, Benjamin/Cummings Publishing Co., Menlo Park, CA, 1981.)
Далее из семи молекул малонил-СоА и одной молекулы ацетил-СоА образуется пальмитат. Этот процесс осуществляется ступенчато, а его конечный результат можно выразить следующим уравнением:
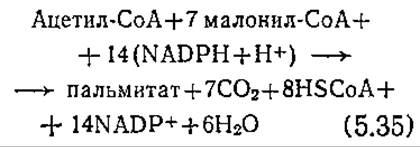
Обратите внимание на то, что в этом процессе в соответствии с уравнением (5.34) на каждую молекулу образующегося малонил-СоА расходуется одна молекула макроэргического фосфата.
В завершение этого краткого обзора биосинтеза рассмотрим пути образования глюкозы и родственных соединений. Мы уже знаем, что продукты катаболизма глюкозы являются важнейшими предшественниками в биосинтезе аминокислот, нуклеотидов и жирных кислот. Следовательно, организмы, растущие на других источниках углерода, например СО2, должны превращать их в глюкозу или в один из ближайших продуктов ее метаболизма. Кроме того, при избытке соединений углерода (по сравнению с другими питательными веществами) многие клетки превращают глюкозу в резервные углеводы и хранят их для последующего использования.
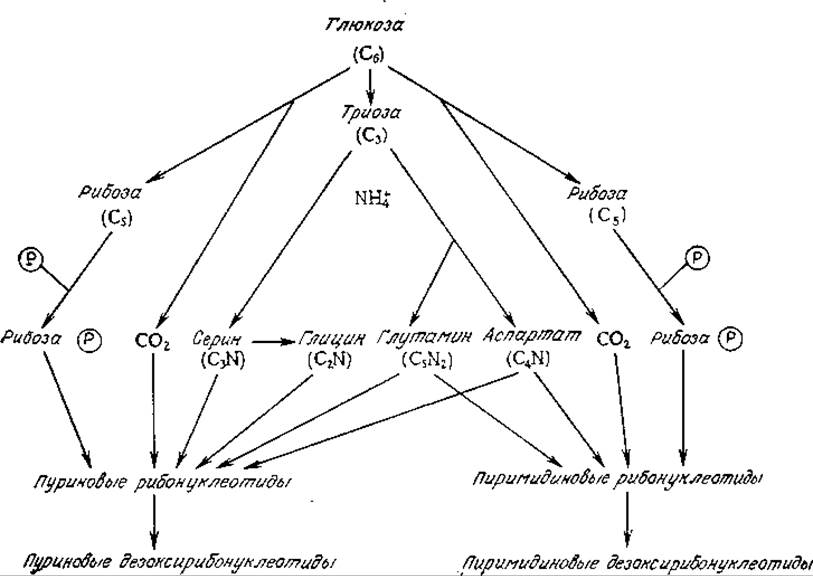
РИС. 5.13. Схема превращения веществ-предшественников в нуклеотиды и дезоксирибонуклеотиды. [Воспроизведено с разрешения из работы: Biochemistry of Bacterial Growth, Mandelstam J., McQuillan K. (eds.), 2d ed., p. 33, Blackwell Scientific Publications, Oxford, 1973.]
Глюконеогенезом называют синтез глюкозы в хемотрофах. Интересно, что в синтезе глюкозы из пирувата участвуют все промежуточные соединения, типичные для метаболического пути ЭМП. Еще более важен тот факт, что все ферменты, катализирующие практически равновесные превращения в пути ЭМП, катализируют обратимые реакции и в биосинтезе глюкозы. В то же время в биосинтезе глюкозы реакции фосфорилирования и дефосфорилирования несколько отличаются от аналогичных реакций в гликолизе и катализируются другими ферментами. Эти биосинтетические реакции, изображенные на рис. 5.14 (снизу-вверх), происходят спонтанно и сопровождаются уменьшением свободной энергии. Общая стехиометрия глюконеогенеза показывает, что в целом процесс сопровождается поглощением энергии и не является повторением пути ЭМП в обратном направлении (GTP — гуанозинтрифосфат):
2 Пиpyват + 4ATP + 2GTP + 2NADH + 2H+ + 4H2О →
→ глюкозa + 2NAD+ + 2GDP + 4ADP + 6Pі (5.36)
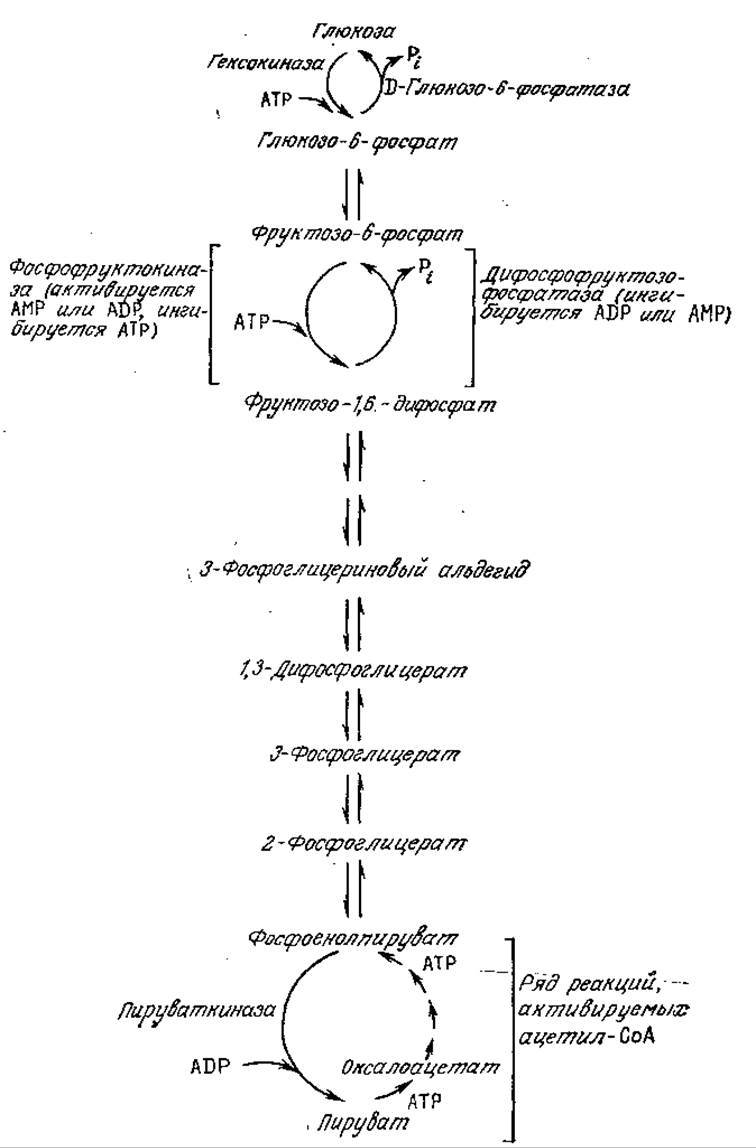
РИС. 5.14. Расщепление глюкозы по пути гликолиза (сверху вниз) и биосинтез глюкозы (снизу-вверх). Для этих двух путей метаболизма характерна идентичность ряда реакций, особенно близких к равновесным. В то же время неравновесные реакции в зависимости от их направления катализируются различными ферментами (большей частью аллостерическими), что позволяет независимо регулировать процессы синтеза и расщепления глюкозы. (Воспроизведено из работы Lehninger A., Bioenergetics, 2d ed., р. 129, W. A. Benjamin, Inc., Palo Alto, CA, 1974.)
Наиболее важная биосинтетическая реакция — это синтез глюкозы из СО2 в растениях. Без этого процесса невозможно существование биосферы в том виде, в каком мы привыкли себе ее представлять. Кроме того, масштабы и эффективность этих реакций определяют объемы возобновляемых ресурсов углеродсодержащего сырья, служащего топливом и исходным материалом в биохимических и химических процессах.
Выше были описаны световые реакции фотосинтеза: поглощение света хлорофиллом и другими пигментами и формирование потока возбужденных электронов, генерирующего АТР и NADPH. Далее мы рассмотрим темповые реакции фотосинтеза, названные так потому, что они протекают и в отсутствие света до тех пор, пока в клетке имеется достаточный запас АТР и NADPH.
Первоначальное включение в цикл СО2 осуществляется в реакции с рибулозо-1,5-дифосфатом:
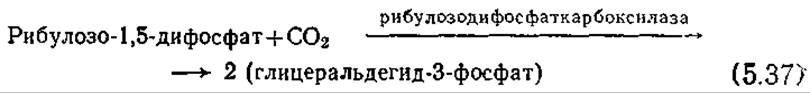
Образующийся на этой стадии глицеральдегид-3-фосфат может далее претерпевать несколько превращений, в частности включаться в аналогичную глюконеогенезу последовательность реакций, в результате которой образуется глюкоза. В реакциях цикла Калвина (рис. 5.15) регенерируется рибулозо-1,5-дифосфат, который может снова ассимилировать СО2 в соответствии с реакцией (5.37). В отличие от цикла ТКК, представляющего собой, по сути дела, источник АТР и NADH, в цикле Калвина расходуются как АТР, так и NADPH. Поскольку в одном цикле Калвина утилизируется одна молекула СО2, то для синтеза глюкозы необходимо повторить этот цикл шесть раз; тогда общее уравнение синтеза глюкозы будет выглядеть следующим образом:
6СО2 + 12NADPH + 12Н+ + 18АТР + 12Н2О →
→ С6Н12О6 + 12NADP+ + 18ADP + 18Рі (5.38)