Биохимия аминокислот - А. Майстер 1961
Промежуточный обмен аминокислот
Глицин, серин и саркозин
Глицин
Эти аминокислоты рассматриваются вместе, поскольку они близки по химической структуре и взаимосвязаны в процессах обмена. В ходе своего обмена глицин подвергается превращениям в другие аминокислоты, в компоненты нуклеиновых кислот, порфиринов, липидов и углеводов. Хотя глицин по своему строению является простейшей аминокислотой, его промежуточный обмен представляет крайне сложную картину.
Известно, что глицин относительно легко синтезируется в теле млекопитающих, а также у микроорганизмов и в растениях. Однако при определенных условиях цыплятам необходимо поступление глицина с пищей (стр. 122). К образованию глицина приводят различные реакции — расщепление серина (стр. 325), распад треонина на глицин и ацетальдегид (стр. 336), деметилирование саркозина (стр. 330), аминирование глиоксиловой кислоты (см. стр. 225). Эти реакции обнаружены в тканях животных. В процессе фотосинтеза меченая СО2 быстро входит в состав гликолевой кислоты и глицина; эти данные указывают на образование глицина из глиоксиловой кислоты [114]. Пути образования глицина у микроорганизмов детально не изучены. Однако имеются данные о взаимопревращении глицина и серина у ряда микробов [115, 116]. У Escherichia coli глиоксиловая кислота, по-видимому, не превращается в глицин [117], тогда как образование глицина, из серина, вероятно, имеет место [118—120].
Вайнхауз и сотрудники [121 —124] доказали, что в организме крыс происходит взаимопревращение глицина и глиоксиловой кислоты. Глицин, глиоксиловая и гликолевая кислоты быстро окисляются срезами печени крысы с образованием СО2, щавелевой кислоты и гиппуровой кислоты (последняя появляется в присутствии бензойной кислоты). При помощи метода «изотопной ловушки» было доказано превращение глицина в глиоксиловую кислоту в гомогенате печени крысы. Найдено, что щавелевая кислота образуется не прямо из глицина, а из глиоксиловой кислоты, в условиях, когда последняя присутствует в относительно больших концентрациях. Дальнейшими исследованиями выяснено, что в обычных условиях щавелевая кислота, вероятно, не образуется и что а-углеродные атомы глицина, гликолевой кислоты и глиоксиловой кислоты переходят в муравьиную кислоту.
Эти данные можно резюмировать следующим образом:
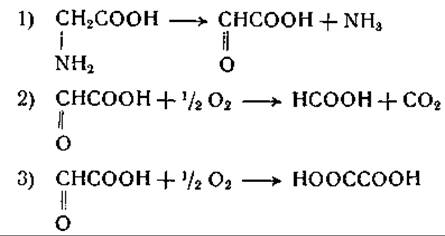
Реакция (3) может протекать при участии ксантиндегидрогеназы [125], а также другого фермента, найденного в печени голубя [123]. Реакция (2) может осуществляться неферментативным путем с участием перекиси водорода, а также под влиянием ферментной системы, детально еще не изученной. Превращение глицина в глиоксиловую кислоту происходит путем окислительного дезаминирования или переаминирования (стр. 226).
Доказано, что муравьиная кислота быстро окисляется в СО2:
НСООН + Н2О2 → СО2 + 2Н2О.
Эта реакция, наблюдаемая в растительных и животных тканях [126], может протекать за счет пероксидазной активности каталазы, с использованием перекиси водорода, образующейся в ходе других реакций [123].
Другие пути образования глиоксиловой кислоты (не из глицина) еще не вполне ясны. У некоторых бактерий глиоксиловая кислота образуется в результате расщепления изолимонной кислоты [127, 128]. В экстрактах из листьев шпината наблюдали образование глицина из рибозо-5-фосфата. При этом процессе в качестве промежуточных продуктов, по-видимому, образуются гликолевый альдегид, гликолевая и глиоксиловая кислоты [129—131].
Глиоксиловая кислота образуется также при действии глициноксидазы (стр. 192) на саркозин, согласно следующему уравнению:
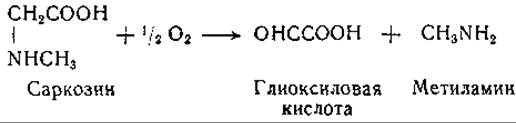
Физиологическое значение этой реакции и аналогичного превращения глицина подвергалось сомнению [132], так как эта оксидазная система действует, по-видимому, только при очень высокой концентрации субстрата. Глиоксиловая кислота образуется также при окислении этаноламина [123, 133] путем дезаминирования его с образованием гликолевого альдегида и дальнейшего окисления последнего.
Углеродные атомы глицина переходят в состав пуринов (стр. 283), порфирина (стр. 322), глутатиона [134] (стр. 268), гликохолевой кислоты, гиппуровой кислоты [135] (стр. 266) и креатина. Как установлено посредством изотопных опытов, синтез креатина происходит путем реакции трансамидинирования между аргинином и глицином и последующего метилирования гуанидинуксусной кислоты (гликоциамина) [136, 137] (стр. 372):
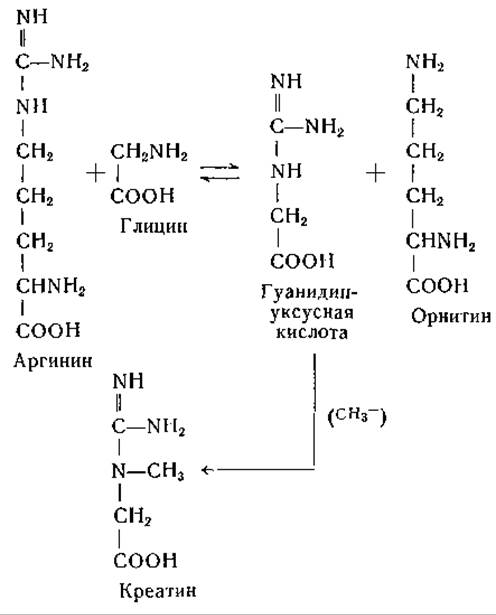
Недавно показано, что реакция трансамидинирования обратима [138]. Эта реакция происходит в почках, тогда как реакция переноса метальной группы протекает, преимущественно в печени. Для больных прогрессирующей мышечной дистрофией характерно выделение с мочой больших количеств креатина, обусловленное неспособностью мышц использовать креатин; выделяющийся с мочой креатин синтезируется не в мышцах, а в печени [139]. Фосфокреатин, образующийся в мышцах, по-видимому, является источником креатинина мочи; последний образуется путем циклизации с отщеплением фосфатной группы фосфокреатина [140]:
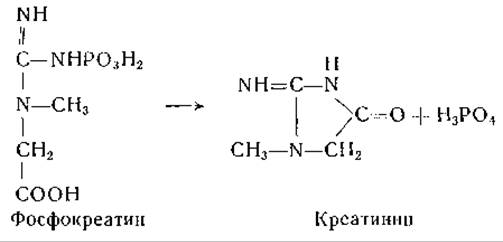
Синтез креатина, по-видимому, не обратим; так, например, метильная группа, вошедшая в состав креатина, уже не является подвижной. У человека потребление с пищей метионина и глицина не оказывает влияния на выделение креатинина с мочой. Интересно, что у цыпленка потребность в пищевом глицине (стр. 122) может быть снижена за счет креатина [141].
У Diplococcus glycinophilus наблюдали анаэробное превращение глицина в уксусную кислоту. На основании опытов с изотопами полагают, что при этом происходит конденсация двух молекул глицина с последующим отщеплением карбоксильных групп [142]. Один из штаммов Achromobacter окислял глицин с образованием аммиака и перекиси водорода [143]. Этот путь превращения глицина, по-видимому, аналогичен процессу его окисления в тканях млекопитающих с образованием глиоксиловой и муравьиной кислот в качестве промежуточных продуктов (см. также [144]).