Биохимия аминокислот - А. Майстер 1961
Промежуточный обмен аминокислот
Глицин, серин и саркозин
Синтез порфиринов
Несколько лет назад было найдено, что глицин является источником азота гемина [145]. Дальнейшие исследования показали, что а-углеродный атом глицина (но не карбоксильный углерод) также используется при синтезе гемина [146, 147]. Исследование продуктов разложения молекулы протопорфирина позволило в значительной мере раскрыть происхождение частей этой молекулы [148—150]. Было выяснено, что четыре атома углерода метановых мостиков и четыре атома углерода в пиррольных кольцах имеют источником а-углеродные атомы глицина. Было также изучено распределение изотопной метки в протопорфирине, образующемся из меченых промежуточных продуктов цикла лимонной кислоты [150, 151].
Шимин и сотрудники [152—155] нашли, что а-углеродные атомы глицина используются в равной степени для синтеза пиррольных колец и для образования метиновых мостиков. Они пришли к выводу, что эти углеродные атомы молекулы протопорфирина возникают за счет одного и того же производного глицина. Согласно схеме Шимина, «активный сукцинат»1 конденсируется с а-углеродным атомом глицина, причем образуется а-амино-β-кетоадипиновая кислота, которая декарбоксилируется и переходит в S-аминолевулиновую кислоту. Последняя может служить предшественником порфирина или подвергаться дезаминированию с образованием альдегида а-кетоглутаровой кислоты, который в свою очередь может превращаться в янтарную кислоту и одноуглеродное соединение, используемое для синтеза пуринов, серина и метальной группы метионина. При введении 5-С14-3-аминолевулиновой кислоты уткам метка была найдена в уреидных группах пуринов, в p-углеродном атоме серина и в метильной группе метионина.
При синтезе порфирина в эритроцитах утки δ-аминолевулиновая кислота [155—157] замещает «активный сукцинат» и глицин [152]. Кроме того, найдено, что при добавлении немеченой δ-аминолевулиновой кислоты в систему, синтезирующую гемин из радиоактивного глицина и янтарной кислоты, радиоактивность образующегося гемина снижается. В опытах с применением S-аминолевулиновой кислоты, меченной N15 или С14 в 5-положении, наблюдали интенсивное включение изотопов в гемин. Шимин и Рассел [152] высказали предположение, что при этом две молекулы 5-аминолевулиновой кислоты конденсируются с образованием соединения, являющегося предшественником пиррольных ядер порфирина (см. схему на стр. 324).
Позднее было найдено, что бесклеточные экстракты эритроцитов утки катализируют образование протопорфирина из 5-аминолевулиновой кислоты, но не образуют его из глицина и янтарной кислоты [153]. Таким образом, система, участвующая в процессе конденсации янтарной кислоты и глицина, нарушается при разрушении клеток. Наблюдения Шимина и сотрудников подтверждены другими исследователями [156, 158].
1 В настоящее время известно, что активным производным янтарной кислоты, участвующим в синтезе порфиринов, является сукцинил-кофермент А. — Прим. ред.
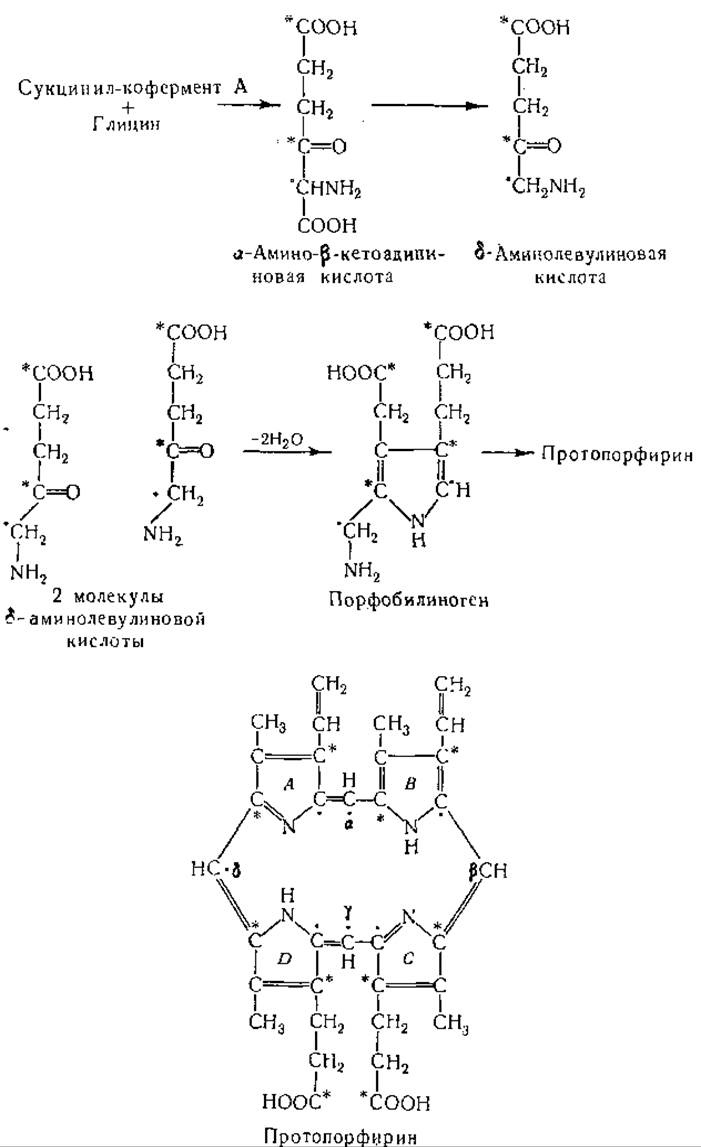
(Звездочками помечены углеродные атомы карбоксильных групп янтарной кислоты, точками — а-углеродные атомы глицина.)
Предполагаемый продукт конденсации двух молекул S-аминолевулиновой кислоты идентичен молекуле порфобилиногена [158—162], который выделяется с мочой у больных, страдающих острой порфирией [159]. Дальнейшие стадии превращения порфобилиногена в порфирины еще полностью не выяснены [163, 164]1.