БИОХИМИЯ - Л. Страйер - 1984
ТОМ 2
ЧАСТЬ II ГЕНЕРИРОВАНИЕ И ХРАНЕНИЕ МЕТАБОЛИЧЕСКОЙ ЭНЕРГИИ
ГЛАВА 14. ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ
14.7. Протоны выталкиваются асимметрично ориентированными трансмембранными комплексами
Генерирование протонного градиента при потоке электронов через три участка дыхательной цепи, в которых происходит запасание энергии, требует их асимметричной ориентации. Кроме того, три соответствующих ферментных комплекса должны располагаться на мембране таким образом, чтобы протоны могли перекачиваться со стороны матрикса на цитоплазматическую сторону. Изучению этих важных аспектов цепи переноса электронов в большой мере способствовало использование субмитохондриальных частиц, образующихся при озвучивании митохондрий (рис. 14.10). Наружная поверхность субмитохондриальных частиц соответствует обращенной к матриксу поверхности внутренней мембраны интактной митохондрии. Таким образом, обе поверхности внутренней митохондриальной мембраны - обращенная к цитоплазме поверхность в интактной митохондрии и обращенная к матриксу поверхность субмитохондриальных частиц-доступны экспериментальному исследованию. Расположение белковых компонентов дыхательной цепи в этих препаратах изучали, используя протеолитические ферменты, специфические антитела, лектины и не проникающие через мембраны меченые реагенты. Например, субъединицы II, V и VI цитохромоксидазы могут быть помечены только со стороны матрикса. Цитохромоксидаза связывает цитохром с исключительно на цитоплазматической поверхности и перекачивает протоны только в одном направлении. Эти эксперименты и аналогичные исследования, проведенные с NADH-Q-редуктазой и QН2-цитохром-с-редуктазой (табл. 14.2), показали, что все три запасающие энергию системы пронизывают насквозь внутренную митохондриальную мембрану и ориентированы асимметрично.
Таблица 14.2. Компоненты митохондриальной цепи переноса электронов
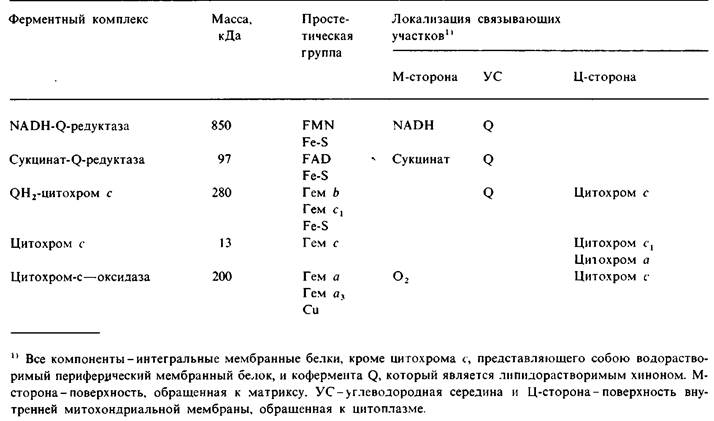
Рис. 14.10. Электронные микрофотографии. А - субмитохондриальная частица с выступами F1 на ее поверхности; Б-субмитохондриальная частица, обработанная мочевиной, удаляющей выступы F1; В-изолированные F1 и Г-реконструированная субмитохондриальная частица, образованная путем добавления F1 (фактора сопряжения) к «ободранным» мембранам. Частица, показанная на рис. Б, может переносить электроны на O2, но неспособна к образованию АТР. Реконструированная частица, показанная на рис. Г, осуществляет окислительное фосфорилирование
Откуда берутся транслоцируемые протоны? Одна из возможностей состоит в том, что это-протоны, которые непосредственно участвуют в химических реакциях, катализируемых указанными тремя системами. Например, когда NАDН передает два электрона на NАDН-Q-редуктазный комплекс, в этот процесс включаются два Н+ - один от самого NАDН и второй из растворителя. Согласно другому предположению, транслоцируемые протоны могут возникать непрямым путем, при конформационных взаимодействиях между каталитическим и белоксвязывающим центрами в различных участках ферментного комплекса. Стехиометрия реакций переноса электронов говорит о том, что только один протон в расчете на электрон или два протона на каждый запасающий энергию участок (пункт фосфорилирования) могут быть «перекачаны» посредством прямого механизма. В то же время отношение Н+/участок, запасающий энергию, находится, как оказалось, в интервале от 3 до 4, что не согласуется с прямым механизмом процесса. Представляется вероятным, что перенос электронов через каждый запасающий энергию участок вызывает перемежающиеся конформационные изменения, которые способствуют переходу протонов из матриксной стороны на цитоплазматическую сторону мембраны. Напомним, что протоны, участвующие в эффекте Бора в гемоглобине, поступают из участка молекулы, отдаленною от группы тема (разд. 4.16).
14.8. АТР синтезируется при обратном токе протонов в матрикс через протонные каналы
Обратимся теперь к использованию протонного градиента для синтеза АТР. Фермент, катализирующий этот процесс, выявляется на электронных микрофотографиях субмитохондриальных частиц в виде сферических выступов на поверхности (рис. 14.10). В интактных митохондриях такие выступы находятся на той стороне внутренней митохондриальной мембраны, которая обращена к матриксу. В 1960 г. Эфраим Рэкер (Efraim Racker) обнаружил, что эти округлые выступы (диаметром 85 А) можно удалить механическим встряхиванием. «Ободранные» субмитохондриальные частицы сохраняют способность к переносу электронов по своей цепи переноса электронов, но синтеза АТР при этом более не происходит. Отделившиеся же выступы диаметром 85 А катализируют гидролиз АТР. Но самым интересным в наблюдениях Рэкера оказался следующий факт: добавление таких АТРазных выступов к «ободранным» субмитохондриальным частицам восстанавливало их способность синтезировать АТР. Эти выступы называют сопрягающим фактором 1, или F1. Физиологическая роль F1 состоит в том, чтобы катализировать синтез АТР. АТРазная активность, проявляемая солюбилированным F1 (в отсутствие протонного градиента), результат обращения присущей ему физиологической реакции.
F1-компонент, масса которого составляет 360 кДа и который содержит пять видов полипептидных цепей (табл. 14.3), представляет собою только часть АТР-синтезирующего механизма митохондрий. Другой важный компонент этого комплекса - F0, гидрофобный сегмент из четырех полипептидных цепей, «заякореннный» на внутренней митохондриальной мембране. F0-этo протонный канал комплекса. «Стебелек» между F0 и F1включает некоторые другие белки (табл. 14.3). Один из них сообщает комплексу чувствительность к олигомицину, антибиотику, блокирующему синтез АТР путем нарушения использования протонного градиента.
Таблица 14.3. Компоненты АТР-синтезнрующего комплекса митохондрий

Ток протонов через канал F0 от цитоплазматической стороны мембраны к матриксу приводит к синтезу АТР, осуществляемому F1. Каким образом ток протонов оказывается сопряженным с синтезом АТР? Как и в случае перекачки протонов, здесь возможны прямой и непрямой механизмы. Существует предположение, что ток протонов непосредственно действует на реакцию синтеза АТР. Согласно этой схеме, Рi активируется и одновременно взаимодействует с ADP, образуя АТР. Существует и другое предположение, а именно что сопряжение тока протонов с синтезом АТР осуществляется путем конформационных изменений, передаваемых через ферментный комплекс.